Новую молекулу, способную бороться с нейропатическими болями при диабете, разработали специалисты ВолгГТУ в составе международного научного коллектива. По их словам, на сегодняшний день таких анальгетиков на рынке не существует. Результаты опубликованы в International Journal of Molecular Sciences.
Ингибирование растворимой эпоксидгидролазы (sEH) является многообещающей терапевтической стратегией лечения нейропатической боли. Эти ингибиторы эффективно уменьшают диабетическую нейропатическую боль и воспаление, что делает их подходящей альтернативой традиционным опиоидам.
Нейропатическая боль - это распространенная и тяжелая форма хронической боли, которая поражает значительную часть населения, среднего и старшего возраста, особенно людей с сахарным диабетом. Данную боль достаточно сложно лечить традиционными анальгетиками, таких как нестероидные противовоспалительные препараты или опиоиды. Вместо этого в качестве терапии первой и второй линии рекомендуются такие препараты, как габапентиноиды, трициклические антидепрессанты и ингибиторы обратного захвата серотонина и норадреналина. Однако эти методы лечения во многих случаях не обеспечивают адекватного облегчения боли для всех людей.
Нейропатическая боль может привести к снижению качества жизни, связанному со здоровьем, повлиять на повседневное функционирование и способствовать ряду сопутствующих заболеваний, влияющих не только на физическое здоровье, но также на психическое благополучие и социальные аспекты.
Растворимая эпоксидгидролаза (sEH) играет большую роль в метаболизме эпоксидно-жирных кислот (EpFAs), которые являются естественными сигнальными молекулами, участвующими в воспалительных и нейропатических путях боли. Было доказано, что в контексте нейропатической боли ингибирование sEH оказывает антиноцицептивное действие, то есть может уменьшить болевые ощущения.
Нейропатическая боль - это распространенная и тяжелая форма хронической боли, которая поражает значительную часть населения, среднего и старшего возраста, особенно людей с сахарным диабетом. Данную боль достаточно сложно лечить традиционными анальгетиками, таких как нестероидные противовоспалительные препараты или опиоиды. Вместо этого в качестве терапии первой и второй линии рекомендуются такие препараты, как габапентиноиды, трициклические антидепрессанты и ингибиторы обратного захвата серотонина и норадреналина. Однако эти методы лечения во многих случаях не обеспечивают адекватного облегчения боли для всех людей.
Нейропатическая боль может привести к снижению качества жизни, связанному со здоровьем, повлиять на повседневное функционирование и способствовать ряду сопутствующих заболеваний, влияющих не только на физическое здоровье, но также на психическое благополучие и социальные аспекты.
Растворимая эпоксидгидролаза (sEH) играет большую роль в метаболизме эпоксидно-жирных кислот (EpFAs), которые являются естественными сигнальными молекулами, участвующими в воспалительных и нейропатических путях боли. Было доказано, что в контексте нейропатической боли ингибирование sEH оказывает антиноцицептивное действие, то есть может уменьшить болевые ощущения.
Исследования показали, что ингибирование sEH может ослабить хроническую боль при таких состояниях, как диабетическая невропатия у мышей. Ингибирование sEH связано с усилением синаптической нейротрансмиссии и пластичности в префронтальной коре, что способствует ее анальгетическому эффекту. Кроме того, ингибиторы sEH были разработаны как потенциальные терапевтические средства для устранения воспаления и нейропатической боли без риска привыкания. Было показано, что EpFA, продуцируемые sEH, опосредуют перекрестную связь между воспалением, окислительным стрессом и инфламмасомой NLRP3, что подчеркивает терапевтический потенциал ингибиторов sEH при диабетических осложнениях. Понимание роли sEH и его модуляции в путях боли имеет решающее значение для разработки новых эффективных стратегий лечения нейропатической боли и улучшения результатов лечения пациентов.
Недавние достижения в области ингибиторов sEH показали многообещающие результаты как в доклинических, так и в клинических исследованиях. Ингибиторы sEH могут помочь поддерживать уровень эндогенной эпоксиэйкозатриеновой кислоты (EET), предлагая терапевтические преимущества при сердечно-сосудистых, неврологических и метаболических заболеваниях.
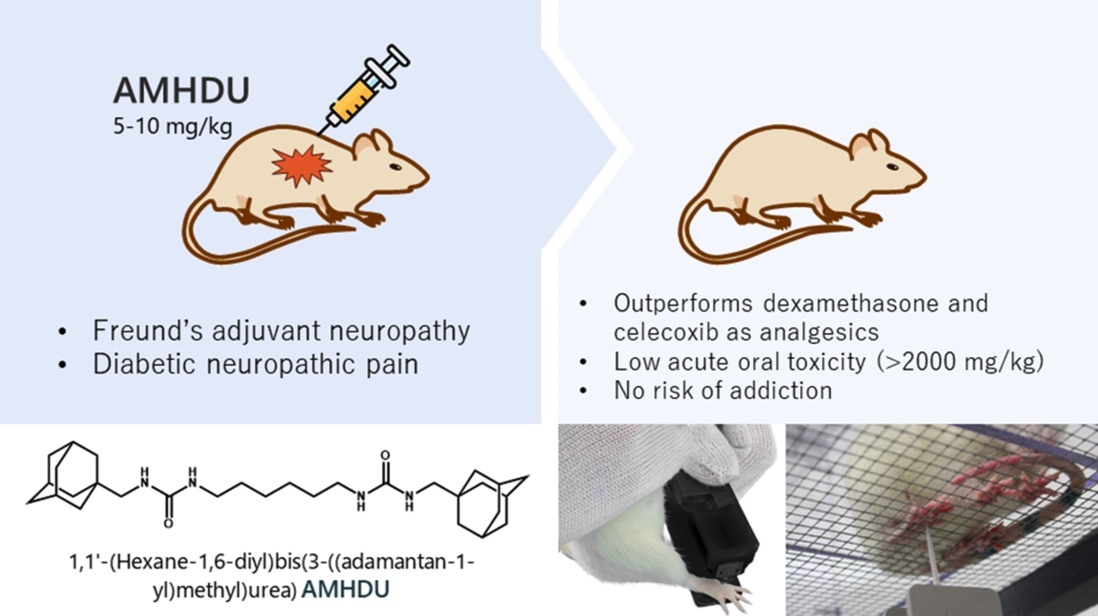
В данном исследовании было продемонстрировано выраженный анальгетический эффект соединения AMHDU на моделях воспалительной и диабетической нейропатии. Отсутствие противовоспалительной активности не характерно для ингибиторов sEH и может быть связано с быстрым клиренсом AMHDU, препятствующим его влиянию на экссудативную фазу воспаления.
- Некоторые из соединений, включают t -TUCB, который продемонстрировал эффективность в стимулировании поляризации макрофагов к противовоспалительным клеткам типа M2 и индукции печеночной аутофагии. Также многоцелевой ингибитор sEH в сочетании с ингибированием ЦОГ-2, продемонстрировал потенциал в условиях, когда эозинофилы и воспаление, связанное с болью, сосуществуют.
- Самое передовое соединение, EC5026, вступило в фазу клинических испытаний Ib в 2024 году, и до сих пор не было зарегистрировано никаких побочных эффектов.
В данном исследовании было продемонстрировано выраженный анальгетический эффект соединения AMHDU на моделях воспалительной и диабетической нейропатии. Отсутствие противовоспалительной активности не характерно для ингибиторов sEH и может быть связано с быстрым клиренсом AMHDU, препятствующим его влиянию на экссудативную фазу воспаления.
- Используя модель диабетической тактильной аллодинии наблюдали, что AMHDU сравним со стандартным габапентином по анальгетической активности, но в отличие от него не имеет потенциала привыкания.
- Низкая острая пероральная токсичность (LD 50 > 2000 мг/кг у крыс) и фармакологически активные дозы (5–30 мг/кг) указывают на высокий терапевтический индекс соединения.