Ген ZNF536 кодирует транскрипционный фактор с преимущественной экспрессией в нейронах коры и гиппокампа, а мутации в этом гене связаны с разными психическими расстройствами. Так, редкие de novo мутации с потерей функции белка (protein-truncating variants, PTV) ассоциированы с расстройствами аутистического спектра, тогда как полногеномные ассоциативные исследования (GWAS) идентифицировали общие интронные варианты, связанные с риском шизофрении.
Такая особенность мутаций и различия в наблюдаемых фенотипах указывают на необходимость детального изучения не только самого белка ZNF536, но и регуляторных элементов, расположенных в некодирующих областях этого гена. Понимание того, как полная потеря функции белка приводит к одному типу нарушений, а изменения в регуляции его активности - к другому, крайне важно для разработки персонализированных терапевтических подходов. А поскольку различные генетические дефекты могут требовать принципиально разных стратегий коррекции: от восстановления функции белка до модуляции его экспрессии или активности сигнальных путей, - обуславливает необходимость точной функциональной диагностики генетического варианта перед выбором метода терапии.
Учёные ФГБНУ «Научный центр психического здоровья», используя данные о структуре гена (рис.1) и технологию CRISPR/Cas9 создали клеточные нейрональные модели с различными типами мутаций гена ZNF536, которые воспроизводят как полную инактивацию гена, так и делецию интронных регуляторных элементов, обогащенных вариантами, ассоциированными с шизофренией.
Такая особенность мутаций и различия в наблюдаемых фенотипах указывают на необходимость детального изучения не только самого белка ZNF536, но и регуляторных элементов, расположенных в некодирующих областях этого гена. Понимание того, как полная потеря функции белка приводит к одному типу нарушений, а изменения в регуляции его активности - к другому, крайне важно для разработки персонализированных терапевтических подходов. А поскольку различные генетические дефекты могут требовать принципиально разных стратегий коррекции: от восстановления функции белка до модуляции его экспрессии или активности сигнальных путей, - обуславливает необходимость точной функциональной диагностики генетического варианта перед выбором метода терапии.
Учёные ФГБНУ «Научный центр психического здоровья», используя данные о структуре гена (рис.1) и технологию CRISPR/Cas9 создали клеточные нейрональные модели с различными типами мутаций гена ZNF536, которые воспроизводят как полную инактивацию гена, так и делецию интронных регуляторных элементов, обогащенных вариантами, ассоциированными с шизофренией.
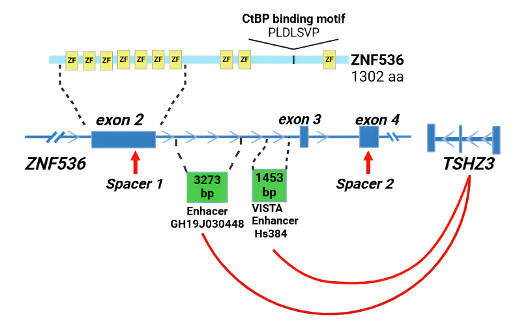
Рис. 1 Схема структуры гена ZNF536 и потенциальных энхансеров в интронной области
Функциональный анализ показал, что инактивация ZNF536 нарушает клеточный ответ на ретиноевую кислоту, приводя к дефектам роста нейритов и снижению экспрессии нейрональных маркеров. При этом различные типы мутаций демонстрируют различные молекулярные фенотипы: полная потеря функции вызывает глубокое нарушение программ дифференцировки, тогда как делеция интронных элементов приводит к промежуточному фенотипу с частичным сохранением функции (рис.2).
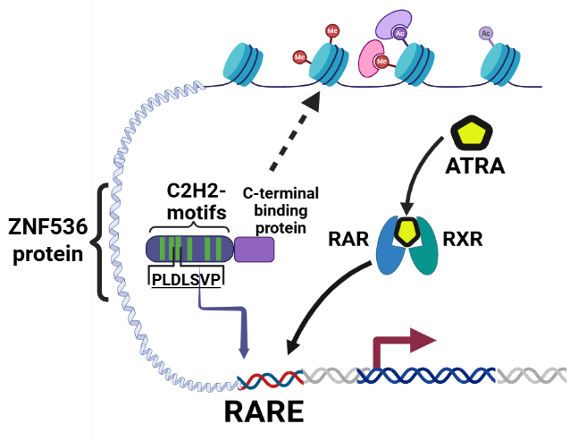
Выявленная связь ZNF536 с сигнальным путем ретиноевой кислоты открывает возможности для разработки фармакологических подходов, направленных на модуляцию этого пути или компенсаторных транскрипционных факторов. Создание характеризованных мутантных клеточных моделей в Биоресурсной коллекции «НейроРесурс» обеспечивает платформу для скрининга потенциальных терапевтических агентов, способных корректировать идентифицированные молекулярные нарушения с учётом конкретного типа генетического дефекта1.
1Созданные клеточные линии, моделирующие мутации в гене ZNF536, представляют собой ресурс для широкого круга исследователей, работающих в области нейробиологии и генетики, и доступны через Биоресурсную коллекцию «НейроРесурс». Исследование выполнено при поддержке Министерства науки и высшего образования Российской Федерации (Федеральная научно-техническая программа развития генетических технологий на 2019-2030 годы, Соглашение № 075-15-2025-474 от 29.05.2025).
1Созданные клеточные линии, моделирующие мутации в гене ZNF536, представляют собой ресурс для широкого круга исследователей, работающих в области нейробиологии и генетики, и доступны через Биоресурсную коллекцию «НейроРесурс». Исследование выполнено при поддержке Министерства науки и высшего образования Российской Федерации (Федеральная научно-техническая программа развития генетических технологий на 2019-2030 годы, Соглашение № 075-15-2025-474 от 29.05.2025).
Источник: Artemiy O. Kurishev, Dmitrii A. Abashkin, Dmitry S. Karpov, Ekaterina V. Marilovtseva, Yulia A. Chaika, Ekaterina V. Semina, Vera E. Golimbet; Schizophrenia risk gene ZNF536 modulates retinoic acid response and neuronal gene networks in SH-SY5Y cells; https://doi.org/10.3389/fnmol.2025.1671354




