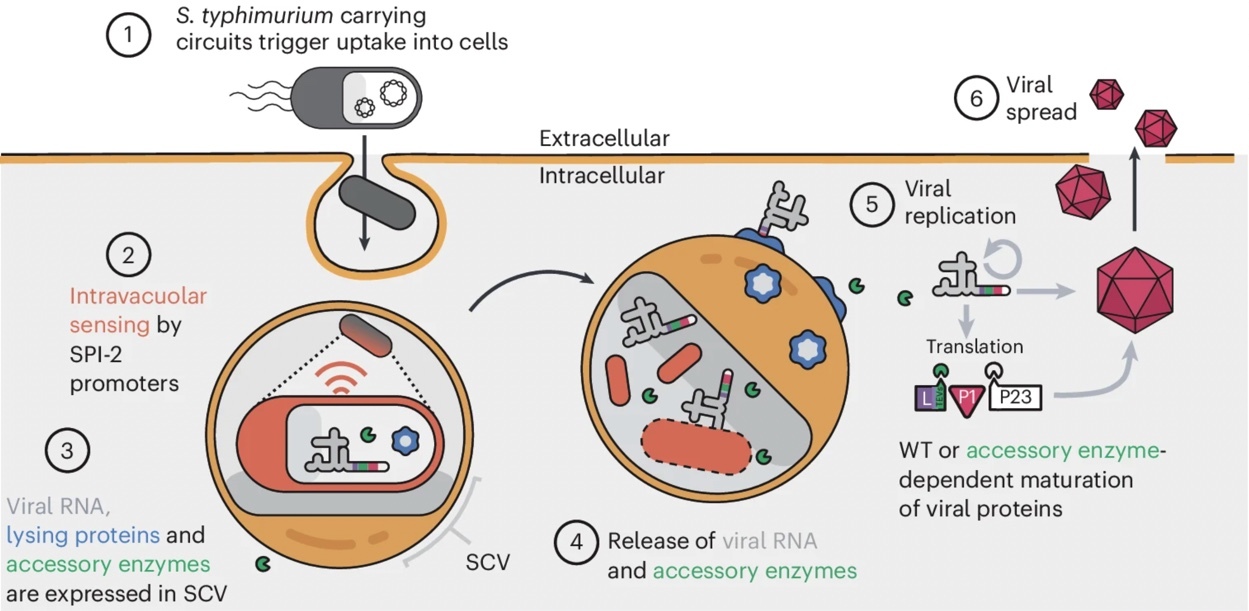
Рис (взят из статьи) 1-Штаммы S. typhimurium, несущие синтетические цепи, проникают внутрь клеток млекопитающих посредством естественных эффекторов, закодированных на островке патогенности сальмонеллы 1 (SPI-1). 2- Поглощённые клеткими S. typhimurium внутри вакуоли, содержащей сальмонеллу (SCV), ощущают внутривакуолярное пространство и инициируют активацию промоторов SPI-2. 3- Инженерные промоторы SPI-2 используются для запуска производства вирусных РНК (репликон полиовируса, сенекавирус А (SVA) или инженерный SVA), лизирующих белков гемолизин Е (HlyE) и белок E фага φX174, а также вспомогательного фермента. 4- После успешного разрушения бактерий и вакуоли вирусные РНК и вспомогательный фермент высвобождаются в цитоплазму хозяина. 5- Дикая форма (WT) вирусных РНК транслируется в цитоплазме и начинается репликация вируса. Полная зрелость вирусных частиц может требовать присутствия вспомогательного фермента.6- Инфекционные частицы выделяются в внеклеточное пространство для заражения соседних клеток. Поскольку бактерии S. typhimurium выполняют роль вирусного капсида, мы назвали платформу Координированная активность прокариота и пикорнавируса для безопасного интрацеллюлярного переноса (CAPPSID).
Компания Columbia Engineering сообщила о создании нового метода лечения рака, использующего модифицированную бактерию Salmonella typhimurium и онколитический вирус Seneca Valley Virus A (SVA). Эта технология получила название CAPPSIDE (Coordinated Activity of Prokaryote and Picornavirus for Safe Intracellular Delivery). Новый метод лечения, описанный в Nature Biomedical Engineering.
CAPPSIDE объединяет уникальные свойства обоих агентов: бактерия проникает внутрь гипоксических зон опухолей, доставляя туда вирус, который эффективно разрушает раковые клетки, избегая обнаружения иммунной системой хозяина. Такой подход решает проблему традиционной вирусной терапии, которая часто нейтрализуется иммунной защитой.
Принцип действия заключается в следующем: генетически модифицированная Salmonella typhimurium транспортирует и транслирует РНК-геном SVA внутри раковой клетки. После проникновения в опухоль бактерии погибают, освобождая вирус, который начинает реплицироваться и поражать раковые клетки. Для повышения безопасности и управляемости вирус был дополнительно адаптирован таким образом, что его жизненный цикл зависит от наличия особого фермента, выделяемого только самой бактерией.
Эффективность CAPPSIDE была доказана в экспериментах на мышах с имплантированным мелкоклеточным раком легких (SMCL). Результаты показали полное уничтожение опухолей у мышей с полноценной иммунной системой, несмотря на наличие антивирусных антител. Метод оказался эффективным как на человеческих, так и на мышиных клеточных культурах.
Технология обещает решить проблемы текущих подходов к борьбе с раком: бактерии сами направляются вглубь опухоли, обеспечивая доставку лечебных веществ прямо в очаг поражения, а онколитический вирус обеспечивает эффективную ликвидацию опухолевых клеток, минуя защитные барьеры иммунной системы.
Исследователи надеются, что их разработка повысит эффективность современных методик иммунотерапии, таких как CAR-T-терапия, усиливая локальные иммунные реакции и улучшая общие результаты лечения. Несмотря на значительные успехи, ученым предстоит провести дополнительные исследования, направленные на повышение стабильности и надежность методики, а также убедиться в её универсальности относительно различных типов рака и условий человеческого организма.
Следующим этапом станет адаптация платформы CAPPSIDE для широкого спектра опухолей и возможных лекарственных комбинаций, а также оценка возможности интеграции с бактериями, прошедшими клиническое тестирование на безопасность.
CAPPSIDE объединяет уникальные свойства обоих агентов: бактерия проникает внутрь гипоксических зон опухолей, доставляя туда вирус, который эффективно разрушает раковые клетки, избегая обнаружения иммунной системой хозяина. Такой подход решает проблему традиционной вирусной терапии, которая часто нейтрализуется иммунной защитой.
Принцип действия заключается в следующем: генетически модифицированная Salmonella typhimurium транспортирует и транслирует РНК-геном SVA внутри раковой клетки. После проникновения в опухоль бактерии погибают, освобождая вирус, который начинает реплицироваться и поражать раковые клетки. Для повышения безопасности и управляемости вирус был дополнительно адаптирован таким образом, что его жизненный цикл зависит от наличия особого фермента, выделяемого только самой бактерией.
Эффективность CAPPSIDE была доказана в экспериментах на мышах с имплантированным мелкоклеточным раком легких (SMCL). Результаты показали полное уничтожение опухолей у мышей с полноценной иммунной системой, несмотря на наличие антивирусных антител. Метод оказался эффективным как на человеческих, так и на мышиных клеточных культурах.
Технология обещает решить проблемы текущих подходов к борьбе с раком: бактерии сами направляются вглубь опухоли, обеспечивая доставку лечебных веществ прямо в очаг поражения, а онколитический вирус обеспечивает эффективную ликвидацию опухолевых клеток, минуя защитные барьеры иммунной системы.
Исследователи надеются, что их разработка повысит эффективность современных методик иммунотерапии, таких как CAR-T-терапия, усиливая локальные иммунные реакции и улучшая общие результаты лечения. Несмотря на значительные успехи, ученым предстоит провести дополнительные исследования, направленные на повышение стабильности и надежность методики, а также убедиться в её универсальности относительно различных типов рака и условий человеческого организма.
Следующим этапом станет адаптация платформы CAPPSIDE для широкого спектра опухолей и возможных лекарственных комбинаций, а также оценка возможности интеграции с бактериями, прошедшими клиническое тестирование на безопасность.