Доклад Совета Российской академии наук
Персонализированная медицина
cостояние научных исследований
и перспективы практического применения
Онкология
Введение
Бремя рака продолжает расти во всем мире, оказывая существенное давление на пациентов, их семьи, сообщества и системы здравоохранения. Рак представляет собой вторую по значимости причину смертности и заболеваемости в мире. По оценке ВОЗ, каждый пятый мужчина и каждая шестая женщина на планете заболеют раком на каком-либо этапе жизни. Изучение процессов канцерогенеза значительно улучшилось за последние два десятилетия, выявив огромные различия не только между типами злокачественных новообразований, но и между пациентами с одним и тем же типом рака. Благодаря этим знаниям противоопухолевое лечение все больше смещается в сторону прецизионных подходов, которые используют системные данные пациентов для принятия персонализированных решений о лечении.
Ключевые особенности прецизионной онкологии
Улучшение результатов лечения пациентов благодаря определению биомаркеров, определяющих оптимальное лечение, частоту ответов и риск побочных эффектов. Данные мета-анализа исследований II фазы, в которых изучалась частота объективного ответа, выживаемость без прогрессирования и общая выживаемость, показал, что пациенты, получавшие противоопухолевое лечение на основе прецизионных подходов, имели более высокие показатели объективного ответа и более низкий процент нежелательных явлений по сравнению с группами стандартного лечения. Прецизионные методы лечения в онкологии используются в более узких показаниях, за счет стремления к ограничению только в тех группах пациентов, которые с наибольшей вероятностью ответят на данный вид терапии.
- Например, одобрение и использование лекарственных средств, нацеленных на EGFR, привело к снижению смертности от рака легкого в США среди мужчин на 6,3 % в период с 2013 по 2016 гг. Опухоль-специфическая общая выживаемость увеличилась с 26 % среди мужчин с диагнозом мНМРЛ в 2001 г. до 35 % в 2014 г. Аналогичные закономерности были обнаружены среди женщин.
- Например, в Нидерландах более широкое использование прецизионной онкологии привело к сокращению продолжительности пребывания в стационаре онкологических больных, при этом средняя продолжительность пребывания в больнице составляет 3–4 дня для пациентов, получающих прецизионные методы лечения, по сравнению с 7 днями для пациентов, получающих стандартную химиотерапию.
- Исследование Французского института рака выявило потенциальную экономию средств, которую может обеспечить молекулярное тестирование за счет сокращения неэффективных назначений.
- Например, вложение 1,7 млн евро в тестирование мутации EGFR во Франции позволило сэкономить 70 млн евро за счет включения только пациентов с НМРЛ, которые ответили на лечение гефитинибом.
Основные направления мировых исследований в области прецизионной онкологии
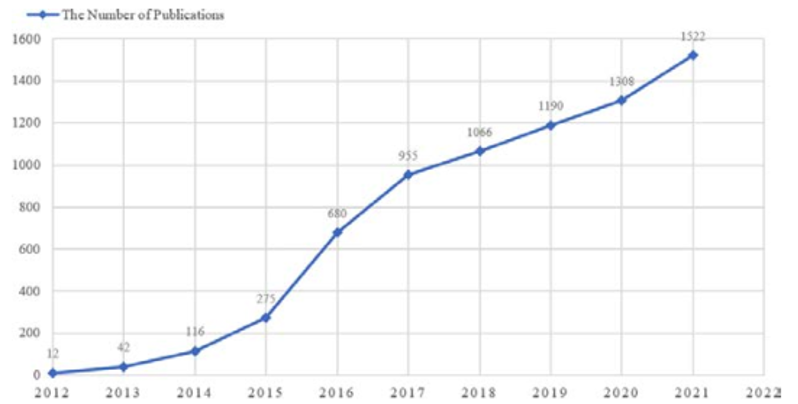
Рис. Увеличение количества публикаций по прецизионной онкологии за последние 10 лет
Важность исследований в области прецизионной онкологии подчеркивается увеличением количества публикаций по прецизионной онкологии за последние 10 лет
В 2018 г. правительство Канады объявило о двух новых крупных инвестициях в исследования в области геномики на общую сумму 255 млн дол. США от федерального правительства и правительств провинций, а также от исследовательских институтов и партнеров из частного сектора.
Precision Medicine Initiative® (PMI) – это инвестиции в размере 215 млн дол. в бюджет Национального института здравоохранения (NIH), направленные на ускорение биомедицинских исследований и предоставление клиницистам новых инструментов для выбора методов лечения, которые можно использовать в индивидуальном подходе к пациентам.
В 2018 г. правительство Канады объявило о двух новых крупных инвестициях в исследования в области геномики на общую сумму 255 млн дол. США от федерального правительства и правительств провинций, а также от исследовательских институтов и партнеров из частного сектора.
Precision Medicine Initiative® (PMI) – это инвестиции в размере 215 млн дол. в бюджет Национального института здравоохранения (NIH), направленные на ускорение биомедицинских исследований и предоставление клиницистам новых инструментов для выбора методов лечения, которые можно использовать в индивидуальном подходе к пациентам.
Таким образом, благодаря проводимым исследованиям и активному финансированию в прецизионной онкологии выделяют следующие направления:
- Развитие агностической таргетной терапии, основанное на генетических аномалиях в опухолях пациентов, независимо от типа рака.
- На основе секвенирования генома опухоли новые клинические испытания:иммунотерапия, тестирование новых комбинаций клеток, антител, малых молекул и лучевой терапии, наномоторов, представляющих собой молекулярные соединения («моторы»), адсорбированные на биослоях активированных ультрафиолетовым светом, со скоростью вращения от 2 до 3 млн оборотов в секунду. Открывая клеточные мембраны и запуская перемещение химических веществ в живые клетки и из них, наномоторы напрямую вызывают гибель клеток. Также разрабатываются планы по созданию консорциума научно-исследовательских учреждений для проведения более глубоких исследований иммунологических характеристик пациентов, получающих иммунотерапию.
- Исследование проблемы резистентности к лечению. Создание репозитория молекулярно-охарактеризованных резистентных образцов из биопсий пациентов. Создание пилотного заочного консорциума по лекарственной устойчивости.
- Разработка новых лабораторных моделей рака человека, основанное на значительном увеличении числа линий раковых клеток человека (выращенных в виде двумерных и трехмерных культур) и ксенотрансплантатов опухолей, полученных от пациентов для разработки лекарств.Запуск инициативы по моделированию рака человека в рамках открытия центров для создания и описания моделей линий раковых клеток нового поколения на основе первичной биопсии и обеспечения их широкого доступа научному сообществу. Пилотная разработка консорциума доклинических моделей.
- Создание консорциума моделей иммунотерапии собак для разработки другой модельной системы, которая может оказаться особенно полезной при изучении лимфом.
- Разработка национальной системы базы данных для размещения и интеграции геномной информации об опухолях с данными о клиническом ответе (например, уменьшение опухоли) и информацией о результатах (например, о продолжительности выживания) в качестве ресурса для ученых, медицинских работников и пациентов.
- Разработка единого масштабируемого репозитория данных о геномике рака, информации о пациентах и реакции на лечение, патологических и рентгенологических изображений и соответствующих доклинических данных.
Развитие успехов в области прецизионной онкологии, сотрудничество с пациентами по всей стране, которые участвуют в клинических испытаниях, спонсируемых национальными институтами онкологии, распространение принципов персонализированной медицины на фундаментальные научные исследования, деятельность в области биомедицинских информационных технологий, результаты организованных исследований позволяют быстрее и эффективнее, чем планировалось или предполагалось ранее, продвигать прецизионную онкологию в мире.
Schwaederle M. et al. Impact of precision medicine in diverse cancers: a meta-analysis of Phase II clinical trials // J Clin Oncol. 2015. 33(32), 3817-25.
Howlader N. et al. The effect of advances in lung-cancer treatment on population mortality // N Engl J Med. 2020. 383, 640–649.
CDDF, ECPC & EFPIA. Joint position paper on personalised oncology. 2019.
Nofziger C., Papaluca M., Terzic A. et al. Policies to aid the adoption of personalized medicine // Nat. Rev. Drug Discov. 2014. 13, 159–160.
Draghia-Akli R. Enabling personalized medicine in Europe: a look at the European Commission’s funding activities in the field of personalized medicine research // Per. Med. 2012. 9, 151–155.
Zhang B., Ao B., Lu X. et al. Global research trends on precision oncology: A systematic review, bibliometrics, and visualized study // Medicine (Baltimore). 2022 Oct 28;101(43):e31380. DOI: 10.1097/MD.0000000000031380. PMID: 36316889; PMCID: PMC9622693
Основные достижения персонализированной медицины в онкологии, примеры успешной реализации в мире
Трастузумаб является хорошо известным примером гуманизированных моноклональных антител IgG, используемого при лечении метастатического рака молочной железы, а также в адьювантных и неоадьювантных режимах, у пациенток с гиперэкспрессией онкогена HER2. HER2 отвечает за пролиферацию опухолевых клеток и имеет избыточную экспрессию у 20–25 % пациентов с раком молочной железы. Положительный статус HER2 свидетельствует о плохом прогнозе, но также является предиктором ответа на трастузумаб. В проведенных исследованиях показано, что трастузумаб, улучшает как безрецидивную выживаемость, так и общую выживаемость пациентов
Рецептор эпидермального фактора роста (EGFR) сверхэкспрессируется при многих эпителиальных раковых заболеваниях, что приводит к нарушению регуляции клеточной пролиферации и агрессивному фенотипу. Таким образом, ингибирование EGFR является многообещающей терапевтической стратегией в исследованиях прецизионной онкологии.
Цетуксимаб, моноклональное антитело, направленное против EGFR, доказал свою эффективность у пациентов мКРР, экспрессирующим KRAS, NRAS дикого типа, который кодирует нижестоящий эффектор EGFR, участвующий во внутриклеточной передаче сигналов. Рандомизированное исследование 572 пациентов мКРР, не отвечающих на стандартную химиотерапию, показало, что статус KRAS «дикого типа» предсказывал ответ на цетуксимаб с улучшением качества жизни и почти вдвое увеличивал общую выживаемость и выживаемость без прогрессирования по сравнению с пациентами с KRAS мутированного типа, получавшими лечение с помощью цетуксимаба.
Таким образом, цетуксимаб лицензирован для лечения мКРР, экспрессирующих ген KRAS дикого типа. Использование статуса KRAS в качестве предиктора ответа на ингибиторы EGFR при мКРР распространяется на другие виды рака, например, немелкоклеточный рак легкого (NSCLC).
Цетуксимаб, моноклональное антитело, направленное против EGFR, доказал свою эффективность у пациентов мКРР, экспрессирующим KRAS, NRAS дикого типа, который кодирует нижестоящий эффектор EGFR, участвующий во внутриклеточной передаче сигналов. Рандомизированное исследование 572 пациентов мКРР, не отвечающих на стандартную химиотерапию, показало, что статус KRAS «дикого типа» предсказывал ответ на цетуксимаб с улучшением качества жизни и почти вдвое увеличивал общую выживаемость и выживаемость без прогрессирования по сравнению с пациентами с KRAS мутированного типа, получавшими лечение с помощью цетуксимаба.
Таким образом, цетуксимаб лицензирован для лечения мКРР, экспрессирующих ген KRAS дикого типа. Использование статуса KRAS в качестве предиктора ответа на ингибиторы EGFR при мКРР распространяется на другие виды рака, например, немелкоклеточный рак легкого (NSCLC).
Существует два основных типа: немелкоклеточный (НМРЛ) и мелкоклеточный рак легкого (МРЛ). Мелкоклеточный составляет около 20 % всех случаев рака легкого. Рак, состоящий из обоих типов, называется смешанным мелкоклеточным/крупноклеточным раком. Из-за гистологической неоднородности лечить рак легкого крайне сложно.
На основании последних данных и понимания генетической основы рака легкого в качестве терапевтических мишеней используются EGFR, K-ras, ALK, MET, CBL и COX2. На основании этих мишеней в исследованиях продемонстрировано использование кризотиниба при лечении НМРЛ. Кризотиниб является ингибитором киназы анапластической лимфомы (ALK).
Эффективность эрлотиниба при лечении рака легкого с мутациями EGFR доказана в исследовании FLEX. Данные гистопатологического исследования и анамнеза больного также учитываются при оценке состояния заболевания и его агрессивности.
Ф. Найберг с соавторами, изучали связь между полиморфизмом олигонулеотидов и острым интерстициальным заболеванием легких у японцев, получающих лечение гефитинибом. Это исследование послужило основой для дальнейших исследований.
Обнаружено, что в китайской популяции полиморфизм ABCC1 связан с предрасположенностью к развитию рака легких у пациентов, проходящих химиотерапию.
Геномные вариации EGFR и ERCC1 также коррелируют с ответом на лекарственную противоопухолевую терапию у пациентов мелкоклеточным раком легкого.
На основании последних данных и понимания генетической основы рака легкого в качестве терапевтических мишеней используются EGFR, K-ras, ALK, MET, CBL и COX2. На основании этих мишеней в исследованиях продемонстрировано использование кризотиниба при лечении НМРЛ. Кризотиниб является ингибитором киназы анапластической лимфомы (ALK).
Эффективность эрлотиниба при лечении рака легкого с мутациями EGFR доказана в исследовании FLEX. Данные гистопатологического исследования и анамнеза больного также учитываются при оценке состояния заболевания и его агрессивности.
Ф. Найберг с соавторами, изучали связь между полиморфизмом олигонулеотидов и острым интерстициальным заболеванием легких у японцев, получающих лечение гефитинибом. Это исследование послужило основой для дальнейших исследований.
Обнаружено, что в китайской популяции полиморфизм ABCC1 связан с предрасположенностью к развитию рака легких у пациентов, проходящих химиотерапию.
Геномные вариации EGFR и ERCC1 также коррелируют с ответом на лекарственную противоопухолевую терапию у пациентов мелкоклеточным раком легкого.
В 2017 г. FDA также одобрило несколько новых иммунотерапевтических препаратов, направленных против лиганда рецептора программируемой клеточной гибели 1 (PD-L1) Т-лимфоцитов или рецептора запрограммированной клеточной смерти-1 (PD-1).
В отличие от терапии CAR Т-клетками, терапия ингибиторами контрольных точек иммунного ответа (PD-L1/PD-1) нацелена на эндогенный белок или рецептор PD-1, который представляет собой рецептор клеточной поверхности суперсемейства иммуноглобулинов экспрессируемых на Т-клетках и про-В-клетках.
PD-1 связывает два лиганда, PD-L1 и PD-L2. Доказано, что PD-1 и его лиганды ослабляют иммунные реакции, что может помешать иммунной системе девитализировать злокачественные клетки.
Ингибиторы PD-1 и PD-L1 разрабатываются в качестве препаратов первой линии против нескольких типов рака, включая метастатическую меланому, НМРЛ, почечно-клеточный рак, рак мочевого пузыря и лимфома Ходжкина.
В отличие от терапии CAR Т-клетками, терапия ингибиторами контрольных точек иммунного ответа (PD-L1/PD-1) нацелена на эндогенный белок или рецептор PD-1, который представляет собой рецептор клеточной поверхности суперсемейства иммуноглобулинов экспрессируемых на Т-клетках и про-В-клетках.
PD-1 связывает два лиганда, PD-L1 и PD-L2. Доказано, что PD-1 и его лиганды ослабляют иммунные реакции, что может помешать иммунной системе девитализировать злокачественные клетки.
Ингибиторы PD-1 и PD-L1 разрабатываются в качестве препаратов первой линии против нескольких типов рака, включая метастатическую меланому, НМРЛ, почечно-клеточный рак, рак мочевого пузыря и лимфома Ходжкина.
- Chapman P.B., Hauschild A., Robert C. Improved survival with vemurafenib in melaNoma with BRAF V600E mutation // N Engl J Med. 2011. 364: 2507–2516.
- Tsai J., Lee J.T., Wang W. Discovery of a Selective inhibitor of oncogenic B-Raf kinase with potent antimelanoma activity // Proc Natl Acad Sci USA. 2008. 105: 3041-3046.
Goldenberg M.M. Trastuzumab, a recombinant DNA-derived humanized monoclonal antibody, a Novel agent for the treatment of metastatic breast Cancer // Clin Ther. 1999. 21: 309–318.
- Piccart-Gebhart M.J., Procter M., Leyland-Jones B. et al. Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer // N Engl J Med. 2005;353:1659-72. DOI: 10.1056/NEJMoa052306
- Romond E.H., Perez E.A., Bryant J. et al. Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer // N Engl J Med 2005;353:1673-84. DOI: 10.1056/NEJMoa052122 -
- Perez E.A., Romond E.H., Suman V.J. et al. Four-year follow-up of trastuzumab plus adjuvant chemotherapy for operable human epidermal growth factor receptor 2-positive breast cancer: joint analysis of data from NCCTG N9831 and NSABP B-31 // J Clin Oncol 2011;29:3366-73. DOI: 10.1200/JCO.2011.35.0868
- Slamon D., Eiermann W., Robert N. et al. Adjuvant trastuzumab in HER2-positive breast cancer // N Engl J Med 2011;365:1273-83. DOI: 10.1056/NEJMoa0910383
- Untch M., Gelber R.D., Jackisch C. et al. Estimating the magnitude of trastuzumab effects within patient subgroups in the HERA trial // Ann Oncol. 2008;19:1090-6. DOI: 10.1093/annonc/mdn005
Wheeler D.L., Dunn E.F., Harari P.M. Understanding resistance to EGFR inhibitors-impact on future treatment strategies // Nat Rev Clin Oncol. 2010. 7: 493–507.
Karapetis C.S., Khambata F.S., Jonker D.J. K-ras mutations and benefit from cetuximab in advanced colorectal cancer // N Engl J Med. 2008. 359: 1757–1765.
Fearon E.R. Molecular genetics of colorectal cancer // Annu Rev Pathol. 2011. 6: 479–507.
Salgia R., Hensing T., Campbell N. et al. Personalized treatment of lung cancer // Semin Oncol. 2011. 38: 74–83.
Curran M.P. Crizotinib: in locally advanced or metastatic non-small cell lung cancer // Drugs. 2012. 72(1): 99–107.
- Ou S.H. Crizotinib: a novel and first-in-class multitargeting tyrosine kinase inhibitor for the treatment of anaplastic lymphoma kinase rearranged non-small cell lung cancer and beyond // Drug Des Devel Ther. 2011. 5: 471–485.
- Shaw A.T., Solomon B., Kenudson M.M. Crizotinib and testing for ALK // J Natl Compr Netw. 2011. 9: 1335–1341.
O’Byrne K.J., Gatzemeir U., Bondarenko I. et al. Molecular biomarkers in non-small cell lung cancer: a retrospective analysis of data from the phase III FLEX study // Lancet Oncol. 2011. 12: 795–805.
Nyberg F., Barratt B.J., Mushiroda T. et al. Interstitial lung disease in gefitinib treated Japanese patients with non-small cell lung cancer: genome-wide analysis of genetic data // Pharmacogenomics. 2011. 12: 965–977.
Yin J.Y., Han L.F., Huang Q. et al. ABCC1 polymorphism Arg723Gln (2168G - A) is associated with lung cancer susceptibility in a Chinese population // Clin Exp Pharmaco Physiol. 2011. 38:632–637.
- Wu J.Y., Shih J.Y., Chen K.Y. et al. Gefitinib therapy in patients with advanced non-small cell lung cancer with or without testing for epidermal growth factor receptor (EGFR) mutations // Medicine. 2011. 90: 159–167.
- Osawa K. SNPsin ERCC1 and drug response to cisplatin in non-small cell lung cancer patients // Pharmacogenomics. 2011. 12: 445–447.
Rizvi N. A. et al. Cancer immunology. Mutational landscape determines sensitivity to PD-1 blockade in non-small cell lung cancer // Science. 2015. 348, 124–128.
Iwai Y., Hamanishi J., Chamoto K., Honjo T. Cancer immunotherapies targeting the PD-1 signaling pathway // J. Biomed. Sci. (2017). 24, 26.
- Alsaab H.O. et al. PD-1 and PD-L1 checkpoint signaling inhibition for cancer immunotherapy: mechanism, combinations, and clinical outcome // Front. Pharmacol. 2017. 8, 561.
- Sunshine J., Taube J.M. PD-1/PD-L1 inhibitors // Curr. Opin. Pharmacol. 2015. 23, 32–38.
Прогнозирование ответа на терапию на основе статуса генной мутации позволяет проводить индивидуализированную терапию и имеет потенциальную экономическую выгоду за счет снижения непомерно высоких затрат на лечение. Таргетная терапия стоит дорого и нельзя недооценивать стоимость персонализированной медицины, особенно в эпоху существенной бюджетной экономии. Персонализированная медицина обеспечивает перспективу экономической выгоды для пациентов за счет ограничения расходов там, где это наиболее рентабельно, за счет того, что лекарства направляются туда, где они будут наиболее эффективными и наименее токсичными. Таким образом, затраты на лечение и осложнения могут быть уменьшены.
По мере того, как персонализированная медицина становится все более популярной и распространенной, лечение больных становится эффективнее. При использовании персонализированного лечения должно использоваться большее количество тестов, что в краткосрочной перспективе может дорого обходиться здравоохранению и страховым компаниям, но при долгосрочном планировании использование персонализированных методик будет выгодным, поскольку будет возможность более ранней диагностики заболевания, его рецидивов и прогрессирования.
Сейчас для принятия решения о лечении онколог должен взвесить не только возраст, состояние здоровья, образ жизни и цели каждого пациента, но и оценить гены и биологию злокачественного новообразования. Правительство должно играть активную роль в быстром утверждении персонализированных медицинских тестов и создавать стимулы для их использования.
По мере того, как персонализированная медицина становится все более популярной и распространенной, лечение больных становится эффективнее. При использовании персонализированного лечения должно использоваться большее количество тестов, что в краткосрочной перспективе может дорого обходиться здравоохранению и страховым компаниям, но при долгосрочном планировании использование персонализированных методик будет выгодным, поскольку будет возможность более ранней диагностики заболевания, его рецидивов и прогрессирования.
Сейчас для принятия решения о лечении онколог должен взвесить не только возраст, состояние здоровья, образ жизни и цели каждого пациента, но и оценить гены и биологию злокачественного новообразования. Правительство должно играть активную роль в быстром утверждении персонализированных медицинских тестов и создавать стимулы для их использования.
- Например, в США в марте 2007 г. Конгрессу был представлен Закон о геномике и персонализированной медицине, охватывающий научные барьеры, неблагоприятное рыночное давление и нормативные препятствия. Благодаря этому, в 2009 г. решено было потратить 19 млрд дол. на модернизацию национальных медицинских информационных технологий и создание электронных медицинских карт, для обеспечения более эффективного и действенного использования данных генетического тестирования и снижения затрат на здравоохранение.
S. 976 (110th): Genomics and Personalized Medicine Act of 2007. URL: https://www.govtrack.us/congress/bills/110/s976
Chanley T. Howell. Stimulus Package Contains $19 Billion for Health Care Technology Spending and Adoption of Electronic Health Records. URL: https://www.foley.com/en/insights/publications/2009/02/stimulus-package-contains-19-billion-for-health-ca
Перечень зарегистрированных в мире ЛП или изделий, которые внедрены и имеют персонализированные показания к применению
Благодаря достижениям в области прецизионной онкологии иммунотерапия была названа в ежегодном отчете ASCO о прогрессе в борьбе со злокачественными новообразованиями «Общественным достижением года». Исследователи годами пытались использовать иммунную систему для лечения рака, но без особого успеха, пока недавно не были обнаружены ингибиторы иммунных контрольных точек (PD-1/PD-L1) и разработана CAR-Т-клеточная терапия.
PD-1/PD-L1
В клинической практике одобрено несколько PD-1 ассоциированных препаратов, включая авелумаб, дурвалумаб и ниволумаб.
- Авелумаб (Бавенсио) представляет собой блокирующее PD-L1 моноклональное антитело для лечения местно-распространенной, метастатической уротелиальной карциномы у пациентов, у которых заболевание не прогрессировало после химиотерапии, содержащей препараты платины и для пациентов метастатической карциномой из клеток Меркеля, в возрасте 12 лет и старше.
- Дурвалумаб (Имфинзи) получил ускоренное одобрение в мире для лечения нерезектабельного местно-распространенного немелкоклеточного рака легкого у взрослых пациентов, не прогрессирующих после химиолучевой терапии на основе препаратов платины.
- Ниволумаб (Опдиво), моноклональное антитело к PD-1 для адъювантного лечения пациентов с метастазами меланомы в лимфатические узлы или пациентов с метастатической меланомой, перенесших радикальную резекцию. Первоначально ниволумаб был одобрен для лечения пациентов с нерезектабельной или метастатической меланомой.
- Пембролизумаб (Кейтруда) одобрен для лечения классической лимфомы Ходжкина (ХЛ) у взрослых и детей с рефрактерной ХЛ или у пациентов с рецидивом после трех или более предыдущих линий лечения. Также препарат одобрен в качестве комбинированной терапии первой линии с пеметрекседом и карбоплатином для пациентов с метастатическим неплоскоклеточным НМРЛ, независимо от экспрессии PD-L1, местно-распространенной или метастатической уротелиальной карциномой, которые прогрессировали после лечения препаратами, содержащими платину.
CAR-Т-клеточная терапия
В августе 2017 г. FDA одобрило первую адоптивную клеточную иммунотерапию (т. е. CAR-Т-клеточную терапию) и первую генную терапию рака – Тисагенлеклейсел. Раковые клетки разработали защиту для уклонения от обнаружения и уничтожения их иммунными клетками. Т-клеточная терапия химерным антигенным рецептором (CAR) – это тип адоптивной клеточной иммунотерапии, при котором собственные иммунные клетки пациента генетически перепрограммируются для обнаружения и уничтожения раковых клеток по всему телу. - -
- Тисагенлеклейсел (Tisagenlecleucel (Kymriah)) представляет собой генетически модифицированную аутологичную Т-клеточную иммунотерапию или CAR Т-клеточную терапию, направленную против антигенов кластера дифференцировки 19 (CD19) при В-клеточном остром лимфобластном лейкозе (ОЛЛ). CD19 расположен на поверхности В-линейных клеток, и, когда он связывается с рецептором антигена на В-лимфоцитах, снижает уровень активации, зависимой от рецептора антигена.
Конъюгаты антитело-лекарственные средства
Конъюгаты антитело-лекарственное средство (ADC) были разработаны как сильнодействующие таргетные препараты против различных видов рака. Назначение этих препаратов состоит в том, чтобы щадить нормальные клетки, в то же время целенаправленно воздействовать на злокачественные клетки.
Эти сложные молекулы состоят из цитотоксического противоракового препарата, связанного с антителом, которое специфически и идеально нацелено на белковый онкомаркер, обнаруженный только на раковых клетках. Антитело прикрепляется к белку-мишени на поверхности раковой клетки, что вызывает клеточный ответ, при котором антитело и лекарство поглощаются раковой клеткой, где лекарство высвобождается, вызывая апоптоз клетки.
Для клинического использования недавно было одобрено три новых ADC: брентуксимаб ведотин, сацитузумаб говитекан и трастузумаб дерукстекан.
Эти сложные молекулы состоят из цитотоксического противоракового препарата, связанного с антителом, которое специфически и идеально нацелено на белковый онкомаркер, обнаруженный только на раковых клетках. Антитело прикрепляется к белку-мишени на поверхности раковой клетки, что вызывает клеточный ответ, при котором антитело и лекарство поглощаются раковой клеткой, где лекарство высвобождается, вызывая апоптоз клетки.
Для клинического использования недавно было одобрено три новых ADC: брентуксимаб ведотин, сацитузумаб говитекан и трастузумаб дерукстекан.
- Брентуксимаб ведотин избирательно воздействует на CD30, который высоко экспрессируется при лимфоме Ходжкина. Этот ADC в настоящее время используется в сочетании с химиотерапией в качестве терапии первой линии у пациентов с прогрессирующей ХЛ. ADC сацитузумаб говитекан нацелен на антиген поверхности клеток трофобласта (Trop-2) и селективно доставляет высокие дозы SN-38, активного метаболита ингибитора топоизомеразы 1, иринотекана. SN-38 в 1000 раз более активен, чем иринотекан. Сацитузумаб говитекан одобрен для интенсивно предлеченных пациентов трижды негативным метастатическим раком молочной железы.
- Трастузумаб дерукстекан одобрен для лечения пациентов с HER2-положительным, местно-распространенным или метастатическим раком молочной железы, получавших лечение трастузумабом (Герцептин), пертузумабом (Перьета) и адо-трастузумабом эмтанзином
Циклин-зависимые киназы CDK4 и CDK6
Циклин-зависимые киназы CDK4 и CDK6 (CDK4/6) обычно не регулируются и чрезмерно активируются во многих типах раковых клеток. Большой интерес был сосредоточен на разработке ингибиторов CDK4/6 для ослабления сигнальных путей роста и восстановления контроля клеточного цикла в раковых клетках. CDK4/6 взаимодействуют с циклином D, который синтезируется в начале G1. Комплекс циклин/CDK управляет продвижением клеточного цикла от G1 к S-фазе. Ингибиторы блокируют эти киназы, чтобы остановить переход клеток из фазы G1 в фазу S.
- В 2017 г. FDA одобрило рибоциклиб (Кискали) в сочетании с ингибитором ароматазы для лечения женщин в постменопаузе с распространенным или метастатическим HER2-отрицательным раком молочной железы, положительным по рецепторам гормонов.
- Впоследствии абемациклиб (Верзенио) был одобрен для использования в комбинации с фулвестрантом, селективным деструктором рецепторов эстрогена (SERD), у аналогичных пациентов, но прогрессироваших после предшествующего лечения.
Фермент PARP
Фермент PARP важен для восстановления одиночных разрывов ДНК, а ингибиторы PARP предотвращают восстановление ДНК, что приводит к гибели клеток. Три ингибитора PARP были одобрены для клинического применения: олапариб, рукапариб и нирапариб.
- Олапариб и рукапариб используются у пациентов с раком яичников с мутацией BRCA, которые ранее получали химиотерапию.
- Нирапариб используется в качестве поддерживающей терапии у пациентов с чувствительным к платине рецидивирующим раком яичников, у которых есть ответ на химиотерапию на основе платины, независимо от статуса BRCA или гомологичной рекомбинации опухоли. Несколько исследований показали эффективность олапариба при раке молочной железы и предстательной железы.
Lyons Y.A., Wu S.Y. Overwijk, W. W. Baggerly, K. A. & Sood, A. K. Immune cell profiling in cancer: molecular approaches to cell-specific identification // npj Pre-cision Oncol. 2017. 1, 26. DOI: 10.1038/s41698-017-0031-0
Shin S.H., Bode A.M., Dong Z. Addressing the challenges of applying precision oncology // npj Precision Oncol. 2017. 1, 28. DOI: 10.1038/s41698-017-0032-z
Chen A. PARP inhibitors: its role in treatment of cancer // Chin J Cancer. 2011 Jul;30(7):463-71. DOI: 10.5732/cjc.011.10111. PMID: 21718592; PMCID: PMC4013421
Эти одобрения являются отражением множества новаторских изменений в лечении рака и готовности онкологов обеспечить более быстрый доступ пациентов к этим жизненно важным методам лечения. В то же время безопасность и нецелевая токсичность, а также развитие резистентности являются основными проблемами, которые необходимо учитывать. Важные вопросы, которые необходимо решить: Почему одни пациенты реагируют, а другие нет? Почему некоторые пациенты сначала реагируют на лечение, но в конечном итоге у них развивается резистентность? Одной из самых больших проблем является идентификация отдельных белков в раковых клетках, на которые можно целенаправленно воздействовать, не нанося вреда нормальным клеткам.
Состояние персонализированной онкологии в России
Несмотря на большое количество проводимых исследований, многие из них находятся в стадии доклинического изучения. Однако представленные результаты имеют высокую потенциальную научную ценность.
- Следует отметить большое количество научно-исследовательских организаций, вовлеченных в проведение исследований в области персонализированной онкологии. Основное направление отечественных исследований в данной сфере связано с разработкой подходов к выбору индивидуального плана лечения при помощи современных методов диагностики.
- В России разработаны подходы к назначению лечения на основе фенотипических и генетических особенностей опухолей с использованием иммунотерапии и таргетных препаратов. Разрабатываются отечественные препараты, в том числе в рамках программ импортозамещения. Разрабатываются решения для выявления молекулярно-генетических особенностей опухоли с помощью методов секвенирования нового поколения – полноэкзомного и полногеномного секвенирования, RNASeq. Развитие данных технологий в онкологии поддерживается из средств федерального бюджета и грантов. Работы по данному направлению согласуются с новейшими зарубежными исследованиями, а результаты исследований находят отражение в современных клинических рекомендациях, руководствах для врачей и монографиях.
- На основе методов секвенирования нового поколения и анализа геномных данных ведутся работы по выявлению молекулярно-генетических предикторов радиочувствительности и радиорезистентности злокачественных новообразований, индивидуальных особенностей метастазирования опухолей.
- В то же время ведутся исследования, посвященные изучению и преодолению лекарственной устойчивости. Такие работы носят фундаментальный характер и составляют перспективную основу для многих других направлений, связанных с разработкой новых методов диагностики и лечения злокачественных новообразований, формированию персонализированных подходов к терапии с учетом индивидуальных генетических особенностей опухоли.
- Ведутся исследования в области применения CAR-T терапии, терапевтических вакцин и онколитических вирусов. Однако их использование в клинической практике единично из-за отсутствия необходимой правовой базы и доступных препаратов. Для дальнейшей оценки возможной эффективности данных методов необходимо проведение экспериментов на животных и клинических исследований.
- Развивающимся направлением диагностики и выявления индивидуальных особенностей опухолей является определение циркулирующих кольцевых ДНК, нуклеиновых кислот, ДНК аптамеров в биологических жидкостях. Однако возможность применения данных технологий требует оценки в рамках клинических исследований
- Использование тераностических возможностей является перспективным для развития прецизионной онкологии. Ведутся исследования в области радиологии, посвященные возможности лечебно-диагностического применения радиофармпрепаратов, но в России подобные исследования находятся на начальном уровне.
- Важным компонентом ПМ является разработка систем помощи принятия врачебных решений, применение систем искусственного интеллекта и машинного обучения для обработки медицинских данных и формирования индивидуального прогноза в клинической практике. В отечественной онкологии применение подобных систем находится на начальном уровне. В настоящее время ведущими научными учреждениями созданы программы для ЭВМ, разрабатываются способы их практического применения. Разработка и внедрение подобных систем является компонентом цифровизации здравоохранения и может способствовать повышению качества медицинской помощи.
- Перспективы развития персонализированной онкологии связаны с внедрением технологий диагностики на основе анализа омиксных данных – исследования протеома и метаболома опухоли. Данное направление активно развивается в России и мире, однако анализ омиксных данных требует применения дорогостоящего оборудования, разработки технологических решений для внедрения в практику, что может явиться ограничением для развития омиксных технологий в России.
Таким образом, в рамках прецизионной онкологии возможно внедрение новых методов диагностики и лечения онкологических заболеваний. В настоящее время наиболее широко исследуются способы применения иммуно- и таргетной терапии в зависимости от молекулярно-генетических и фенотипических особенностей опухоли.
В России активно развиваются геномные технологии, что способствует повышению качества диагностики. Для дальнейшего развития отрасли необходима разработка новых таргетных препаратов, в том числе с использованием импортозамещающих технологий.
Перспективными разделами прецизионной онкологии является применение CAR-T терапии, терапевтических вакцин и онколитических вирусов, омиксных технологий и систем искусственного интеллекта, однако их развитие в России требует дополнительных инвестиций.
Опубликованы свидетельства о регистрации программ для ЭВМ, предназначенных для прогнозирования развития клинических состояний, однако разработка способов их клинического применения находится на начальном уровне.
В России активно развиваются геномные технологии, что способствует повышению качества диагностики. Для дальнейшего развития отрасли необходима разработка новых таргетных препаратов, в том числе с использованием импортозамещающих технологий.
Перспективными разделами прецизионной онкологии является применение CAR-T терапии, терапевтических вакцин и онколитических вирусов, омиксных технологий и систем искусственного интеллекта, однако их развитие в России требует дополнительных инвестиций.
Опубликованы свидетельства о регистрации программ для ЭВМ, предназначенных для прогнозирования развития клинических состояний, однако разработка способов их клинического применения находится на начальном уровне.
Предложения по перспективному планированию:
- Объединить усилия университетов и исследовательских центров по разработке персонализированных подходов в диагностике, лечении и профилактике онкологических заболеваний с привлечением финансовых ресурсов (грантов, государственных программ).
- Развитие и клиническая валидация CAR-T терапии, терапевтических вакцин и онколитических вирусов с привлечением ведущих специалистов в области биотехнологии и разработки вакцин, лекарственного лечения онкологических заболеваний.
- Разработка и клиническая валидация новых таргетных лекарственных препаратов, в том числе с привлечением импортозамещающих технологий на базе ведущих профильных центров с привлечением фармкомпаний.
- Развитие и внедрение в клиническую практику геномных и информационных технологий, позволяющих формировать индивидуальный прогноз и план лечения пациента, в том числе на основе генетических и фенотипических особенностей опухоли. Разработка подходов к применению омиксных технологий для диагностики и выбора тактики лечения онкологических заболеваний. Применение технологий изучения и редактирования генома, обработки клинических данных с использованием систем искусственного интеллекта позволит повысить эффективность лечения онкологических больных.
- Создание новых и совершенствование существующих образовательных программ по прецизионной онкологии, подготовка квалифицированных кадров, стажировка и повышение квалификации сотрудников, привлечение и закрепление ведущих ученых и перспективных молодых специалистов в области персонифицированной медицины. Включение в программы подготовки врачей-онкологов изучение персонализированного подхода в онкологии. Проведение профильных научно-практических конференций, симпозиумов и круглых столов.
Болезни системы кровообращения
Основные направления мировых исследований
Актуальность исследований по ПМ, проводимых по направлению «Болезни системы кровообращения» (БСК), определяют: большая гетерогенность популяции кардиологических пациентов, многофакторная этиология, сложные патогенетические механизмы развития и прогрессирования патологии, присутствие высокой коморбидности и острая потребность в персонализации терапии на фоне роста числа медикаментозных и немедикаментозных методов лечения.
В аспекте персонализированных подходов к оказанию медицинской помощи при БСК определяются несколько направлений, включающих:
В аспекте персонализированных подходов к оказанию медицинской помощи при БСК определяются несколько направлений, включающих:
- оценку индивидуального риска развития и прогрессирования заболеваний БСК на основе идентификации молекулярно-генетических маркеров и других биомаркеров;
- применение персонализированных методов лечения заболеваний и коррекции состояний, в том числе персонализированное применение лекарственных препаратов, основанное на анализе генетических особенностей и биомаркеров;
- использование биомаркеров для мониторинга эффективности лечения и оценки прогноза пациента;
- персонализированные информационные технологи в медицине с использованием вычислительных инструментов и искусственного интеллекта.
Основные достижения персонализированной медицины в БСК и примеры успешной реализации в мире
Учитывая гетерогенность заболеваний в структуре БСК, успех и перспективы ПМ крайне различаются, в зависимости от вклада генетического компонента в патогенез заболевания.
Наследственные и генетически-обусловленные заболевания в кардиологии являются той группой патологий, в отношении которой, наверное, в наибольшей степени стало актуально применение принципов персонифицированного подхода. Это произошло благодаря появлению новых прорывных технологий секвенирования генома и разработке сложных алгоритмов биоинформатического анализа, построенных на обработке Big Data, что в совокупности позволило приблизить к реальной клинической практике применение знаний относительно генетической природы наследственных заболеваний сердца.
При этом речь идет не только о выделении конкретного генетического дефекта и сигнального пути, участвующего в развитии болезни, но и о выяснении путей модуляции активности белков – участников данного сигнального пути и, соответственно, определении новых терапевтических подходов.
Наследственные и генетически-обусловленные заболевания в кардиологии являются той группой патологий, в отношении которой, наверное, в наибольшей степени стало актуально применение принципов персонифицированного подхода. Это произошло благодаря появлению новых прорывных технологий секвенирования генома и разработке сложных алгоритмов биоинформатического анализа, построенных на обработке Big Data, что в совокупности позволило приблизить к реальной клинической практике применение знаний относительно генетической природы наследственных заболеваний сердца.
При этом речь идет не только о выделении конкретного генетического дефекта и сигнального пути, участвующего в развитии болезни, но и о выяснении путей модуляции активности белков – участников данного сигнального пути и, соответственно, определении новых терапевтических подходов.
К перспективным с точки зрения разработки таргетной терапии механизмам развития заболевания относится чрезмерная вовлеченность миозина в сократительную активность при гипертрофической кардиомиопатии (ГКМП) – в нормальном миокарде в покое вовлечено около 10 % молекул миозина, при наличии саркомерных мутаций – основной причины заболевания, их количество резко возрастает, что и приводит к гипертрофии миокарда. Ингибирование миозина оказалось эффективным лечебным воздействием, уменьшающим степень гипертрофии и обструкции выносящего тракта левого желудочка сердца. Патологическая гипертрофия при так называемых фенокопиях ГКМП развивается совершенно иначе.
Расопатии – группа наследственных заболеваний, проявляющихся в детском возрасте и являющихся следствием нарушений в сигнальном пути Ras/MARK, при которых, кроме выраженной гипертрофии миокарда (чаще бивентрикулярной), у больных фиксируются признаки дисэмбриогенеза. При редком рецессивном гликогенозе 2-го типа (болезнь Помпе) увеличение толщины стенки миокарда развивается за счет накопления гликогена вследствие дефекта гена GAA. Похожим образом развивается гипертрофия миокарда при другой болезни накопления – болезни Данона, связанной с дефектом гена LAMP2, кодирующего одноименный лизосомальный фермент. Все эти сведения активно исследуются в отношении разработки таргетного лечения.
Выявление патологической гипертрофии миокарда во многих случаях требует постановки генетического диагноза для выявления заболеваний, имеющих специфическое лечение (болезнь Данона, Фабри, амилоидоз и т.д.). С точки зрения прогнозирования течения болезни с использованием омиксных технологий до настоящего времени не получено результатов, готовых к внедрению в клинику, однако подобные исследования активно проводятся.
Перспективным направлением представляется профилирование микроРНК больных ГКМП, позволяющее выявить дефектные гены, ответственные за развитие заболевания. Эти данные могут позволить разработать недорогой способ выявления дефектных генов.
Расопатии – группа наследственных заболеваний, проявляющихся в детском возрасте и являющихся следствием нарушений в сигнальном пути Ras/MARK, при которых, кроме выраженной гипертрофии миокарда (чаще бивентрикулярной), у больных фиксируются признаки дисэмбриогенеза. При редком рецессивном гликогенозе 2-го типа (болезнь Помпе) увеличение толщины стенки миокарда развивается за счет накопления гликогена вследствие дефекта гена GAA. Похожим образом развивается гипертрофия миокарда при другой болезни накопления – болезни Данона, связанной с дефектом гена LAMP2, кодирующего одноименный лизосомальный фермент. Все эти сведения активно исследуются в отношении разработки таргетного лечения.
Выявление патологической гипертрофии миокарда во многих случаях требует постановки генетического диагноза для выявления заболеваний, имеющих специфическое лечение (болезнь Данона, Фабри, амилоидоз и т.д.). С точки зрения прогнозирования течения болезни с использованием омиксных технологий до настоящего времени не получено результатов, готовых к внедрению в клинику, однако подобные исследования активно проводятся.
Перспективным направлением представляется профилирование микроРНК больных ГКМП, позволяющее выявить дефектные гены, ответственные за развитие заболевания. Эти данные могут позволить разработать недорогой способ выявления дефектных генов.
Попытка воздействия на аналогичный с ГКМП миозиновый механизм не увенчалась клиническим успехом при дилатационной кардиомиопатии (ДКМП). Дальнейшие поиски выявили, что ДКМП сопровождается интенсивным апоптозом (развивающаяся вследствие дефекта гена LMNA, вторая по частоте генетически обусловленная форма заболевания, составляющая примерно 8 % случаев).
В исследованиях на животных обнаружили, что потеря функции ламина А/С из-за его генетического дефекта активирует путь митоген-активируемой протеинкиназы p38 (MAPK). Активация пути p38 MAPK также была продемонстрирована при исследовании биоптатов сердца взрослых пациентов с ДКМП, связанной с патогенными вариантами гена LMNA. Активация этого пути ведет к усилению апоптоза кардиомиоцитов, их гипертрофии, снижению сократительной способности миокарда.
Обнаружение при ДКМП носительства патогенных вариантов генов ламина А/С, фосфоламбана, десмоплакина и филамина С свидетельствует о наличии высокого риска внезапной смерти и стало отдельным показанием для имплантации кардиовертера – дефибриллятора вне зависимости от фракции выброса.
В исследованиях на животных обнаружили, что потеря функции ламина А/С из-за его генетического дефекта активирует путь митоген-активируемой протеинкиназы p38 (MAPK). Активация пути p38 MAPK также была продемонстрирована при исследовании биоптатов сердца взрослых пациентов с ДКМП, связанной с патогенными вариантами гена LMNA. Активация этого пути ведет к усилению апоптоза кардиомиоцитов, их гипертрофии, снижению сократительной способности миокарда.
Обнаружение при ДКМП носительства патогенных вариантов генов ламина А/С, фосфоламбана, десмоплакина и филамина С свидетельствует о наличии высокого риска внезапной смерти и стало отдельным показанием для имплантации кардиовертера – дефибриллятора вне зависимости от фракции выброса.
Изучение механизмов развития легочной артериальной гипертензии вывило несколько звеньев, которые в настоящее время являются объектом интенсивного изучения.
Ключевой механизм – активация пролиферации за счет угнетения сигнальных путей, препятствующих ее развитию (опосредованные через рецептор 2-го типа костного морфогенетического белка), а также их регуляция с помощью эстрогенов. Описаны многочисленные патогенные варианты генов белков, кодирующих эти сигнальные пути и приводящих к выраженному дисбалансу в пользу существенной активации пролиферации. Модуляция сигнального пути костных морфогенетических пептидов тирозинкиназного пути исследуются как потенциальные цели лечения ЛАГ.
Включение в обследование больного омиксных технологий дает возможность в ряде случаев устанавливать точный диагноз или существенно улучшить качество прогностических моделей, способных изменить тактику ведения больного.
Омиксные технологии при разработке плана ведения больного ЛАГ в настоящее время практически не используются. Исключение составляет использование генотипирования для постановки диагноза венооклюзионной болезни легких, имеющей мало клинических отличий от идиопатической ЛАГ, но обладающей существенно худшим прогнозом и высокой вероятностью потенциально фатальных осложнений при применении стандартной ЛАГ-специфической терапии. Появление «прорывных» данных, вероятно, будет связано с уточнением регуляторных механизмов, причастных к развитию заболевания.
Ключевой механизм – активация пролиферации за счет угнетения сигнальных путей, препятствующих ее развитию (опосредованные через рецептор 2-го типа костного морфогенетического белка), а также их регуляция с помощью эстрогенов. Описаны многочисленные патогенные варианты генов белков, кодирующих эти сигнальные пути и приводящих к выраженному дисбалансу в пользу существенной активации пролиферации. Модуляция сигнального пути костных морфогенетических пептидов тирозинкиназного пути исследуются как потенциальные цели лечения ЛАГ.
Включение в обследование больного омиксных технологий дает возможность в ряде случаев устанавливать точный диагноз или существенно улучшить качество прогностических моделей, способных изменить тактику ведения больного.
Омиксные технологии при разработке плана ведения больного ЛАГ в настоящее время практически не используются. Исключение составляет использование генотипирования для постановки диагноза венооклюзионной болезни легких, имеющей мало клинических отличий от идиопатической ЛАГ, но обладающей существенно худшим прогнозом и высокой вероятностью потенциально фатальных осложнений при применении стандартной ЛАГ-специфической терапии. Появление «прорывных» данных, вероятно, будет связано с уточнением регуляторных механизмов, причастных к развитию заболевания.
Высокий риск у больных с LQTS 1-го типа обнаруживается у гомозиготных и компаунд-гетерозиготных носителей патогенных вариантов гена KCNQ1. Для больных высокого риска при LQTS2 характерно расположение патогенного варианта в области, кодирующей пору канала KCNH2, при LQTS3 – в области поры и трансмембранных доменов в SCN5A.
Кроме того, учитывая существенные различия в ведении больных с разными типами LQTS, генотипирование приобретает принципиальное значение для разработки персонализированного подхода.
Кроме того, учитывая существенные различия в ведении больных с разными типами LQTS, генотипирование приобретает принципиальное значение для разработки персонализированного подхода.
Кальциноз клапанов сердца – одна из распространенных причин развития приобретенных пороков сердца. Несмотря на снижение смертности из-за расширения объема хирургических и транскатетерных вмешательств,бремя приобретенных пороков, связанных с кальцификации клапанов, остается по-прежнему значительным.
По мнению большинства экспертов доля пациентов, которые будут нуждаться в хирургическом лечении, возрастет к 2050 г. как минимум в два раза. Notch сигналинговый путь рассматривается в качестве основного регулятора процессов кальцификации клапанов сердца. Предпринятые в настоящее время в мире попытки обосновать применение ингибиторов ГМГ-КоА-редуктазы, витамина К, ингибитора RANKL препарата деносумаба для сдерживания темпов прогрессирования аортального стеноза не подтвердили свою эффективность в реальной клинической практике. Поэтому дальнейшие исследования Notch сигналинга как потенциальной мишени для терапевтического воздействия представляется чрезвычайно актуальным.
По мнению большинства экспертов доля пациентов, которые будут нуждаться в хирургическом лечении, возрастет к 2050 г. как минимум в два раза. Notch сигналинговый путь рассматривается в качестве основного регулятора процессов кальцификации клапанов сердца. Предпринятые в настоящее время в мире попытки обосновать применение ингибиторов ГМГ-КоА-редуктазы, витамина К, ингибитора RANKL препарата деносумаба для сдерживания темпов прогрессирования аортального стеноза не подтвердили свою эффективность в реальной клинической практике. Поэтому дальнейшие исследования Notch сигналинга как потенциальной мишени для терапевтического воздействия представляется чрезвычайно актуальным.
Миокардиты и перикардиты – широко распространенная в общей популяции населения патология сердца, которая вызывает большие трудности у практикующих врачей как в диагностике, так и в лечении из-за отсутствия четких представлений о патогенезе заболеваний и в связи с особенностями верификации диагноза.
Исследования последних лет демонстрируют, что развитие воспалительных заболеваний миокарда и перикарда должны рассматриваться не только с позиции нарушений приобретенного, но и врожденного иммунитетов. По мнению большинства исследователей, инфламмасома NLRP3 не только запускает созревание провоспалительных цитокинов (интерлейкина-1β и -18) для инициации воспалительной реакции, но и играет ключевую роль в модуляции хронического воспаления, нарушая физиологическую адаптацию кардиомиоцитов и приводя к прогрессированию сердечной недостаточности.
Исследования в области врожденного иммунитета и его роли в патогенезе воспалительных заболеваний миокарда и перикарда открывает новые возможности для обоснования терапии блокаторами интерлейкина-1 и ингибиторами янус-киназы, а также для разработки нового класса препаратов – ингибиторов инфламмасом.
Исследования последних лет демонстрируют, что развитие воспалительных заболеваний миокарда и перикарда должны рассматриваться не только с позиции нарушений приобретенного, но и врожденного иммунитетов. По мнению большинства исследователей, инфламмасома NLRP3 не только запускает созревание провоспалительных цитокинов (интерлейкина-1β и -18) для инициации воспалительной реакции, но и играет ключевую роль в модуляции хронического воспаления, нарушая физиологическую адаптацию кардиомиоцитов и приводя к прогрессированию сердечной недостаточности.
Исследования в области врожденного иммунитета и его роли в патогенезе воспалительных заболеваний миокарда и перикарда открывает новые возможности для обоснования терапии блокаторами интерлейкина-1 и ингибиторами янус-киназы, а также для разработки нового класса препаратов – ингибиторов инфламмасом.
Исследования последнего десятилетия показали, что при разработке персонализованного подхода к лечению многих заболеваний следует учитывать состояние микробиома кишечника. Его изменения могут лежать в основе более агрессивного течения болезни, пенетрации генетически обусловленной патологии и могут служить одной из целей лечения. Список метаболитов микробиоты кишечника, потенциально модулирующих течение БСК, постоянно пополняется, при этом выделяют потенциально патогенные и протекторные метаболиты.
За последнее десятилетие описано более 300 эндогенных метаболитов кишечных бактерий, включая моноамины, биогенные амины, производные индола, фенолы, витамины, аминокислоты с разветвленной цепью, липиды и т.п. Наиболее активно изучаются короткоцепочечные жирные кислоты, желчные кислоты, которые могут оказывать провоспалительное или противовоспалительное действие в зависимости от типа и концентрации желчных кислот. Также исследуют влияние разного уровня синтеза незаменимых аминокислот (лейцина, изолейцина и валина), триметиламин-N-оксида, липополисахаридов (эндотоксинов). Подходы, которые в настоящее время относят к области прецизионной медицины, основанные на омиксных технологиях, теоретически могут помочь в выявлении конкретных бактериальных штаммов, ассоциированных с конкретной БСК, и разработке индивидуальных планов лечения на их основе.
Развитие ДКМП в исходе миокардита может быть частично связано с тем, что кишечные бактериоиды способны синтезировать пептид, клеточный иммунный ответ на который также комплиментарен к тяжелой цепи миозина 6. Антибактериальная терапия препятствовала прогрессированию ДКМП в эксперименте.
Комплексный геномный (GWAS) и биоинформатический анализ 47 309 случаев сердечной недостаточности и 930 014 контрольных лиц выявил ассоциацию концентрации Шигелл в микробиоте с вероятностью развития хронической сердечной недостаточности (ХСН) и ГКМП.
Одним из возможных путей участия микробиоты кишечника в развитии ЛАГ может быть увеличение поступления в кровь метаболитов, активирующих воспалительные процессы.
За последнее десятилетие описано более 300 эндогенных метаболитов кишечных бактерий, включая моноамины, биогенные амины, производные индола, фенолы, витамины, аминокислоты с разветвленной цепью, липиды и т.п. Наиболее активно изучаются короткоцепочечные жирные кислоты, желчные кислоты, которые могут оказывать провоспалительное или противовоспалительное действие в зависимости от типа и концентрации желчных кислот. Также исследуют влияние разного уровня синтеза незаменимых аминокислот (лейцина, изолейцина и валина), триметиламин-N-оксида, липополисахаридов (эндотоксинов). Подходы, которые в настоящее время относят к области прецизионной медицины, основанные на омиксных технологиях, теоретически могут помочь в выявлении конкретных бактериальных штаммов, ассоциированных с конкретной БСК, и разработке индивидуальных планов лечения на их основе.
Развитие ДКМП в исходе миокардита может быть частично связано с тем, что кишечные бактериоиды способны синтезировать пептид, клеточный иммунный ответ на который также комплиментарен к тяжелой цепи миозина 6. Антибактериальная терапия препятствовала прогрессированию ДКМП в эксперименте.
Комплексный геномный (GWAS) и биоинформатический анализ 47 309 случаев сердечной недостаточности и 930 014 контрольных лиц выявил ассоциацию концентрации Шигелл в микробиоте с вероятностью развития хронической сердечной недостаточности (ХСН) и ГКМП.
Одним из возможных путей участия микробиоты кишечника в развитии ЛАГ может быть увеличение поступления в кровь метаболитов, активирующих воспалительные процессы.
- К ним относится продукт окисления триметиламина (ТМА) – N-оксид триметиламина (ТМАО).
- Более высокая доля кишечных бактерий, продуцирующих ТМА/ТМАО, наблюдалась у больных ЛАГ. К таким продуцентам относятся Clostridium, Desulfovibrio, Enterobacter, Escherichia, Klebsiella, Pseudomonas, Rothia, Prevotella, Clostridium, Staphylococcus, Streptococcus, Anaerostipes rhamnosivorans и Collinsella.
- Еще одним возможным механизмом является увеличение на фоне дисбактериоза проницаемости кишечной стенки и появление в кровотоке бактериального эндотоксина. Среди многочисленных последствий появления этого провоспалительного агента привлекают внимание данные о резком угнетении активности рецептора костного морфогенетического белка 2-го типа в экспериментальной модели с гетерозиготным нокаутом гена BMPR2. Это угнетение сопровождается развитием ЛАГ.
Одним из направлений является изучение возможностей применения уже созданных лекарств с известным действием по новым показаниям. Так, при расопатиях (синдроме Нунан) исследовался ингибитор mTOReverolimus и Ras/MARK trametinib, при легочной артериальной гипертензии исследуется возможность применения препаратов sotatersept, tacralimus, ematinib, tamoxifen, модулирующих описанные вероятные пути патогенеза.
Исследование механизмов регуляции генома привело к разработке РНК-таргетной терапии в двух ключевых направлениях – разработке так называемых антисмысловых олигонуклеотидов и микро РНК.
Существенный прорыв был сделан при разработке аденовирусных векторов доставки генов, обеспечивающих долгосрочную экспрессию трансгенов в генной терапии, причем именно эти векторы оказались наиболее безопасными и эффективными. В эксперименте исследована возможность редактирования с помощью аденовирусного вектора гена RBM20, кодирующего РНК-связывающий белок 20, мутации которого являются частой причиной семейной дилатационной кардиомиопатии (ДКМП).
Анализ исследований последнего десятилетия, использующих омиксные технологии (протеомику, геномику, метаболомику, транскриптомику, микробиомику) демонстрирует их направленность на изучение роли генетических вариаций, биомаркеров и метаболитов в развитии сердечной недостаточности (СН), прогнозировании ее неблагоприятных исходов, а также на отбор пациентов, у которых можно ожидать наилучший ответ на терапию препаратами, применяемыми для лечения СН. При всем многообразии используемой методологии и различиях в дизайне проведенных исследований по персонализированной медицине их авторы сходятся во мнении о необходимости дальнейшей работы в области СН.
Очень перспективными представляются исследования, проводимые в мире по так называемому глубокому фенотипированию, когда при СН осуществляется сетевой анализ биологических данных с комплексным использованием омниксных технологий в дополнение к клиническо-инструментальным и лабораторным характеристикам больных.
В последние годы появился целый ряд новых биомаркеров для оценки сердечно-сосудистых заболеваний, в том числе и при ХСН. Многие из них показали обнадеживающие результаты при прогнозировании развития сердечно-сосудистых заболеваний.
Очень перспективными представляются исследования, проводимые в мире по так называемому глубокому фенотипированию, когда при СН осуществляется сетевой анализ биологических данных с комплексным использованием омниксных технологий в дополнение к клиническо-инструментальным и лабораторным характеристикам больных.
- В качестве примера можно привести программу BIOSTAT-CHF (The BIOlogy Study toTAilored Treatment in Chronic Heart Failure), организованную в 11 европейских странах, в которой анализируются демографические характеристики, биомаркеры, геномные и протеомные параметры у пациентов с СН с низкой фракцией выброса левого желудочка. В рамках этой программы получены новые данные по прецизионному фенотипированию при СН.
В последние годы появился целый ряд новых биомаркеров для оценки сердечно-сосудистых заболеваний, в том числе и при ХСН. Многие из них показали обнадеживающие результаты при прогнозировании развития сердечно-сосудистых заболеваний.
- Так, у пациентов с ХСН BNP и NT-proBNP являются самыми сильными предикторами смертности и госпитализации по поводу ХСН.
- Это прежде всего касается полиморфизма некоторых генов «воспаления» – генов интерлейкинов 4 и 10, промотора гена CD14. Наличие таких противоречивых данных о связи полиморфизма этих и других генов с развитием ХСН можно объяснить национальными особенностями, использованием разных методик определения полиморфизма, неоднородностью обследованных групп по полу, возрасту, наличию или отсутствию факторов риска заболевания. Особое внимание привлекает полиморфизм генов, которые влияют на семейство β-адренорецепторов (β-АР).
Edelberg J.M., Sehnert A.J., Mealiffe M.E. et al. The Impact of Mavacamten on the Pathophysiology of Hypertrophic Cardiomyopathy: A Narrative Review // Am J Cardiovasc Drugs 2022. 22(5):497–510. DOI: 10.1007/s40256-022-00532-x
Monda E., Bakalakos A., Rubino M. et al. Targeted Therapies in Pediatric and Adult Patients With Hypertrophic Heart Disease: From Molecular Pathophysiology to Personalized Medicine // Circ Heart Fail. 2023:e010687. DOI:10.1161/CIRCHEARTFAILURE.123.010687
MacRae C.A., Taylor M.R.G., Mestroni L. et al. Efficacy and Safety of ARRY-371797 in LMNA-Related Dilated Cardiomyopathy: A Phase 2 Study // Circ Genom Precis Med 2023. 16(1):e003730. DOI: 10.1161/CIRCGEN.122.003730
Keen J.L., Al-Naamani N., Ventetuolo C.E. The Future of PAH Treatment // Advances in Pulmonary Hypertension 2023. 22(1):55–61. DOI: 10.21693/1933-088x-22.1.55
Baulina N., Pisklova M., Kiselev I. et al. Circulating miR-499a-5p Is a Potential Biomarker of MYH7-Associated Hypertrophic Cardiomyopathy // Int J Mol Sci. 2022. 23(7). DOI: 10.3390/ijms23073791
Orphanou N., Papatheodorou E., Anastasakis A. Dilated cardiomyopathy in the era of precision medicine: latest concepts and developments // Heart Fail Rev. 2022. 27(4):1173–1191. DOI: 10.1007/s10741-021-10139-0
Neves R., Bains S., Bos J.M. et al. Precision therapy in congenital long QT syndrome // Trends in Cardiovascular Medicine. 2022. DOI: 10.1016/j.tcm.2022.06.006
Dankovtseva E., Osipova N., Minushkina L. et al. Possibilities of molecular biopsy in differential diagnosis of pulmonary arterial hypertension: case description and literature review // Medical news of the North Caucasus. 2018. 13(3). DOI: 10.14300/mnnc.2018.13100
Wang J., Zhang X., Yang X. et al. Revitalizing myocarditis treatment through gut microbiota modulation: unveiling a promising therapeutic avenue // Frontiers in Cellular and Infection Microbiology. 2023, 13. DOI: 10.3389/fcimb.2023.1191936
Luo Q., Hu Y., Chen X. et al. Effects of Gut Microbiota and Metabolites on Heart Failure and Its Risk Factors: A Two-Sample Mendelian Randomization Study // Front Nutr. 2022, 9:899746. DOI: 10.3389/fnut.2022.899746
Huang L., Zhang H., Liu Y., Long Y. The Role of Gut and Airway Microbiota in Pulmonary Arterial Hypertension // Frontiers in Microbiology. 2022, 13. DOI: 10.3389/fmicb.2022.929752
Nakano T.A., Rankin A.W., Annam A. et al. Trametinib for Refractory Chylous Effusions and Systemic Complications in Children with Noonan Syndrome // J Pediatr. 2022, 248:81-88 e81. DOI: 10.1016/j.jpeds.2022.05.030
Au H.K.E., Isalan M., Mielcarek M. Gene Therapy Advances: A Meta-Analysis of AAV Usage in Clinical Settings // Frontiers in Medicine. 2022, 8. DOI: 10.3389/fmed.2021.809118
1
Основные достижения ПМ по артериальной гипертензии
Концепция персонализированной медицины распространяется и на артериальную гипертензию (АГ). Она предполагает стратификацию риска развития АГ и выбор антигипертензивного лечения с учетом индивидуальных особенностей пациента. Так, комплексный учет генетических и фенотипических характеристик, включающих пол, возраст, антропометрические, этнические данные, клинические и физиологические показатели, связанные с профилем артериального давления (АД), поведенческие факторы, а также особенности окружающей среды может существенно улучшить эффективность терапии и снизить риски осложнений.
Динамичное развитие геномных исследований АГ и ассоциированных сердечно-сосудистых заболеваний, а также использование новых аналитических инструментов, открывают многообещающие перспективы замедления роста глобального бремени АГ и ее осложнений. Так, метод менделевской рандомизации раскрывает причинно-следственные связи между клиническими исходами и биомаркерами, которые вскоре могут стать мишенями для лекарств и обеспечить прорыв в лечении АГ. Определенные надежды улучшения профилактики и лечения АГ связывают и с технологией полигеномного секвернирования, которая в сочетании с большими популяционными исследованиями позволила идентифицировать более 1000 генетических локусов, ассоциированных с АГ.
Новейшие методы редактирования генома позволяют корректировать генетические мутации, связанные с АГ и эффективно развивать генную терапию, которая может нейтрализовать негативное влияние генетических факторов на формирование заболевания.
Учитывая многофакторный характер АГ, несомненный потенциал для прогнозирования развития АГ и индивидуализации ее лечения имеет интеграция разных типов данных – клинических, генетических, молекулярных, социально-бытовых (образ жизни, диета, степень физической активности и др.). Обработка этих данных с помощью современных методов аналитики, искусственного интеллекта и машинного обучения, способных учитывать огромное количество данных о характеристиках пациентов и их связь с различными вариантами лечения, позволит строить более точные модели прогнозирования риска и эффективности терапии.
Более сложные подходы к прогнозированию реакции на антигипертензивные препараты поднимают два практических вопроса: Превышает ли польза от прогнозирования этой реакции затраты на сбор и анализ больших объемов данных? Имеет ли данная стратегия смысл с точки зрения заботы об отдельных людях, населении или о том и другом? Ответы зависят от преимуществ использования персонализированной медицины. В связи с этим разумным подходом для персонализированного лечения АГ может быть концепция компромисса между простотой и персонализацией. Так, более персонализированные стратегии лечения могут принести наибольшую пользу пациентам, у которых простые стратегии с низкой информационной нагрузкой оказываются неэффективными. При этом особо высока потребность в разработке новых подходов прогнозирования ответа на антигипертензивные препараты и дорогостоящие инвазивные методы лечения у больных с резистентной АГ, при которой аспекты персонализированной терапии остаются наименее изученным.
К настоящему времени накоплено большое количество информации о полиморфизме генов, связанных с регуляцией АД. Только за последние пять лет понимание генетической основы АГ пришло к полигенным ассоциациям, охватывающим ~30 моногенных редких вариантов и >1,5 тыс. однонуклеотидных вариантов.
Крупномасштабные исследования геномики, в каждом из которых изучалось более 750 000 человек, выявили сотни локусов, связанных с изменениями уровней АД. В крупномасштабном исследовании с проведением полногеномного секвестрирования, включавшем мета-анализ более 900 тыс. участников, был также выявлен ряд связей последовательностей генов с уровнем систолического, диастолического АД и АГ.
Доступны данные о широком профиле биомаркеров. Изучались и отмечены различия у лиц с АГ в составе целого ряда метаболитов.
В оценке эффективности фармакотерапии и выявлении причин ее снижения, а также прогнозировании выраженности ответа на препарат и появления побочных эффектов может помочь фармакометаболомика. В частности, получены данные, касающиеся различий ответа на бета-блокаторы, диуретики и лизиноприл.
Согласно опубликованному в 2023 г. шведскому рандомизированному исследованию обнаружена неоднородность реакции АД на четыре антигипертензивных препарата (лизиноприл, кандесартан, гидрохлоротиазид и амлодипин), которая может иметь существенное значение для персонализированной терапии.
Согласно мета-анализу была документирована ассоциация одного из генетических вариантов с ослаблением реакции АД на β-блокаторы и увеличением риск неблагоприятных сердечно-сосудистых исходов при их использовании.
В настоящее время британскими учеными разрабатывается персонализированный подход к лечению АГ на основе генетического тестирования совместно с определением дополнительных биомаркеров. Однако на текущий момент времени крупномасштабное клиническое лечение АГ на основе генома невозможно из-за потребности в специальной инфраструктуре и малодоступных ресурсах для геномных тестов. Следовательно, персонализированный подход к лечению АГ должен основываться на показателях фенотипа, связанных с особенностями течения заболевания, а также с нервной и гуморальной регуляцией АД. Одним из таких показателей является вариабельность уровней АД, играющая важную роль в прогрессировании сердечно-сосудистых заболеваний и терапии АГ.
Для персонализированной терапии АГ китайскими учеными разработана классификация REASOH, основанная на этиологии АГ и включающая шесть основных ее вариантов: ренин-зависимую гипертензию, гипертензию на основе атеросклероза у пожилых людей, симпатико-активную гипертензию, вторичную гипертензию, солечувствительную гипертензию и гипергомоцистеинемическую гипертензию.
Перспективным направлением персонализированной медицины является развитие искусственного интеллекта, улучшающего процесс принятия клинических решений. Так, в ходе сельского когортного исследования Китайскими учеными было установлено, что оценка полигенного риска с использованием 13 одиночных нуклеотидных полимофизмов в сочетании с учетом традиционных факторов риска значительно улучшала качество модели прогнозирования возникновения АГ.
Также примечательны результаты катарских ученых, согласно которым комбинация полногеномного секвенирования и методики искусственного интеллекта помогла определить уникальный профиль генетической предрасположенности к АГ разных этнических групп.
Важно отметить, что использование искусственного интеллекта для прогнозирования развития АГ на основе факторов риска может быть эффективным даже без анализа генетического материала. Так, ряду научных групп удалось создать модели прогнозирования развития АГ по данным рутинных показателей ежегодных медицинских осмотров, а H.F. Golino с коллегами использовали только антропометрические данные.
На основе данных исследований SPRINT и ACCORD BP с целью персонализации сердечно-сосудистой пользы от интенсивности антигипертензивного лечения американскими учеными была разработана соответствующая программа машинного обучения.
Особенно актуальным персонализированный подход лечения АГ представляется в том случае, когда стандартная стратегия лечения оказывается недостаточно эффективной. Так, выявлен ряд характеристик для отбора пациентов с резистентной АГ для проведения ренальной денервации, позволяющих ожидать наибольшей эффективности лечения. Наиболее распространенным примером искусственного интеллекта для диагностики АГ является суточное мониторирование АД. Однако эта методика сопряжена с рядом неудобств для пациента, а осциллометрический способ измерения АД имеет свои ограничения. В связи с этим в настоящее время предлагается мониторирование АД при помощи более точного и удобного для пациента метода фотоплетизмографии и емкостной технологии.
Динамичное развитие геномных исследований АГ и ассоциированных сердечно-сосудистых заболеваний, а также использование новых аналитических инструментов, открывают многообещающие перспективы замедления роста глобального бремени АГ и ее осложнений. Так, метод менделевской рандомизации раскрывает причинно-следственные связи между клиническими исходами и биомаркерами, которые вскоре могут стать мишенями для лекарств и обеспечить прорыв в лечении АГ. Определенные надежды улучшения профилактики и лечения АГ связывают и с технологией полигеномного секвернирования, которая в сочетании с большими популяционными исследованиями позволила идентифицировать более 1000 генетических локусов, ассоциированных с АГ.
Новейшие методы редактирования генома позволяют корректировать генетические мутации, связанные с АГ и эффективно развивать генную терапию, которая может нейтрализовать негативное влияние генетических факторов на формирование заболевания.
Учитывая многофакторный характер АГ, несомненный потенциал для прогнозирования развития АГ и индивидуализации ее лечения имеет интеграция разных типов данных – клинических, генетических, молекулярных, социально-бытовых (образ жизни, диета, степень физической активности и др.). Обработка этих данных с помощью современных методов аналитики, искусственного интеллекта и машинного обучения, способных учитывать огромное количество данных о характеристиках пациентов и их связь с различными вариантами лечения, позволит строить более точные модели прогнозирования риска и эффективности терапии.
Более сложные подходы к прогнозированию реакции на антигипертензивные препараты поднимают два практических вопроса: Превышает ли польза от прогнозирования этой реакции затраты на сбор и анализ больших объемов данных? Имеет ли данная стратегия смысл с точки зрения заботы об отдельных людях, населении или о том и другом? Ответы зависят от преимуществ использования персонализированной медицины. В связи с этим разумным подходом для персонализированного лечения АГ может быть концепция компромисса между простотой и персонализацией. Так, более персонализированные стратегии лечения могут принести наибольшую пользу пациентам, у которых простые стратегии с низкой информационной нагрузкой оказываются неэффективными. При этом особо высока потребность в разработке новых подходов прогнозирования ответа на антигипертензивные препараты и дорогостоящие инвазивные методы лечения у больных с резистентной АГ, при которой аспекты персонализированной терапии остаются наименее изученным.
К настоящему времени накоплено большое количество информации о полиморфизме генов, связанных с регуляцией АД. Только за последние пять лет понимание генетической основы АГ пришло к полигенным ассоциациям, охватывающим ~30 моногенных редких вариантов и >1,5 тыс. однонуклеотидных вариантов.
Крупномасштабные исследования геномики, в каждом из которых изучалось более 750 000 человек, выявили сотни локусов, связанных с изменениями уровней АД. В крупномасштабном исследовании с проведением полногеномного секвестрирования, включавшем мета-анализ более 900 тыс. участников, был также выявлен ряд связей последовательностей генов с уровнем систолического, диастолического АД и АГ.
Доступны данные о широком профиле биомаркеров. Изучались и отмечены различия у лиц с АГ в составе целого ряда метаболитов.
В оценке эффективности фармакотерапии и выявлении причин ее снижения, а также прогнозировании выраженности ответа на препарат и появления побочных эффектов может помочь фармакометаболомика. В частности, получены данные, касающиеся различий ответа на бета-блокаторы, диуретики и лизиноприл.
Согласно опубликованному в 2023 г. шведскому рандомизированному исследованию обнаружена неоднородность реакции АД на четыре антигипертензивных препарата (лизиноприл, кандесартан, гидрохлоротиазид и амлодипин), которая может иметь существенное значение для персонализированной терапии.
Согласно мета-анализу была документирована ассоциация одного из генетических вариантов с ослаблением реакции АД на β-блокаторы и увеличением риск неблагоприятных сердечно-сосудистых исходов при их использовании.
В настоящее время британскими учеными разрабатывается персонализированный подход к лечению АГ на основе генетического тестирования совместно с определением дополнительных биомаркеров. Однако на текущий момент времени крупномасштабное клиническое лечение АГ на основе генома невозможно из-за потребности в специальной инфраструктуре и малодоступных ресурсах для геномных тестов. Следовательно, персонализированный подход к лечению АГ должен основываться на показателях фенотипа, связанных с особенностями течения заболевания, а также с нервной и гуморальной регуляцией АД. Одним из таких показателей является вариабельность уровней АД, играющая важную роль в прогрессировании сердечно-сосудистых заболеваний и терапии АГ.
Для персонализированной терапии АГ китайскими учеными разработана классификация REASOH, основанная на этиологии АГ и включающая шесть основных ее вариантов: ренин-зависимую гипертензию, гипертензию на основе атеросклероза у пожилых людей, симпатико-активную гипертензию, вторичную гипертензию, солечувствительную гипертензию и гипергомоцистеинемическую гипертензию.
Перспективным направлением персонализированной медицины является развитие искусственного интеллекта, улучшающего процесс принятия клинических решений. Так, в ходе сельского когортного исследования Китайскими учеными было установлено, что оценка полигенного риска с использованием 13 одиночных нуклеотидных полимофизмов в сочетании с учетом традиционных факторов риска значительно улучшала качество модели прогнозирования возникновения АГ.
Также примечательны результаты катарских ученых, согласно которым комбинация полногеномного секвенирования и методики искусственного интеллекта помогла определить уникальный профиль генетической предрасположенности к АГ разных этнических групп.
Важно отметить, что использование искусственного интеллекта для прогнозирования развития АГ на основе факторов риска может быть эффективным даже без анализа генетического материала. Так, ряду научных групп удалось создать модели прогнозирования развития АГ по данным рутинных показателей ежегодных медицинских осмотров, а H.F. Golino с коллегами использовали только антропометрические данные.
На основе данных исследований SPRINT и ACCORD BP с целью персонализации сердечно-сосудистой пользы от интенсивности антигипертензивного лечения американскими учеными была разработана соответствующая программа машинного обучения.
Особенно актуальным персонализированный подход лечения АГ представляется в том случае, когда стандартная стратегия лечения оказывается недостаточно эффективной. Так, выявлен ряд характеристик для отбора пациентов с резистентной АГ для проведения ренальной денервации, позволяющих ожидать наибольшей эффективности лечения. Наиболее распространенным примером искусственного интеллекта для диагностики АГ является суточное мониторирование АД. Однако эта методика сопряжена с рядом неудобств для пациента, а осциллометрический способ измерения АД имеет свои ограничения. В связи с этим в настоящее время предлагается мониторирование АД при помощи более точного и удобного для пациента метода фотоплетизмографии и емкостной технологии.
Rochais F., Vilardaga J.P., Nikolaev V.O. et al. Realtime optical recording of beta1-adrenergic receptor activation reveals supersensitivity of the Arg389 variant to carvedilol // J. Clin. Invest. 2007. Vol. 117. P. 229–235.
Evangelou E., Warren H.R. Genetic analysis of over 1 million people identifies 535 new loci associated with blood pressure traits // Nat Genet. 2018. 50, 1412–1425. DOI: 10.1038/s41588-018-0205-x
Giri A., Hellwege J.N., Keaton J.M. et al. Trans-ethnic association study of blood pressure determinants in over 750,000 individuals // Nat Genet. 2019. 51, 51–62. DOI: 10.1038/s41588-018-0303-9
Giri A., Hellwege J.N., Keaton J.M. et al. Trans-ethnic association study of blood pressure determinants in over 750,000 individuals // Nat Genet. 2019. 51, 51–62. DOI: 10.1038/s41588-018-0303-9
Campbell D., Aman A., Iniesta R. et al. Pharmaco-metabolomics of blood pressure response to beta-blockers and diuretics // J Hypertens. 2018;36:e124-e125. DOI: 10.1097/01
Geng T.T., Jafar T.H. Hypertension Pharmacogenomics in CKD: The Clinical Relevance and Public Health Implications // Kidney 360. 2022. 3, 204–207. DOI: 10.34067/KID.0007792021
Niu M., Wang Y., Zhang L. et al. Identifying the predictive effectiveness of a genetic risk score for incident hypertension using machine learning methods among populations in rural China // Hypertens Res. 2021; 44:1483–1491. DOI: 10.1038/s41440-021-00738-7
Kanegae H., Suzuki K., Fukatani K. et al. Highly precise risk prediction model for new-onset hypertension using artificial intelligence techniques // The Journal of Clinical Hypertension. 2020; 22(3):445-450. DOI: 10.1111/jch.13759
Мaxwell A., Li R., Yang B. et al. Deep learning architectures for multi-label classification of intelligent health risk prediction // BMC Bioinform. 2017;18:523. DOI: 10.1186/s12859-017-1898-z
Мaxwell A., Li R., Yang B. et al. Deep learning architectures for multi-label classification of intelligent health risk prediction // BMC Bioinform. 2017;18:523. DOI: 10.1186/s12859-017-1898-z
Golino H.F., Amaral L.S., Duarte S.F. et al. Predicting increased blood pressure using machine learning// Journal of obesity. 2014. Vol. 2014. DOI: 10.1155/2014/637635
Townsend R.R., Mahfoud F., Kandzari D.E. et al. Catheter-based renal denervation in patients with uncontrolled hypertension in the absence of antihypertensive medications (SPYRAL HTN-OFF MED): a randomised, sham-controlled, proof-of-concept trial // Lancet. 2017;390(10108):2160–70. DOI: 10.1016/s0140-6736(17)32281-x
Kandzari D.E., Bohm M., Mahfoud F. et al. Effect of renal denervation on blood pressure in the presence of antihypertensive drugs: 6-month efficacy and safety results from the SPYRAL HTN-ON MED proof-of-concept randomised trial // Lancet. 2018;391(10137):2346–55. DOI: 10.1016/s0140-6736(18)30951-6
Azizi M., Schmieder R.E., Mahfoud F. et al. Endovascular ultrasound renal denervation to treat hypertension (RADIANCE-HTN SOLO): a multicentre, international, single-blind, randomised, sham-controlled trial // Lancet. 2018;391(10137):2335–45. DOI: 10.1016/s0140-6736(18)31082-1
Kandzari D.E., Bohm M., Mahfoud F. et al. Effect of renal denervation on blood pressure in the presence of antihypertensive drugs: 6-month efficacy and safety results from the SPYRAL HTN-ON MED proof-of-concept randomised trial // Lancet. 2018;391(10137):2346–55. DOI: 10.1016/s0140-6736(18)30951-6
Azizi M., Schmieder R.E., Mahfoud F. et al. Endovascular ultrasound renal denervation to treat hypertension (RADIANCE-HTN SOLO): a multicentre, international, single-blind, randomised, sham-controlled trial // Lancet. 2018;391(10137):2335–45. DOI: 10.1016/s0140-6736(18)31082-1
Nitzan M., Nitzan I. Feasibility of Precision Medicine in Hypertension Management-Scope and Technological Aspects // J Pers Med. 2022;7;12(11):1861. DOI: 10.3390/jpm12111861. PMID: 36573720; PMCID: PMC9698650
Chowdhury M.E.H., Mahbub Z.B., Uddin M.M. et al. Estimating Blood Pressure from the Photoplethysmogram Signal and Demographic Features Using Machine Learning Techniques // Sensors. 2020;20:3127.DOI: 10.3390/s20113127
Chowdhury M.E.H., Mahbub Z.B., Uddin M.M. et al. Estimating Blood Pressure from the Photoplethysmogram Signal and Demographic Features Using Machine Learning Techniques // Sensors. 2020;20:3127.DOI: 10.3390/s20113127
2
Персонификация антитромботической терапии при ишемической болезни сердца
Высококонкурентный рынок антитромботических препаратов в мире сегодня является наиболее динамично развивающимся. По состоянию на 2022 г. он составил 42 млрд дол. США. Ожидается, что к 2029 г. этот показатель практически удвоится и составит 76 млрд дол. США. Рост числа сердечно-сосудистых, онкологических заболеваний, гериатрической популяции и малоподвижный образ жизни определяют динамику развития рынка антитромботических средств.
В аспекте прецессионных подходов к использованию антитромботических препаратов стоит выделить несколько направлений исследований: доказательная медицина как инструмент персонификации; биомаркеры персонификации; фармакогенетические исследования; продвинутые предиктивные модели; системы поддержки принятия решений и технологии искусственного интеллекта.
В аспекте прецессионных подходов к использованию антитромботических препаратов стоит выделить несколько направлений исследований: доказательная медицина как инструмент персонификации; биомаркеры персонификации; фармакогенетические исследования; продвинутые предиктивные модели; системы поддержки принятия решений и технологии искусственного интеллекта.
Доказательная медицина как инструмент персонификации.
Клинические исследования последних лет в области использования антитромботической терапии позволяют вырабатывать более индивидуализированные алгоритмы ведения пациентов. Примером могут служить новые шкалы риска, такие как DAPT, PRECISE-DAPT, позволяющие выделять отдельные группы пациентов, нуждающихся в продлении антитромбоцитарной терапии или, наоборот, ее укорочении.
- Субанализ клинических исследований в аспекте этнических особенностей эффективности и безопасности терапии приводит к появлению новых субпопуляционных алгоритмов по эскалации, деэскалации и продолжительности терапии.
- Сформированы отдельные режимы дозирования антитромботических препаратов в зависимости от массы тела пациента.
- Отдельным направлением последних лет являются исследования гендерных особенностей эффективности и безопасности антитромботических средств с акцентом на женскую популяцию. Это способствует появлению риск-скоринга, учитывающего гендерную характеристику.
Биомаркеры персонификации.
Тестирование функциональной активности тромбоцитов (ФАТ) у пациентов, получающих ингибиторы P2Y12 рецепторов тромбоцитов, стало предметом исследований в последние десятилетия. Сегодня на рынке доступно несколько «открытых» и «закрытых» тест-систем (LTA, VerifyNow, Multiplate, VASP и др.).
Тестирование ФАТ при использовании ацетисалициловой кислоты (АСК) не доказало своей клинической целесообразности и вариабельность в ответе на прием препарата была связана с его биодоступностью и формой выпуска. При этом исследования по персонификации терапии АСК продолжились с использованием других биомаркеров. Так, определение уровня тромбоксана B2 позволяет индивидуализировать дозу АСК.
Субанализ рандомизированных клинических исследований прямых оральных антикоагулянтов, не требующих лабораторного контроля, показал достоверную связь между концентрацией препарата в крови и профилем эффективности/безопасности.
Определение анти-Ха активности для ингибиторов фактора-Xa, «разбавленного» тромбинового времени и экаринового теста для прямых ингибиторов тромбина коррелирует с MS-концентрацией препаратов в крови.
- Доказано, что высокая остаточная активность тромбоцитов по данным ФАТ у пациентов с ОКС после ЧКВ ассоциирована с риском тромбоза стента и крупных сердечно-сосудистых событий (MACE). При этом клиническая целесообразность эскалации антитромбоцитарной терапии на основании тестирования ФАТ не подтвердилась.
- Проведенные исследования имели методологические дефекты или недостаточную статистическую мощность. Есть общее понимание необходимости дальнейших исследований в этом направлении.
- Возможность деэскалации терапии ингибиторами пуриновых рецепторов (c тикагрелора/прасугрела до клопидогрела) с целью минимизации геморрагических рисков была доказана в клинических исследованиях (TOPIC, TROPICAL-ACS и др.). В этом случае тестирование ФАТ доказано в качестве одного из способов деэскалации терапии. Продемонстрирована также возможность снижения дозы прасугрела как вариант деэскалации. Требуется проведение новых исследований.
Тестирование ФАТ при использовании ацетисалициловой кислоты (АСК) не доказало своей клинической целесообразности и вариабельность в ответе на прием препарата была связана с его биодоступностью и формой выпуска. При этом исследования по персонификации терапии АСК продолжились с использованием других биомаркеров. Так, определение уровня тромбоксана B2 позволяет индивидуализировать дозу АСК.
Субанализ рандомизированных клинических исследований прямых оральных антикоагулянтов, не требующих лабораторного контроля, показал достоверную связь между концентрацией препарата в крови и профилем эффективности/безопасности.
Определение анти-Ха активности для ингибиторов фактора-Xa, «разбавленного» тромбинового времени и экаринового теста для прямых ингибиторов тромбина коррелирует с MS-концентрацией препаратов в крови.
- Некоторые категории пациентов (гериатрия, ХБП, экстремальная масса тела и др.) могут получить пользу от персонифицированного подбора дозы препаратов на основании лабораторного мониторинга.
- Отдельные исследования подтверждают эффективность этого подхода. Требуется проведение крупных рандомизированных клинических исследований.
Фармакогенетические исследования.
Существенным преимуществом фармакогенетических исследований перед биомаркерным мониторингом является возможность заблаговременного (до момента инициации терапии) принятия решения о выборе терапии.
Исследования полиморфизма CYP2C9 и VKORC-1 для коррекции дозы варфарина стали первыми, продемонстрировавшими возможности фармакогенетических исследований у пациентов, получающих антитромботические препараты.
Важным вектором фармакогенетических исследований последних лет становятся полигенные ассоциации в исследованиях больших баз данных с использованием технологий полногеномного секвинирования. Так, в исследовании GWAS STUDY была продемонстрирована предикторная роль полиморфизма генов SCOSSP1, CDC42BPA и CTRAC1 в части риска тромбоза коронарного стента и ишемических событий у пациентов, получающих антитромбоцитарные препараты.
Достижения в области фармакогенетических и биомаркерных исследований позволяют ревалидизировать стандартные шкалы тромботического риска и формировать новые предиктивные модели. Так, комбинация клинических данных, данных функциональных исследований, тестирования ФАТ и фармакогенгетической информации позволила сформировать шкалу POPular, персонифицирующую антитромбоцитарную стратегию у пациентов после ЧКВ. Дальнейшие исследования в этой области могут стать основанием для создания ПО-систем поддержки принятия решений при назначении антитромботической терапии наподобие тех, которые уже успешно внедрены для пациентов, получающих терапию антагонистами витамина К (DAWN-AC, INR-STAR, Warfarindosing algorithm и др.).
Антитромботические средства, доступные сегодня на рынке, имеют высокую эффективность, но при этом обладают большой гетерогенностью в части снижения риска тромботических событий и неблагоприятных исходов при разной патологии в различных группах пациентов. Исследования последних лет с использованием технологий искусственного интеллекта позволяют идентифицировать дополнительные генетические факторы, которые до настоящего времени считались «минорными», но могут в совокупности с другими характеристиками (клинические, анамнестические и др.) влиять на резистентность терапии.
Исследования полиморфизма CYP2C9 и VKORC-1 для коррекции дозы варфарина стали первыми, продемонстрировавшими возможности фармакогенетических исследований у пациентов, получающих антитромботические препараты.
- В последующих работах показано, что полиморфизм CYP2C19 у пациентов, получающих клопидогрел, ассоциирован с повышенной частотой неблагоприятных сердечно-сосудистых событий и тромбозов стента.
- Другие гены-кандидаты, кодирующие белки, участвующие в процессе метаболизма и транспорта ингибиторов пуриновых рецепторов, не продемонстрировали такой же мощной корреляции.
- Однако в этой связи перспективным направлением будущих исследований можно считать работы с полигенными предикторами, которые могут персонифицировать терапию в аспекте межлекарственного взаимодействия.
- Было показано, что полиморфизм PPAR и CYP3A4 у пациентов, получающих клопидогрел, не играют существенной роли в метаболизме препарата, но влияют на эффективность при совместном использовании со статинами и фибратами.
Важным вектором фармакогенетических исследований последних лет становятся полигенные ассоциации в исследованиях больших баз данных с использованием технологий полногеномного секвинирования. Так, в исследовании GWAS STUDY была продемонстрирована предикторная роль полиморфизма генов SCOSSP1, CDC42BPA и CTRAC1 в части риска тромбоза коронарного стента и ишемических событий у пациентов, получающих антитромбоцитарные препараты.
Достижения в области фармакогенетических и биомаркерных исследований позволяют ревалидизировать стандартные шкалы тромботического риска и формировать новые предиктивные модели. Так, комбинация клинических данных, данных функциональных исследований, тестирования ФАТ и фармакогенгетической информации позволила сформировать шкалу POPular, персонифицирующую антитромбоцитарную стратегию у пациентов после ЧКВ. Дальнейшие исследования в этой области могут стать основанием для создания ПО-систем поддержки принятия решений при назначении антитромботической терапии наподобие тех, которые уже успешно внедрены для пациентов, получающих терапию антагонистами витамина К (DAWN-AC, INR-STAR, Warfarindosing algorithm и др.).
Антитромботические средства, доступные сегодня на рынке, имеют высокую эффективность, но при этом обладают большой гетерогенностью в части снижения риска тромботических событий и неблагоприятных исходов при разной патологии в различных группах пациентов. Исследования последних лет с использованием технологий искусственного интеллекта позволяют идентифицировать дополнительные генетические факторы, которые до настоящего времени считались «минорными», но могут в совокупности с другими характеристиками (клинические, анамнестические и др.) влиять на резистентность терапии.
- Так, в исследовании Genome-wide Association Study с использованием базы данных однонуклеотидных полиморфизмов (SNPs) удалось выявить 20 SNPs, которые были ассоциированы с девятью белок-кодирующими генами, из которых были выделены пять генов-кандидатов, формировавших «белковую сеть», ассоциированную с экспрессией P2Y12 рецепторов тромбоцитов, являющихся мишенью для антитромбоцитарной терапии.
- Таким образом, технология искусственного интеллекта позволила сформировать профайл пациентов в тайваньской популяции, которые могут иметь отдельные особенности действия антитромботических препаратов. Возможности машинного обучения и искусственного интеллекта станут важнейшим инструментом в исследованиях последующих лет.
Data bridge market research. URL: https://www.databridgemarketresearch.com/reports/global-antithrombotic-drugs-market (дата обращения: 10.02.2023).
Juhani K., William W., Davide C. et al. ESC Guidelines for the diagnosis and management of chronic coronary syndromes: The Task Force for the diagnosis and management of chronic coronary syndromes of the European Society of Cardiology (ESC) // European Heart Journal. 2019. Vol. 41, Iss. 3. P. 407–477.
Gorog D.A., Jeyalan V., Markides R.I.L. et al. Comparison of De-escalation of DAPT intensity or duration in East Asian and Western patients with ACS undergoing PCI: a systematic review and meta-analysis // Thromb Haemost, 2023. Vol. 123. P. 773–792.
Bianca R. Antithrombotic therapy and body mass: an expert position paper of the ESC Working Group on Thrombosis // European Heart Journal. 2018. Vol. 39. Iss. 19. P. 1672–1686.
Maas A., Rosano G., Cifkova R. et al. Cardiovascular health after menopause transition, pregnancy disorders, and other gynaecologic conditions: a consensus document from European cardiologists, gynaecologists, and endocrinologists // European Heart Journal. 2021. Vol. 42(10). P. 967–984.
Levine G.N., Bates E.R., Bittl J.A. et al. ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease: a report of the American College of Cardiology American Heart Association Task Force on Clinical Practice Guidelines // Journal of the American College of Cardiology. 2016. Vol. 68. P. 1082–1115.
Becker D.M., Segal J., Vaidya D. et al. Sex differences in platelet reactivity and response to low-dose aspirin therapy // JAMA. 2006. Vol. 295(12). P. 1420–1427.
Levine G.N., Bates E.R., Bittl J.A. et al. ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease: a report of the American College of Cardiology American Heart Association Task Force on Clinical Practice Guidelines // Journal of the American College of Cardiology. 2016. Vol. 68. P. 1082–1115.
Becker D.M., Segal J., Vaidya D. et al. Sex differences in platelet reactivity and response to low-dose aspirin therapy // JAMA. 2006. Vol. 295(12). P. 1420–1427.
Udaya S.T., Laurent B., Daniel A. et al. Consensus and Update on the Definition of On-Treatment Platelet Reactivity to Adenosine Diphosphate Associated With Ischemia and Bleeding // J Am Coll Cardiol. 2013. Vol. 62 (24). P.2261–2273.
Anastasia A., Albert F. Role of platelet function testing in acute coronary syndromes: a meta-analysis // Open Heart. 2022, Vol. 9(2), e002129.
Mattia G., Dominick J. A.. De-escalation of antiplatelet therapy in acute coronary syndromes: Why, how and when? // Front Cardiovasc Med. 2022. 9: 975969.
Hyo-Soo Kim, Jeehoon Kang et al. Prasugrel-based de-escalation of dual antiplatelet therapy after percutaneous coronary intervention in patients with acute coronary syndrome (HOST-REDUCE-POLYTECH-ACS): an open-label, multicentre, non-inferiority randomised trial // The Lancet. 2020. Vol. 396. Iss. 10257. P. 1079–1089.
Deepak L.Bh., Tilo Gr. et al. Enteric Coating and Aspirin Nonresponsiveness in Patients With Type 2 Diabetes Mellitus // J Am Coll Cardiol. 2017. Vol. 69(6). P. 603–612.
Nischal N.H., Navin M. et al. Personalized allocation of acetylsalicylic acid therapy for secondary prevention of coronary artery disease // Front. Cardiovasc. 2022, Sec. Thrombosis and Haemostasis, Vol. 9.
Paul A. R., Thorsten L. et al. The Effect of Dabigatran Plasma Concentrations and Patient Characteristics on the Frequency of Ischemic Stroke and Major Bleeding in Atrial Fibrillation Patients: The RE-LY Trial (Randomized Evaluation of Long-Term Anticoagulation Therapy) // Journal of the American College of Cardiology. 2014. Vol. 63. Iss. 4. P. 321–328.
Claire D. Laboratory Monitoring of Direct Oral Anticoagulants (DOACs) // Biomedicines. 2021. Vol. 9(5).P. 445.
Tania A., Veronica R. et al. To Measure or Not to Measure: Direct Oral Anticoagulant Laboratory Assay Monitoring in Clinical Practice // Advances in Hematology. 2023, Vol. 2023: 9511499.
Zhitong Li, Xin Wang et al. Atrial cardiomyopathy markers predict ischemic cerebrovascular events independent of atrial fibrillation in patients with acute myocardial infarction // Front. Cardiovasc. Med. 2022, Sec. Coronary Artery Disease, Vol. 9.
Daniel M.F. Claassens, Gerrit J.A. Vos et al. A Genotype-Guided Strategy for Oral P2Y12 Inhibitors in Primary PCI // N Engl J Med. 2019. Vol. 381(17). P. 1621–1631.
Munir Pirmohamed, Girvan Burnside et al. A Randomized Trial of Genotype-Guided Dosing of Warfarin // N Engl J Med. 2013. Vol. 369(24). P. 2294–2303.
Thomas O Bergmeijer, Alfi Yasmina et al. Effect of CYP3A4*22 and PPAR-α Genetic Variants on Platelet Reactivity in Patients Treated with Clopidogrel and Lipid-Lowering Drugs Undergoing Elective Percutaneous Coronary Intervention // Genes (Basel). 2020. Vol. 11(9). P. 1068.
Sri H Kanuri, Rolf P Kreutz. Pharmacogenomics of Novel Direct Oral Anticoagulants: Newly Identified Genes and Genetic Variants // J Pers Med. 2019. Vol. 9(1). P. 7.
Shefali Setia Verma, Thomas O. Bergmeijer Genomewide Association Study of Platelet Reactivity and Cardiovascular Response in Patients Treated With Clopidogrel: A Study by the International Clopidogrel Pharmacogenomics Consortium // Clin Pharmacol Ther. 2020. Vol. 108(5). P. 1067–1077.
Paul W.A. Janssen, Thomas O. Bergmeijer et al. Tailored P2Y12 inhibitor treatment in patients undergoing non-urgent PCI-the POPular Risk Score study // Eur J Clin Pharmacol. 2019. Vol. 75(9). P. 1201–1210.
Chi-Hsiao Yeh, Yi-Ju Chou et al. Artificial-Intelligence-Assisted Discovery of Genetic Factors for Precision Medicine of Antiplatelet Therapy in Diabetic Peripheral Artery Disease // Biomedicines. 2022. Vol. 10(1). P.116.
3
Персонализированная медицина в сердечно-сосудистой хирургии
Прогнозирование риска жизнеугрожающих осложнений после кардиохирургических операции являются краеугольным камнем оценки качества оказываемой помощи. Актуальные клинические рекомендации рекомендуют дооперационную оценку риска с использованием валидированных шкал EuroSCORE-II и STS. Однако все больше авторов заявляет о недостаточной точности этих шкал при использовании на практике.
Набирающие популярность в медицине методы машинного обучения имеют превосходство над традиционными методами статистического анализа и являются многообещающими инструментами для персонального прогнозирования неблагоприятных послеоперационных исходов в кардиохирургии. Результаты, полученные в ряде исследований, свидетельствуют о преимуществах использования методов машинного обучения в прогнозной персонализированной аналитике при оказании кардиохирургической помощи, что обусловлено более высокой дискриминацией моделей машинного обучения в сравнении с традиционно используемой логистической регрессией, на основе которой были разработаны применяющиеся в настоящий момент шкалы риска.
Набирающие популярность в медицине методы машинного обучения имеют превосходство над традиционными методами статистического анализа и являются многообещающими инструментами для персонального прогнозирования неблагоприятных послеоперационных исходов в кардиохирургии. Результаты, полученные в ряде исследований, свидетельствуют о преимуществах использования методов машинного обучения в прогнозной персонализированной аналитике при оказании кардиохирургической помощи, что обусловлено более высокой дискриминацией моделей машинного обучения в сравнении с традиционно используемой логистической регрессией, на основе которой были разработаны применяющиеся в настоящий момент шкалы риска.
Технология 3D-печати все больше признается в качестве ценного инструмента хирургического планирования, позволяющего получить представление о сложных внутрисердечных структурах с точными размерами и предоставляющего хирургу возможность визуализировать сердце перед операцией.
Протезирование аортального клапана неостворками из аутоперикарда
операции Оzaki, при доступности данных визуализации (компьютерная томография или магнитно-резонансная томография сердечных структур), модели корня аорты для конкретного пациента могут быть напечатаны в короткие сроки, что позволяет хирургу определить персональный размер створок аортального клапана и подготовить их до начала операции.
Протезирование аортального клапана неостворками из аутоперикарда
операции Оzaki, при доступности данных визуализации (компьютерная томография или магнитно-резонансная томография сердечных структур), модели корня аорты для конкретного пациента могут быть напечатаны в короткие сроки, что позволяет хирургу определить персональный размер створок аортального клапана и подготовить их до начала операции.
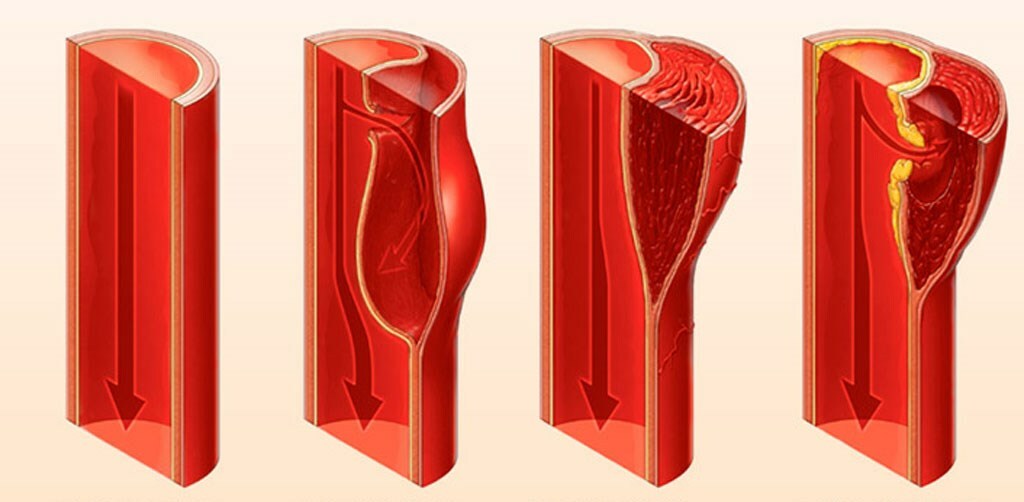
Расслоение аорты типа I часто сопровождаются диссекцией брахиоцефальных артерий, формируя очаги мальперфузии в двух и более артериальных бассейнах.
Применение стандартной методики протезирования дуги аорты не может учесть всех вариантов особенностей кровотока в поврежденной аорте и жизненно-важных сосудах. В данном случае только применение персонализированных подходов позволяет безопасно выполнить вмешательство. Персонализированных подход включает в себя выбор индивидуального типа перфузии, зон артериальной канюляции, сопоставимых между собой типов протезов дуги аорты и брахиоцефальной зоны.
Эти протезы различаются по количеству бранш, их диаметру, трехмерному расположению бранш. Планирование и изготовление таких групп протезов производится под конкретную клиническую ситуацию на основе трехмерных моделей, полученных при КТ, а также с учетом функциональных проб, определяющих клиническую значимость пораженных артерий.
Для повышения эффективности следует использовать две группы протезов: протезы зоны брахиоцефального сегмента и зоны дуги аорты. Каждая из этих групп позволяет персонифицировано решить уникальную клиническую задачу по протезированию в соответствующей зоне, но при этом сохраняется полная унификация соединения обеих групп протезов на завершающем этапе вмешательства.
Выбор оптимального способа протезирования и изготовление протезов сложной формы, соответствующих варианту расслоения, позволяет сократить время операции, увеличить ее радикальность, выполнить вмешательство на брахиоцефальных артериях без прекращения церебрального и системного кровотока.
Применение стандартной методики протезирования дуги аорты не может учесть всех вариантов особенностей кровотока в поврежденной аорте и жизненно-важных сосудах. В данном случае только применение персонализированных подходов позволяет безопасно выполнить вмешательство. Персонализированных подход включает в себя выбор индивидуального типа перфузии, зон артериальной канюляции, сопоставимых между собой типов протезов дуги аорты и брахиоцефальной зоны.
Эти протезы различаются по количеству бранш, их диаметру, трехмерному расположению бранш. Планирование и изготовление таких групп протезов производится под конкретную клиническую ситуацию на основе трехмерных моделей, полученных при КТ, а также с учетом функциональных проб, определяющих клиническую значимость пораженных артерий.
Для повышения эффективности следует использовать две группы протезов: протезы зоны брахиоцефального сегмента и зоны дуги аорты. Каждая из этих групп позволяет персонифицировано решить уникальную клиническую задачу по протезированию в соответствующей зоне, но при этом сохраняется полная унификация соединения обеих групп протезов на завершающем этапе вмешательства.
Выбор оптимального способа протезирования и изготовление протезов сложной формы, соответствующих варианту расслоения, позволяет сократить время операции, увеличить ее радикальность, выполнить вмешательство на брахиоцефальных артериях без прекращения церебрального и системного кровотока.
Улучшение жизненного прогноза после операции на открытом сердце, кроме успешно выполненного кардиохирургического вмешательства, в высокой̆ степени зависит от соблюдения пациентом рекомендаций врача, касающихся медикаментозной терапии и физической активности, и регулярного контроля параметров сердечно-сосудистой̆ системы: уровня артериального давления (АД), контроля электрокардиограммы (ЭКГ) и т.д.
На сегодняшний̆ день потенциально эффективным инструментом являются программы дистанционного мониторинга пациентов с использованием персональных гаджетов, которые отчасти уже разработаны и могут быть внедрены в реальную клиническую практику. Использование таких программ позволяет выявлять нарушения ритма сердца, контролировать уровень артериального давления, уровень физической̆ активности и прием медикаментозной терапии пациентами после проведенной кардиохирургической операции.
На сегодняшний̆ день потенциально эффективным инструментом являются программы дистанционного мониторинга пациентов с использованием персональных гаджетов, которые отчасти уже разработаны и могут быть внедрены в реальную клиническую практику. Использование таких программ позволяет выявлять нарушения ритма сердца, контролировать уровень артериального давления, уровень физической̆ активности и прием медикаментозной терапии пациентами после проведенной кардиохирургической операции.

Использование непрерывного дистанционного мониторинга пациентов с имплантированными электрокардиостимуляторами способно обеспечить новый уровень детализации диагностических данных, позволяя расширить тактику ведения пациентов от имплантации устройства до лечения заболеваний. Удаленное наблюдение за пациентами с имплантируемыми электрокардиостимуляторами включает в себя дистанционный мониторинг, при котором выполняется контроль устройства, которое автоматически передает тревожные события, в том числе инициированные пациентом из-за опасений о возможной неисправности устройства или подозрения на аритмию или другое клиническое событие. Система удаленного мониторинга обеспечивает непрерывную диагностику и позволяет сократить количество предписанных врачом посещений клиники пациентам.
Рекомендации ESC/EACTS по реваскуляризации миокарда 2018 // Российский кардиологический журнал. 2019;(8):151–226. DOI: 10.15829/1560-4071-2019-8-151-226
Allyn J., Allou N., Augustin P. et al. Comparison of a Machine Learning Model with EuroSCORE II in Predicting Mortality after Elective Cardiac Surgery: A Decision Curve Analysis // PLoS One. 2017;6;12(1):e0169772. DOI: 10.1371/journal.pone.0169772
72. Molina R.S., Molina-Rodríguez M.A., Rincón F.M., Maldonado J.D. Cardiac Operative Risk in Latin America: A Comparison of Machine Learning Models vs EuroSCORE-II // Ann Thorac Surg. 2022;113(1):92-99. DOI: 10.1016/j.athoracsur.2021.02.052
72. Molina R.S., Molina-Rodríguez M.A., Rincón F.M., Maldonado J.D. Cardiac Operative Risk in Latin America: A Comparison of Machine Learning Models vs EuroSCORE-II // Ann Thorac Surg. 2022;113(1):92-99. DOI: 10.1016/j.athoracsur.2021.02.052
Benedetto U., Dimagli A., Sinha S. et al. Machine learning improves mortality risk prediction after cardiac surgery: Systematic review and meta-analysis // J Thorac Cardiovasc Surg. 2022. 163(6):2075-2087.e9. DOI: 10.1016/j.jtcvs.2020.07.105
Ozaki S., Kawase I., Yamashita H. et al. Aortic Valve Reconstruction Using Autologous Pericardium for Aortic Stenosis // Circ J. 2015;79(7):1504-10. DOI: 10.1253/circj.CJ-14-1092. PMID: 25818901
Pirola S., Mastroiacovo G., Mostardini G. et al. Preoperative Ozaki technique measures on tridimensional engineered root // J Cardiovasc Comput Tomogr. 2022;16(1):51-53. DOI: 10.1016/j.jcct.2021.09.008
Vegesna A., Tran M., Angelaccio M., Arcona S. Remote patient monitoring via non-invasive digital technologies: a systematic review // Telemed. J. E. Health. 2017; 23 (1): 3–17. DOI: 10.1089/ tmj.2016.0051
Varma N., Braunschweig F., Burri H. et al. Remote monitoring of cardiac implantable electronic devices and disease management // Europace. 2023. 2;25(9):euad233. DOI: 10.1093/europace/euad233
Зарегистрированные в мире лекарственные препараты или изделия, которые внедрены в практику и имеют персонализированные показания к применению
Понимание молекулярных механизмов патогенеза БСК и знания о генетической природе заболевания позволяют внедрять и новые терапевтические подходы, а также создавать новые классы препаратов.
Модуляторы функции саркомера.
Самым ярким примером может служить создание нового класса препаратов – модуляторов функции саркомера (АТФ-азной активности миозина) на основе малых молекул.
Ингибирование миозина оказалось эффективным лечебным воздействием, уменьшающим степень гипертрофии и обструкции выносящего тракта левого желудочка сердца (PMID 76878205).
Ингибирование миозина оказалось эффективным лечебным воздействием, уменьшающим степень гипертрофии и обструкции выносящего тракта левого желудочка сердца (PMID 76878205).
- В частности, появление нового препарата мавакамтена, а вслед за ним и омикамтива, является первым примером создания препарата для терапии КМП на основе знания о молекулярном патогенезе заболевания (PMID 34004177).
Препараты для лечения транстиретинового амилоидоза.
Другим примером создания препаратов на основе знания о молекулярном патогенезе заболевания являются препараты для лечения транстиретинового амилоидоза.
В настоящий момент доступно три класса различных по механизму препаратов:
В настоящий момент доступно три класса различных по механизму препаратов:
- на основе антител, стабилизрующих транстиретиновые тетрамеры;
- на основе микроРНК, снижающее синтез самого транстиретина;
- на основе антител, приводящих к разрушению и выведению нерастворимых амилоидных агрегатов.
Препараты для лечения кардиомиопатий, ассоциированных с системными и метаболическими заболеваниями.
В дополнение ряд новых препаратов активно разрабатывается в области детской кардиологии, в частности, при КМП, ассоциированных с системными и метаболическими заболеваниями.
Среди первых можно привести пример фермент-заместительной терапии у пациентов с болезнью Фабри. Также среди новых препаратов, направленных на молекулярный патогенез болезни Фабри, можно выделить шапероновую терапию, приводящую к стабилизации фермента альфа-галактозидазы, а также субстрат-редуцирующую терапию, снижающую потребность в эффективно-функционирующем нативном ферменте.
Еще одним примером может являться ферментзаместительная терапия α-глюкозидазой при болезни Помпе (PMID 31298581). Потенциальная возможность и клиническая перспективность разработки таких подходов подчеркивает важность своевременной диагностики пациентов с болезнями накопления и с КМП в рамках этих заболеваний.
Среди первых можно привести пример фермент-заместительной терапии у пациентов с болезнью Фабри. Также среди новых препаратов, направленных на молекулярный патогенез болезни Фабри, можно выделить шапероновую терапию, приводящую к стабилизации фермента альфа-галактозидазы, а также субстрат-редуцирующую терапию, снижающую потребность в эффективно-функционирующем нативном ферменте.
Еще одним примером может являться ферментзаместительная терапия α-глюкозидазой при болезни Помпе (PMID 31298581). Потенциальная возможность и клиническая перспективность разработки таких подходов подчеркивает важность своевременной диагностики пациентов с болезнями накопления и с КМП в рамках этих заболеваний.
Персонифицированные подходы применения препаратов у пациентов с РАСопатиями.
Персонифицированные подходы применения препаратов с учетом молекулярного патогенеза КМП развиваются и для еще одной тяжелой группы педиатрических пациентов – пациентов с РАСопатиями.
Поскольку в основе тяжелой гипертрофии миокарда в данном случае лежит активация проростовых и прогипертрофических сигнальных каскадов, применение различных киназных ингибиторов (МАP-киназ и тирозинкиназ) является потенциально эффективным при данной патологии. Поскольку такие препараты активно применяются в онкологии и разрешены к клиническому применению во всех возрастных группах, то попытки их использования с недавнего времени предпринимаются и в отношении пациентов с РАСопатиями.
Как единичные сообщения в формате описания клинических случаев, так и идущие клинические исследования показывают потенциальную эффективность ингибитора МЕК-киназ траметиниба. Описаны положительные эффекты данного препарата в виде уменьшения гипертрофии и обструкции левого желудочка, а также нормализация уровня NT-proBNP у пациентов первых месяцев жизни с ГКМП, вызванного мутацией RIT1 (PMID 31047013).
Несмотря на то, что эффективность и безопасность данных препаратов в отношении гипертрофии миокарда все еще остается спорной и требуют проведения более широких клинических исследований, потенциал их создания и использования в группе РАС-каскад-ассоциированной ГКМП очевиден. Среди других направлений применения уже созданных лекарств с известным действием по новым показаниям исследуется возможность применения препаратов sotatersept, tacralimus, ematinib, tamoxifen, модулирующих описанные новые молекулярные пути патогенеза, при легочной артериальной гипертензии
Поскольку в основе тяжелой гипертрофии миокарда в данном случае лежит активация проростовых и прогипертрофических сигнальных каскадов, применение различных киназных ингибиторов (МАP-киназ и тирозинкиназ) является потенциально эффективным при данной патологии. Поскольку такие препараты активно применяются в онкологии и разрешены к клиническому применению во всех возрастных группах, то попытки их использования с недавнего времени предпринимаются и в отношении пациентов с РАСопатиями.
Как единичные сообщения в формате описания клинических случаев, так и идущие клинические исследования показывают потенциальную эффективность ингибитора МЕК-киназ траметиниба. Описаны положительные эффекты данного препарата в виде уменьшения гипертрофии и обструкции левого желудочка, а также нормализация уровня NT-proBNP у пациентов первых месяцев жизни с ГКМП, вызванного мутацией RIT1 (PMID 31047013).
Несмотря на то, что эффективность и безопасность данных препаратов в отношении гипертрофии миокарда все еще остается спорной и требуют проведения более широких клинических исследований, потенциал их создания и использования в группе РАС-каскад-ассоциированной ГКМП очевиден. Среди других направлений применения уже созданных лекарств с известным действием по новым показаниям исследуется возможность применения препаратов sotatersept, tacralimus, ematinib, tamoxifen, модулирующих описанные новые молекулярные пути патогенеза, при легочной артериальной гипертензии
Молекулярно-обоснованная терапия у ламинопатий.
Еще одной группой КМП, для которой в настоящее время реализуется попытка применения молекулярно-обоснованной терапии, являются ламинопатии.
Так, после ряда экспериментальных исследований с использованием клеточных моделей и генетически-модифицированных животных была продемонстрирована потенциальная эффективность ингибиторов МАРК-киназного каскада в случае ламин-ассоциированных вариантов ДКМП, и в настоящее время завершено клиническое исследование третьей фазы препарата с применением таргетного препарата (PMID 29237693).
Речь идет об исследовании REALM-DCM (исследование ARRY-371797 (PF-07265803)) у взрослых пациентов с симптомной ДКМП, вызванной мутацией гена ламина A/C, в котором оценивалась эффективность ARRY-371797, перорального ингибитора митоген-активируемой протеинкиназы p38. Несмотря на первоначальное внимание ко взрослым, это исследование может улучшить понимание связанных генетических вариантов у детей, улучшить персонализированную стратификацию риска и обеспечить основу для разработки целевых методов лечения.
Так, после ряда экспериментальных исследований с использованием клеточных моделей и генетически-модифицированных животных была продемонстрирована потенциальная эффективность ингибиторов МАРК-киназного каскада в случае ламин-ассоциированных вариантов ДКМП, и в настоящее время завершено клиническое исследование третьей фазы препарата с применением таргетного препарата (PMID 29237693).
Речь идет об исследовании REALM-DCM (исследование ARRY-371797 (PF-07265803)) у взрослых пациентов с симптомной ДКМП, вызванной мутацией гена ламина A/C, в котором оценивалась эффективность ARRY-371797, перорального ингибитора митоген-активируемой протеинкиназы p38. Несмотря на первоначальное внимание ко взрослым, это исследование может улучшить понимание связанных генетических вариантов у детей, улучшить персонализированную стратификацию риска и обеспечить основу для разработки целевых методов лечения.
Использование вирусных носителей на основе адено-ассоциированных вирусов (AAV).
Безопасность и эффективность использования вирусных носителей на основе адено-ассоциированных вирусов (AAV) открыла новую эру в терапии генетически-обусловленных заболеваний. Это в полной мере коснулось и группы кардиомиопатий, а также генетически-обусловленных нарушений ритма. Поскольку в результате применения AAV-ассоциированной генной терапии восполняется функциональный эффект отсутствующего или дефектнофункционирующего гена, то разработка таких препаратов возможна только для кардиомиопатий, возникающих вследствие мутаций с потерей функции гена (loss of function).
Среди описанных генетических вариантов кардиомиопатий к ним, прежде всего, относятся КМП в рамках болезни Данона, а также ДКМП, ассоциированная с потерей функции белка RBM20, нарушения ритма вследствие дефектов кальциевого гомеостаза, а также для ряда митохондриальных кардиомиопатий.
Если для большинства перечисленных нозологий разработки генотерапевтических препаратов находятся на доклинической стадии, то в случае болезни Данона и ассоциированной с ней КМП промежуточные результаты активно идущего клинического исследования свидетельствуют об эффективности заместительной генной терапии в отношении LAMP2-ассоциированной гипертрофии миокарда.
Среди описанных генетических вариантов кардиомиопатий к ним, прежде всего, относятся КМП в рамках болезни Данона, а также ДКМП, ассоциированная с потерей функции белка RBM20, нарушения ритма вследствие дефектов кальциевого гомеостаза, а также для ряда митохондриальных кардиомиопатий.
Если для большинства перечисленных нозологий разработки генотерапевтических препаратов находятся на доклинической стадии, то в случае болезни Данона и ассоциированной с ней КМП промежуточные результаты активно идущего клинического исследования свидетельствуют об эффективности заместительной генной терапии в отношении LAMP2-ассоциированной гипертрофии миокарда.
Генная терапия в области кардиомиопатий и нарушений ритма.
Говоря о генной терапии в области КМП и нарушениях ритма, нельзя не упомянуть о первом заболевании с вовлечением сердечно-сосудистой системы, которое явилось объектом применения геномодифицирующей терапии. Речь идет о миодистрофии Дюшена/Бекера, частью фенотипа которых является ДКМП. Текущие руководства по лечению дистрофинопатий рекомендуют начинать терапию ингибиторами АПФ до подросткового возраста, когда пациенты находятся в стадии А (в группе риска) (PMID 30275251).
В настоящий момент ведутся попытки разработки генотип-специфичных алгоритмов расчета риска злокачественных желудочковых нарушений ритма сердца (ЖНР) и, соответственно, определения показаний к имплантации кардиовертера-дефибриллятора (ИКД), особенно для пациентов с ДКМП и аритмогенной кардиомиопатией (АКМП) на фоне частой мутации R14del в гене PLN (PMID 35699837, 34113975). Таким образом, в когорте пациентов с КМП четко прослеживается тенденция на создание ген-специфичных и даже мутаций-специфичных алгоритмов расчета риска злокачественных ЖНР и определения показаний к имплантации ИКД, что лишний раз подчеркивает важность формирования многоцентровых когорт пациентов с детальной информацией о генотип-фенотипических корреляциях.
- Первые исследования D. Duboc и соавторов показали, что ингибиторы АПФ замедляют развитие ДКМП и в итоге улучшают выживаемость (PMID 15766818, 17719312).
- Также для данных заболеваний общепризнанным эффективным генотерапевтическим подходом является exon-skipping терапия (терапия, приводящая к выключению патологических экзонов из рамки считывания – стратегия пропуска экзона). Подсчитано, что ≈70 % пациентов с делециями, ассоциированными с МДД, можно лечить с помощью стратегии пропуска экзона.
- В настоящее время US Food and Drug Administration (FDA) одобрены четыре антисмысловых олигонуклеотида (AONs), которые вводятся пациентам в виде еженедельных внутривенных инфузий, и «работают» пропуская поврежденные экзоны. Однако эта терапия ограничена определенными мутациями, сложностями проникновения AONs в ткань миокарда и скелетную мускулатуру, а также недостаточной эффективности, так как эта терапия обеспечивает лишь 5 % нормального содержания дистрофина (PMID 34898968).
- В частности, в доклинических исследованиях была показана возможность применения нуклеаз CRISPR/Cas9, способных к редактированию генома, с доставкой через аденоассоциированные вирусные векторы. Эти исследования направлены на восстановление рамки считывания гена для получения укороченного, но частично активного белка – подход, аналогичный лечению AONs. Как и в генной терапии, редактирование генов может потребовать только однократного введения. Учитывая тропность некоторых серотипов AAV к сердцу, данный подход обладает большим потенциалом в отношении ДКМП на фоне МДД (PMID 37288568).
В настоящий момент ведутся попытки разработки генотип-специфичных алгоритмов расчета риска злокачественных желудочковых нарушений ритма сердца (ЖНР) и, соответственно, определения показаний к имплантации кардиовертера-дефибриллятора (ИКД), особенно для пациентов с ДКМП и аритмогенной кардиомиопатией (АКМП) на фоне частой мутации R14del в гене PLN (PMID 35699837, 34113975). Таким образом, в когорте пациентов с КМП четко прослеживается тенденция на создание ген-специфичных и даже мутаций-специфичных алгоритмов расчета риска злокачественных ЖНР и определения показаний к имплантации ИКД, что лишний раз подчеркивает важность формирования многоцентровых когорт пациентов с детальной информацией о генотип-фенотипических корреляциях.
Персонифицированный подход в отношении генетически-обусловленных заболеваний, в частности, при кардиомиопатиях и наследственных нарушениях ритма, основан, прежде всего, на корректной постановке генетического диагноза и определении генетического дефекта, лежащего в основе заболевания, но не ограничивается этим. Современные знания о генетике кардиомиопатий позволяют разрабатывать геноспецифичные алгоритмы расчета рисков, определять показания к высокотехнологичным методам лечения и выстраивать прогноз заболевания исходя из генетического фона. Знание генетической природы и молекулярных механизмов развития заболеваний позволило разработать ряд новых геноспецифичных пепаратов для персонифицированной терапии, и их количество в ближайшее время будет постоянно увеличиваться. Комплексное ведение пациентов с КМП с учетом возрастной группы, генетического дефекта и наличия новых терапевтических подходов определяет возможности прецизионной медицины в данной группе пациентов.
https://clinicaltrials.gov
Анализ полноты исследований экспертной группой
Анализируя основные достижения российской науки и индустрии в направлении ПМ при болезнях системы кровообращения, необходимо отметить широкую географию научных исследований: научные организации практически из всех регионов РФ вовлечены в решение вопросов ПМ.
Основные направления научных исследований по ПМ при болезнях системы кровообращения в РФ направлены преимущественно на усовершенствование способов оценки индивидуального риска развития и прогрессирования заболеваний сердечно-сосудистой системы на основе идентификации причинных молекулярно-генетических маркеров и других биомаркеров, а также на изучение возможностей использования биомаркеров и генетических маркеров для мониторинга эффективности лечения и оценки прогноза пациента.
Проведение исследований по данным направлениям позволило существенно повысить диагностическую и прогностическую точность рутинных методов обследования пациентов при различных патологиях сердечно-сосудистой системы, включая такие социально значимые заболевания, как ишемическая болезнь сердца, артериальная гипертензия и хроническая сердечная недостаточность.
Однако существенным барьером на пути внедрения алгоритмов и способов персонифицированного прогнозирования клинического течения и исходов заболевания является высокая стоимость используемых лабораторных методов исследования, необходимость специальных условий и высококвалифицированных специалистов для проведения генетических исследований, что, с учетом труднодоступности отдельных удаленных районов РФ, приводит к недоступности данных методов для большинства лечебных учреждений практического здравоохранения.
Основные направления научных исследований по ПМ при болезнях системы кровообращения в РФ направлены преимущественно на усовершенствование способов оценки индивидуального риска развития и прогрессирования заболеваний сердечно-сосудистой системы на основе идентификации причинных молекулярно-генетических маркеров и других биомаркеров, а также на изучение возможностей использования биомаркеров и генетических маркеров для мониторинга эффективности лечения и оценки прогноза пациента.
Проведение исследований по данным направлениям позволило существенно повысить диагностическую и прогностическую точность рутинных методов обследования пациентов при различных патологиях сердечно-сосудистой системы, включая такие социально значимые заболевания, как ишемическая болезнь сердца, артериальная гипертензия и хроническая сердечная недостаточность.
Однако существенным барьером на пути внедрения алгоритмов и способов персонифицированного прогнозирования клинического течения и исходов заболевания является высокая стоимость используемых лабораторных методов исследования, необходимость специальных условий и высококвалифицированных специалистов для проведения генетических исследований, что, с учетом труднодоступности отдельных удаленных районов РФ, приводит к недоступности данных методов для большинства лечебных учреждений практического здравоохранения.
- С точки зрения практического внедрения, методы персонифицированной медицины наиболее актуальны для больных с доказанным высоким вкладом генетического компонента в развитие и прогрессирование заболевания. В первую очередь, это имеет отношение к наследственным кардиомиопатиям, точная генетическая диагностика которых во многом определяет тактику дальнейшего лечения и прогноз пациента, а также своевременный скрининг родственников пациента при наличии показаний, что может обеспечить у таких лиц предотвращение развития заболевания или его более позднюю манифестацию.
- Что касается заболеваний с полигенным типом наследования, таких как артериальная гипертензия и ишемическая болезнь сердца, на сегодняшний день определены сотни локусов и генов, ассоциированных с развитием и прогрессированием данных заболеваний. В научной литературе, опубликованной российскими учеными за анализируемый промежуток времени, большое внимание уделено вопросам персонифицированного прогнозирования исходов данных заболеваний в зависимости от наличия тех или иных однонуклеотидных полиморфизмов генов. Вместе с тем наиболее перспективным в данной области является проведение исследований с использованием технологий полногеномного секвенирования. Это особенно актуально для такой многонациональной страны, как РФ, поскольку этнические генетические особенности имеют место в том числе и при патологиях сердечно-сосудистой системы с полигенным типом наследования.
- Число научных исследований с применением технологий полногеномного секвенирования при БСК в РФ продолжает увеличиваться. Однако в литературе активно обсуждается несколько вопросов, связанных с данными исследованиями: экономическая эффективность данных методов исследования; проблема хранения, доступа и защиты данных полногеномного секвенирования. Ассоциации генов с теми или иными патологическими состояниями, продемонстрированные по данным полногеномного секвенирования, в дальнейшем должны верифицироваться на основании генетического анализа однонуклеотидных полиморфизмов для подтверждения наличия связи с развитием и прогрессированием заболевания, в том числе с учетом этнической принадлежности индивида.
- Исходя из приведенных данных, видна ключевая роль больших наборов данных и коллекций образцов ДНК пациентов с заболеваниями сердечно-сосудистой системы для проведения эффективных научных исследований. Решить эту проблему, вероятно, может внедрение информационных медицинских систем с возможностью их интеграции и сложной компьютерной обработки. А также создание крупных регистров по отдельным нозологиям, в том числе редким заболеваниям сердечно-сосудистой системы.
- Анализ больших объемов данных невозможен без применения технологий искусственного интеллекта. Научные исследования в области применения технологий машинного обучения и искусственного интеллекта в отечественной медицинской науке также набирают все большую популярность и позволяют получать уникальные научные данные, обладающие высокими перспективами внедрения в практическое здравоохранение, в том числе разрабатываются алгоритмы персонального расчета параметров имплантируемых клапанов сердца, стентов, применения отдельных групп лекарственных препаратов
- Проведение научных исследований по поиску молекулярно-генетических предикторов развития и прогрессирования заболеваний сердечно-сосудистой системы активно поддерживается Министерством здравоохранения РФ, Министерством науки и высшего образования РФ и Российским научным фондом
- Другой пул исследований, отвечающих критериям персонализированной медицины, относится к исследованию фундаментальных процессов жизнедеятельности клеток и тканей в норме и при патологии. Исследования отечественных ученых в данной области полностью соответствуют мировому уровню.
- Большое внимание уделяется вкладу субклеточных структур (микровезикул) в процессы воспаления, фиброгенеза, атерогенеза при сердечно-сосудистых заболеваниях. Пристальное внимание ученых обращено на такие органеллы клетки, как митохондрии. Исследование структуры и функции митохондрий в норме и при патологии, в том числе ишемическом повреждении, обеспечивает высокие перспективы обнаружения новых терапевтических мишеней, которые будут способствовать повышению эффективности медикаментозных методов лечения сердечно-сосудистых заболеваний. Исследуется роль микроРНК, которые представляют собой короткие некодирующие РНК длиной 18–25 нуклеотидов, регулирующие около трети генома на посттранскрипционном уровне. Российскими учеными показано значение микроРНК в качестве маркеров прогноза при ишемической болезни сердца, включая острый инфаркт миокарда, отторжении трансплантированного сердца, тромбозах глубоких вен, цереброваскулярных заболеваниях и т.д. Таким образом, данное направление научных работ является крайне перспективным с точки зрения позиционирования российской науки на мировом уровне и подготовки научного «фундамента» для проведения дальнейших, более практически ориентированных исследований с перспективой внедрения в рутинную клиническую практику.
Несмотря на успехи российской науки в области персонифицированной медицины по направлениям диагностики и прогнозирования болезней системы кровообращения, в вопросах применения персонализированных методов в лечении заболеваний и коррекции состояний, в том числе персонализированное применение лекарственных препаратов, основанное на анализе генетических особенностей и биомаркеров, существуют определенные трудности. На фоне общемирового роста числа препаратов с доказанным действием на геном и молекулярные механизмы реализации генетических заболеваний в РФ отечественных препаратов с таким профилем активности не зарегистрировано. Это может быть обусловлено колоссальным размером затрат, необходимых для разработки таргетных молекул, которые не могут быть компенсированы средствами государственного задания или грантом научного фонда. В данной области необходимо внедрение более масштабных мер государственной поддержки с привлечением крупных инвестиций. Развитие данного направления в медицинской науке является крайне важным в первую очередь в долгосрочной перспективе, в том числе с точки зрения импортозамещения/импортоопережения и обеспечения лекарственной безопасности населения РФ.
Сильные и слабые стороны. Предложения по перспективному планированию

Сильными сторонами направления персонализированной медицины при болезнях системы кровообращения в РФ является широкий спектр научных исследований, проводимых на высоком мировом уровне, посвященных вопросам диагностики и персонификации прогноза пациентов при различных заболеваниях сердечно-сосудистой системы. Данное направление исследований активно поддерживается научным фондом и профильными Министерствами РФ.
Вопросы разработки и применения медикаментозных препаратов с таргетной направленностью менее изучены в российской популяции. В данной области необходимо принятие управленческих решений, направленных на привлечение крупных инвестиций для разработки новых терапевтических молекул, способных модицифировать влияние патологических мутаций генов.

Ближайшими перспективами развития ПМ по направлению БСК является разработка стратегий внедрения омиксных технологий в реальную клиническую практику. Трансляция результатов научных исследований с высокой доказательной базой в клинические рекомендации по нозологиям сердечно-сосудистой системы с выделением отдельного финансирования и проработкой маршрутизации образцов биоматериала пациента в профильные научно-диагностические центры (при отсутствии возможности проведения генетической диагностики по месту жительства).
Необходимо расширение спектра специальных образовательных программ по направлению ПМ при БСК с размещением информации в сети интернет и возможностью дополнительной профессиональной подготовки на базе программы непрерывного медицинского образования. Также существует необходимость более углубленного изучения основ генетики и информационных технологий в медицинских высших учебных заведениях для подготовки специалистов, способных глубоко понимать и развивать направление персонализированной медицины, которое в обозримом будущем будет укреплять свои позиции в сфере оказания качественной медицинской помощи населению РФ.
Эндокринология
Основные направления мировых исследований
Современные представления о ПМ в эндокринологии являются классическими терапевтическими подходами, базирующимися на «трех китах» – профилактике, диагностике и лечении, но примененными с обязательным учетом индивидуальных особенностей организма (генетических, физиологических, биохимических и др.) и течения заболевания.
Значительные усилия направлены на разработку методов выявления болезни на ранних стадиях ее развития. Для прогнозирования риска необходимо выявление факторов, влияющих на риск развития заболевания. Ни один отдельно взятый фактор не способен точно спрогнозировать риск развития и характер течения заболевания, но несколько факторов, объединенные в шкалу риска, дают достаточно точный прогноз.
Основные направления исследований:
Значительные усилия направлены на разработку методов выявления болезни на ранних стадиях ее развития. Для прогнозирования риска необходимо выявление факторов, влияющих на риск развития заболевания. Ни один отдельно взятый фактор не способен точно спрогнозировать риск развития и характер течения заболевания, но несколько факторов, объединенные в шкалу риска, дают достаточно точный прогноз.
Основные направления исследований:
- Разработка полигенных и комбинированных шкал риска развития ожирения, сахарного диабета, других эндокринных заболеваний. Оценка полигенного риска позволяет не только улучшить прогноз развития заболевания, но и риск развития его осложнений.
- На основе омиксных технологий идентификация метаболитов, играющих ключевые роли в прогнозе событий (например, развитие тех или иных осложнений СД).
- Идентифицикация причинных вариантов развития моногенных форм сахарного диабета («диабет молодых со взрослым началом» – maturity-onset diabetes of the young (MODY)), характеризующийся моногенными дефектами функции β-клеток с использованием технологии экзомного секвенирования.
- Прогнозирование эффективности лечения СД2 той или иной группой препаратов на основе ПШР и комбинированных шкал.
- Разработка новых терапевтических стратегий на основе системных исследований, использующих методологию реконструкции сетей молекулярных взаимодействий.
- Разработка и использование на основе компьютерных технологий медицинских помощников, систем поддержки принятия решения в прогнозировании, диагностике и лечении ожирения, СД и других эндокринных заболеваний.
- Совершенствование систем мониторинга и контроля уровня глюкозы, например, в формате «искусственной поджелудочной железы» (закрытая петля).
- Использование клеточных технологий, основанных на замещении β-клеток для лечения больных диабетом, индукция пролиферации стволовых клеток по пути инсулин-продуцирующих клеток.
- Геномные технологии для разработки новых таргетных препаратов.
- Изучение микробиома и его изменений при различных эндокринных заболеваниях для создания пробиотиков, восстанавливающих нормальный бактериальный состав.
- Разработка систем таргетной доставки препаратов в различные органы и ткани. В частности, систем доставки препаратов в жировую ткань для активации в ней обменных процессов, браунинга и расхода энергии.
- Разработка новых способов доставки инсулина в организм: подкожные патчи; разворачивающиеся при пероральном приеме устройства с микроиглами; проглатываемые микроаппликаторы, которые прилипают к тканям желудочно-кишечного тракта и доставляют откалиброванные дозы инсулина (доклинические исследования); пероральные и ингаляционные формы инсулина.
- Предотвращение развития СД1 путем формирования иммунологической интолерантности (моноклональные антитела).
- Идентификация новых молекулярно-генетических механизмов развития нейроэндокринных опухолей, в том числе поиск новых герминальных, спорадических и соматических мутаций, приводящих к развитию этих заболеваний.
- Внедрение мультиомиксных технологий, включающих изучение метилома, транскриптома, протеома, гликома нейроэндокринных опухолей для улучшения понимания механизмов их патогенеза, биологического поведения и прогноза.
- Использование новых мишеней таргетной терапии нейроэндокринных опухолей.
- Разработка способов прогнозирования ответа на различные виды лечения нейроэндокринных опухолей.
- Внедрение тераностики в алгоритмы ведения больных с нейроэндокринными опухолями.
Основные достижения ПМ и примеры успешной реализации в мире
1
Диабет и ожирение
GWAS показали вклад полигенных изменений в риск ожирения. К настоящему времени разработаны полигенные шкалы риска (ПШР) ожирения, которые позволяют определить людей, имеющих увеличенный риск его развития.
- Так, ПШР,разработанная в 2019 г. на основании анализа четырех когорт (UKBB, Partners Healthcare, Framingham Offspring/CARDIA и Avon Longitudinal Study of Parents and Children), показала, что 43 % участников, имевших самый высокий 10 % риск по ПШР, страдали ожирением (ИМТ≥30 кг/м2) по сравнению с 9,5 % среди тех, кто был в самом низком 10 % риске.
- GWAS выявили множество генетических локусов, связанных с СД2. По отдельности эти генетические варианты имеют очень небольшой эффект, но комбинация сотен наиболее значимых из них в ПШР может дать существенный вклад в прогнозирование риска полигенных заболеваний, таких как СД2.
- ПШР показали многообещающие результаты в предикции СД2. Однако большинство исследований показало, что комбинация клинических факторов риска (возраст, пол, ИМТ, СД у родителей, уровни давления, ХС-ЛПВП и триглицеридов) обеспечивала более точный прогноз для развития СД2, чем ПШР [C-статистическая-величина: 0,835 (0,831–0,839) по сравнению с 0,763 (0,758–0,767) соответственно].
- В то же время добавление ПШР к клиническим моделям риска способно в определенной мере улучшить прогноз.
Еще одним важным фактором, влияющим на точность генетического прогнозирования СД2 и других полигенных заболеваний, является расовая и национальная принадлежность. Из уже установленных фактов на это указывает более быстрая прогрессия СД у азиатов и более высокая чувствительность к инкретиномиметикам у людей страдающих СД2 и проживающих в Китае и Японии.
Геномные исследования служат толчком для создания новых лекарственных препаратов. Например, было показано, что полиморфизм в гене TCF7L2 опосредует терапевтический эффект аналогов глюкагоноподобного пептида-1. Гены PPARG и KCNJ11 функционально связаны с мишенями для сахароснижающих препаратов –тиазолидиндионов и производных сульфонилмочевины.
Использование технологии экзомного секвенирования позволило идентифицировать новые причинные мутации моногенных форм сахарного диабета, например, обнаружены дефекты в гене GATA6. Такие исследования позволяют понять механизм реализации патологического процесса, поэтому необходимы в клинической практике для постановки своевременного диагноза.
Использование технологии экзомного секвенирования позволило идентифицировать новые причинные мутации моногенных форм сахарного диабета, например, обнаружены дефекты в гене GATA6. Такие исследования позволяют понять механизм реализации патологического процесса, поэтому необходимы в клинической практике для постановки своевременного диагноза.
Разработка медицинских помощников и систем поддержки принятия решения наиболее активно развивается в прогнозировании, диагностике и лечении ожирения, СД и других эндокринных заболеваний. При СД искусственный интеллект в сочетании с медицинскими приборами, носимыми устройствами и смартфонами, может помочь врачам и пациентам, улучшая прогнозирование риска и диагностические модели, тем самым повышая персонализацию лечения и самоконтроль заболевания.
При гестационном диабете разработано несколько приложений mHealth для регистрации информации о пациентке и предоставления общих советов и рекомендаций. Однако, по данным иностранной литературы, практически нет инструментов, объединяющих mHealth и ИИ, которые были бы созданы для расширения возможностей женщин с гестационным диабетом и помощи в принятии клинических решений как медицинскими работниками, так и пациентами [13].
- В ходе шестинедельного исследования было показано, что усовершенствованный болюсный калькулятор на основе ИИ для лечения диабета 1-го типа эффективен в качестве вспомогательной системы для самостоятельного лечения этого заболевания, причем у пациентов, использующих это устройство, не наблюдалось эпизодов гипогликемии.
- В метанализе исследований влияния мобильных приложений на контроль гликемии у молодых пациентов с СД 1-го типа вспомогательные приложения с калькулятором углеводов и доз инсулина благоприятно влияли на снижение HbA1c.
При гестационном диабете разработано несколько приложений mHealth для регистрации информации о пациентке и предоставления общих советов и рекомендаций. Однако, по данным иностранной литературы, практически нет инструментов, объединяющих mHealth и ИИ, которые были бы созданы для расширения возможностей женщин с гестационным диабетом и помощи в принятии клинических решений как медицинскими работниками, так и пациентами [13].
В последние годы различные миРНК определены как возможные цели лечения, однако практическая разработка таких препаратов только начинается.
- В 2022 г. в России зарегистрирован инновационный инъекционный препарат для лечения дислипидемии – инклисиран (торговое наименование Симбрава). Это первый и единственный в классе гиполипидемических средств препарат, созданный на основе малой интерферирующей РНК.
- Препарат инклисиран показан для лечения пациентов с первичной гиперхолестеринемией (семейной гетерозиготной и несемейной гиперхолестеринемией) или смешанной дислипидемией в качестве дополнения к диете.
- Основанием для регистрации инклисирана стали результаты клинических испытаний III фазы ORION-9, -10 и -11. В клинических исследованиях приняли участие более 3,5 тыс. пациентов с сердечно-сосудистыми заболеваниями или гетерозиготной семейной гиперхолестеринемией, принимающих максимальные дозы статинов. Одна инъекция инклисирана в шесть месяцев достоверно снижала уровень ХЛНП на 52 % относительно исходного уровня к 17-му месяцу терапии и удерживал его снижение на 54 % на постоянном уровне в течение последующего периода лечения.
Первая коммерческая замкнутая система MiniMed 670G (Medtronic, Northridge, CA, USA) была одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США еще в сентябре 2016 г. для использования людьми с диабетом 1-го типа в возрасте от 14 лет и старше. Дальнейшее развитие технологий в этом направлении шла, с одной стороны, по пути микронизации, точности и скорости реагирования, с другой – по пути создания бигормональных систем, сочетающих глюкагон или амилин с инсулином.
В последние годы ведутся работы, предполагающие использование клеточных технологий, основанных на замещении β-клеток для лечения больных диабетом. Стволовые клетки могут быть потенциальным источником инсулин-продуцирующих клеток. Результаты показывают, что в качестве источника инсулин-продуцирующих клеток для аллогенной трансплантации могут выступать как эмбриональные, так и взрослые стволовые клетки. Основной проблемой остается обеспечение иммунологической интолерантности полученных β-клеток, что обеспечивается созданием «обезличенных» клеток и созданием микросфер с селективной проницаемостью.
В плане разработки новых методов доставки инсулина в организм клинические испытания ведутся для пероральных инсулинов.
Компания Орамед начала клиническое исследование (КИ) комбинированного перорального инсулина с ингибиторами ферментов ORMD-0801 в ноябре 2020 г., в настоящее время исследование завершилось.
Компания Орамед начала клиническое исследование (КИ) комбинированного перорального инсулина с ингибиторами ферментов ORMD-0801 в ноябре 2020 г., в настоящее время исследование завершилось.
- Первоначальный анализ показал, что исследование не достигло первичной конечной точки, однако в дальнейшем установлено, что субпопуляция пациентов с объединенными специфическими параметрами, такими как индекс массы тела (ИМТ), исходный уровень HbA1c, возраст, пол и масса тела, хорошо реагировала на пероральный инсулин.
- Эти подгруппы продемонстрировали статистически значимое снижение HbA1c с поправкой на плацебо более, чем на 1 %.
- Из сверхдлинных стоит отметить инсулин, который вводится один раз в неделю – Icodec. Комапания Новонордиск завершила КИ данного препарата и в августе 2023 г. заявила о намерении подать заявку на его регистрацию в США, ЕС и Китае.
Исследования, направленные на предотвращение развития СД1 путем формирования иммунологической интолерантности (моноклональные антитела), увенчались успехом в 2022 г.: 17 ноября 2022 г. впервые в истории диабетологии FDA (США) зарегистрировало препарат – теплизумаб – для замедления развития СД 1-го типа (СД1) у взрослых и детей в возрасте 8 лет и старше, у которых в настоящее время диагностирован СД1 на «доклинической» стадии, т.е. при наличии дисгликемии недиабетического уровня и нескольких специфических антител к β-клеткам поджелудочной железы.
Одобрение препарата получено по итогам исследования TriaL Net-10, в котором внутривенно вводили теплизумаб (антитело к СD3) в течение 14 дней и получили снижение на 40 % вероятности развития СД1 за период наблюдения.
Одобрение препарата получено по итогам исследования TriaL Net-10, в котором внутривенно вводили теплизумаб (антитело к СD3) в течение 14 дней и получили снижение на 40 % вероятности развития СД1 за период наблюдения.
- При долгосрочном наблюдении за участниками исследования было зафиксировано, что клинический дебют СД1 удавалось отсрочить на 2,5–3 года!
- Несмотря на относительную скромность исследования, нельзя не выделить принципиально новый долгожданный результат: появилось антитело, способное существенно замедлить развитие СД1 у лиц с высокой вероятностью его развития (родственники лиц с СД1, имеющие антитела к глутаматдекарбоксилазе и дисгликемию недиабетического уровня), но не для людей с уже состоявшимся дебютом СД1, что определяет «терапевтическое окно» времени вмешательства.
Арсенал средств для лечения СД 2-го типа (СД2) пополнился новым препаратом – двойным агонистом рецепторов глюкагоноподобного пептида 1-го типа и глюкозозависимого инсулинотропного полипептида.
Этот препарат – Тирзепатид (Mounjaro™) – был одобрен в мае 2022 г. FDA (США) для подкожных инъекций один раз в неделю для контроля гликемии.
Этот препарат – Тирзепатид (Mounjaro™) – был одобрен в мае 2022 г. FDA (США) для подкожных инъекций один раз в неделю для контроля гликемии.
- В программе исследований SURPASS (всего восемь исследований третьей фазы) было показано, что препарат не только эффективно снижает уровень гликированного гемоглобина (HbA1c), но и превосходит все препараты сравнения по степени снижения массы тела.
- В США препарат одобрен в трех дозах (5, 10 или 15 мг).
- Лечение препаратом приводит к снижению HbA1c на 1,8–2,0 пункта и массы тела на 7–10 кг (в зависимости от дозы) в течение 40 недель лечения. 2/3 участников исследования (более 60 %), принимавших самую высокую дозу, удалось снизить массу тела на 20 %.
Персонифицированная терапия пациентов с СД2 и хронической болезнью почек (ХБП) пополнилась нестероидным антагонистом минералокортикоидных рецепторов (МКР).
Первый представитель этого класса препаратов – финеренон, зарегистрирован в США и Европе в 2022 г.
Первый представитель этого класса препаратов – финеренон, зарегистрирован в США и Европе в 2022 г.
- В серии рандомизированных клинических исследований (FIDELIO-DKD и FIGARO-DKD, объединенных в программу FIDELITY) препарат доказал высокую эффективность не только как нефропротектор, но и в качестве кардиопротектора.
- Через три года терапии финереноном, в добавление к максимально переносимым дозам ингибиторов ренин-ангиотензиновой системы, у пациентов с СД2 и ХБП отмечалось значимое снижение рисков сердечно-сосудистых событий на 14 % (Р = 0,0018) и почечных событий на 23 % (P = 0,0002), независимо от исходных значений расчетной скорости клубочковой фильтрации, уровня альбуминурии, HbA1c.
- Механизм нефропротективного действия препарата связывают с противовоспалительным и антифибротическим действиями антагонистов МКР на уровне почечного интерстиция, что является уникальным и не присущим другим классам нефропротекторов (блокаторам ренин-ангиотензиновой системы и глифлозинам).
- Существенное преимущество этого класса препаратов, в отличие от стероидных антагонистов МКР, – значимо меньшее развитие побочных явлений, таких как гиперкалиемия и гирсутизм.
Установлено, что применение пиоглитазона в малых дозах позволяет снизить риск развития инсульта, инфаркта миокарда, а также развития СД2 у лиц без СД. При этом риск развития отечного синдрома, в том числе прогрессирования сердечной недостаточности, а также набора массы тела был ниже на фоне приема доз менее 45 мг/сут.
Дополнительно, несмотря на данные мета-анализов, свидетельствующих о нейтральных эффектах ингибиторов натрий-глюкозного котранспортера 2-го типа (иНГЛТ-2) в отношении фатальных, нефатальных инсультов, а также относительно влияния на частоту развития инсультов в целом, наблюдаются различия во влиянии препаратов на частоту различных подтипов инсультов.
Дополнительно, несмотря на данные мета-анализов, свидетельствующих о нейтральных эффектах ингибиторов натрий-глюкозного котранспортера 2-го типа (иНГЛТ-2) в отношении фатальных, нефатальных инсультов, а также относительно влияния на частоту развития инсультов в целом, наблюдаются различия во влиянии препаратов на частоту различных подтипов инсультов.
- В мета-анализе 2021 г. показано, что терапия ни одним из исследуемых иНГЛТ-2 не приводит к уменьшению частоты ишемического инсульта и транзиторных ишемических атак, однако терапия канаглифлозином (КАНА) в исследовании CANVAS вызвала снижение риска геморрагического инсульта (RR = 0,434, 95 % CI 0,207–0,912, p = 0,027) [21]. Примечательно, что терапия КАНА достоверно уменьшала риск инсульта у пациентов с СД2 и снижением скорости клубочковой фильтрации (СКФ) менее 45 мл/мин ∙ 1,73 м2 по результатам апостериорного анализа исследований CANVAS и CREDENCE, достоверно не влияя на риск инсульта у пациентов с сохранной СКФ.
- Результаты мета-анализа 2021 г. показали, что применение иНГЛТ-2 ассоциировано со снижением риска фибрилляции предсердий на 18 % (RR = 0,82, 95% CI 0,70–0,96) и закономерно сопровождается уменьшением риска кардио-эмболического подтипа ишемического инсульта на 68 % (RR = 0,32, 95 % CI 0,12–0,85) по сравнению с плацебо.
Разработаны препараты для лечения моногенных форм ожирения. Начато исследование IIb фазы (Trial Id: NCT05198362) по изучению эффективности и безопасности препарата Tesomet – фиксированной комбинации ингибитора обратного захвата моноаминов (tesofensine) и β-1-селективного блокатора (metoprolol) при лечении гипоталамического ожирения в рамках синдрома Прадера – Вилли.
- К сожалению, исследование препарата было приостановлено в октябре 2021 г. компанией-производителем Saniona в связи с ограниченным финансированием.
При таких орфанных синдромах, характеризующихся гиперфагией, как синдромы Альстрема и Барде – Бидля, перспективно использование сетмеланотида – вещества, восстанавливающего нарушенную работу рецептора меланокортина (MC4R).
- Проведено многоцентровое рандомизированное 52-недельное исследование III фазы этого препарата (ClinicalTrials.gov, NCT03746522). Препарат обеспечил хорошее снижение массы тела у детей с синдромами Барде – Бидля, но при синдроме Альстрема эффективность препарата доказать не удалось.
Важность лечения ожирения, в том числе не только распространенного экзогенно-конституционального, но и орфанных, моногенных форм, трудно переоценить. Поэтому важной инновацией в изменении структуры эндокринологической службы в стране стало создание особого Центра лечения ожирения на базе ГНЦ ФГБУ «НМИЦ эндокринологии» Минздрава России.
2
Нейроэндокринология
В течение последних лет ведутся активные исследования, направленные на расшифровку молекулярных характеристик нейроэндокринных опухолей (НЭО) гипофиза (PitNET). Полученные данные представляют особый интерес, так как открывают возможности для персонализированной терапии.
Соматотропиномы являются наиболее часто встречающимися функционирующими НЭО гипофиза.
Соматотропиномы являются наиболее часто встречающимися функционирующими НЭО гипофиза.
- Нейрохирургию считают первой линией лечения этого заболевания, но она позволяет достичь ремиссии только у половины пациентов.
- При неэффективности хирургического лечения используют медикаментозную терапию; в большинстве случаев препаратами выбора являются аналоги соматостатина (АС) первого поколения, однако, по данным проспективных исследований, контроль заболевания достигается только в 30–40 % случаев.
В ряде случаев применение АС первого поколения ограничивает не только недостаточная эффективность, но и необходимость парентерального введения препаратов, что нередко доставляет дискомфорт пациенту и, учитывая необходимость длительного введения, влияет на качество жизни.
Также известно, что АС могут оказавать неблагоприятное влияние на углеводный обмен, что приводит к ограничениям в их использовании, особенно у больных с плохо компенсируемым сахарным диабетом. Все это стало поводом для создания новых форм АС первого поколения и молекул, оказывающих эффект, подобный действию АС.
Одним из таких препаратов является палтусотин (Paltusotine) – представитель принципиально нового класса оральных селективных небелковых (не-пептидных) агонистов соматостатиновых рецепторов 2-го типа, разработанный фармацевтической компанией Сrinetics.
В настоящее время препарат находится во второй фазе как препарат для лечения карциноидного синдрома (NCT05361668). Исследования последних лет также направлены на создание прогностических шкал или моделей предикции ответа на терапию АС первого поколения.
Также известно, что АС могут оказавать неблагоприятное влияние на углеводный обмен, что приводит к ограничениям в их использовании, особенно у больных с плохо компенсируемым сахарным диабетом. Все это стало поводом для создания новых форм АС первого поколения и молекул, оказывающих эффект, подобный действию АС.
Одним из таких препаратов является палтусотин (Paltusotine) – представитель принципиально нового класса оральных селективных небелковых (не-пептидных) агонистов соматостатиновых рецепторов 2-го типа, разработанный фармацевтической компанией Сrinetics.
- В исследованиях второй фазы получены данные об эффективности и безопасности применения этого препарата у больных акромегалией.
- В сентябре 2023 г. объявлено о завершении исследования палтусотина третьей фазы PATHFNDR-1(NCT04837040), которое подтвердило эти результаты.
- В 2024 г. планируется завершить еще одно исследование третьей фазы PATHFNDR-2 (NCT05192382).
В настоящее время препарат находится во второй фазе как препарат для лечения карциноидного синдрома (NCT05361668). Исследования последних лет также направлены на создание прогностических шкал или моделей предикции ответа на терапию АС первого поколения.
- Так исследователями из Бразилии на основе машинного обучения разработана модель предикции ответа на терапию АС первого поколения при лечении акромегалии.
- Эта модель включает данные о поле пациента, возрасте на момент диагностики заболевания, уровнях гормона роста и инсулиноподобного фактора роста-1, данные об экспрессии соматостатиновых рецепторов 2 и 5-го типов в соматотропиномах, а также о паттернах грануляции цитокератина (плотно- или редкогранулированные).
- Точность модели оказалась 86,3 %, положительная прогностическая ценность 83,3 % и отрицательная прогностическая ценность 87,5 %.
Несмотря на активный поиск, в настоящее время отсутствуют новые опухоль-ориентированные препараты для лечения НЭО гипофиза, секретирующих адренокортикотропный гормон.
- Тем важнее исследования, закончившиеся в 2022 г., полученные результаты которых в ближайшем будущем могут изменить нашу практику лечения больных гиперкортицизмом.
- В первую очередь это относится к препарату осилдростат (торговое название «истуриса»), ингибитору 11-бета-гидроксилазы, отличающемуся от разрешенного ЕМА и используемого в течение более 50 лет препарата метопирон (метирапон) большей продолжительностью действия и меньшим количеством побочных эффектов.
- В 2022 г. опубликованы результаты двух многоцентровых исследований, подтвердивших высокую эффективность препарата, позволившую на сегодняшний день рекомендовать этот ингибитор стероидогенеза ЕМА и FDA при лечении всех форм гиперкортизолизма, если не достигнуто излечение хирургическим путем.
Постоянно расширяется использование, особенно в сфере нейроэндокринологии и онкоэндокринологии, пептидов как носителей радиоактивной метки с двойным применением – тераностиков, т.е. препаратов, используемых с диагностической и лечебной целью.
Потенциальный переворот в диагностике кортикотропином, позволяющий уточнять и латерализацию, может достигаться при проведении ПЭТ/КТ с использованием меченного галлием кортиколиберина 68Ga CRH.
Потенциальный переворот в диагностике кортикотропином, позволяющий уточнять и латерализацию, может достигаться при проведении ПЭТ/КТ с использованием меченного галлием кортиколиберина 68Ga CRH.
- Из 24 наблюдений в 100 % случаев была получена идентификация кортикотропином, причем даже не выявляемых на МРТ. Дополнительное наложение изображения ПЭТ на МРТ обеспечивало латерализацию опухоли, при этом в случаях эктопических опухолей, продуцирующих адренокортикотропный гормон (АКТГ), захвата в гипофизе не выявляли.
- Если дальнейшие исследования на большем количестве больных подтвердят эти данные, появится надежная неинвазивная альтернатива катетеризации каменистых синусов, причем с лучшими результатами.
В настоящее время наиболее широко изучаются возможности применения петидов DOTATOC и DOTATATE, являющихся аналогами соматостатина, в диагностике и лечении нейроэндокринных опухолей.
Эти пептиды, хелатированные с радиоизотопами, используемыми при позитронно эмиссионной томографии (ПЭТ), а именно Ga-68 для диагностики и Lu-177 для пептидной рецепторной радионуклидной терапии (ПРРТ), составляют так называемые тераностические пары.
Эти пептиды, хелатированные с радиоизотопами, используемыми при позитронно эмиссионной томографии (ПЭТ), а именно Ga-68 для диагностики и Lu-177 для пептидной рецепторной радионуклидной терапии (ПРРТ), составляют так называемые тераностические пары.
- По результатам исследования NETTER-1 в 2018 г. Lu-177-DOTATATE уже одобрен для лечения НЭО желудочно-кишечного тракта (ЖКТ) и поджелудочной железы (ПЖ) стадий G1 and G2.
- В настоящее время продолжаются исследования третьей фазы препаратов Lu-177-DOTATATE (NETTER-2, NCT03972488) и Lu-177-Edotreotide (DOTATOC) (COMPOSE, NCT04919226) при лечении НЭО ЖКТ и ПЖ стадий G2 и G3.
С учетом того, что не все НЭО экспрессируют большое количество соматостатиновых рецепторов 2-го типа (ССР2), ведется разработка антагонистов этих рецепторов, которые обладают большей связывающей способностью с опухолевыми клетками по сравнению с агонистами ССР2, и являются новыми кандидатами для формирования тераностических пар.
Также создаются новые радиоизотопы для лечения НЭО, например, Tb-161(тербиум-161).
Таким образом, многообразие радиоизотопов и пептидов, применяемых и разрабатываемых для тераностики НЭО, позволит реализовать персонализированный подход к лечению НЭО различных локализаций и различными особенностями экспрессии соматостатиновых рецепторов.
Также создаются новые радиоизотопы для лечения НЭО, например, Tb-161(тербиум-161).
Таким образом, многообразие радиоизотопов и пептидов, применяемых и разрабатываемых для тераностики НЭО, позволит реализовать персонализированный подход к лечению НЭО различных локализаций и различными особенностями экспрессии соматостатиновых рецепторов.
3
Клиническая эндокринология
Активно внедряются в практику антитела к фрагментам клеток или клеточным рецепторам, а также селективные рецепторные модуляторы.
Важным оказался успех антитела к рецептору инсулиноподобного фактора роста 1-го типа, тепротумумаба в лечении эндокринной офтальмопатии и, как выяснилось позже, претибиальной микседемы. R. Crespo-Trevino и соавторы доказали эффективность п
репарата и при этом ассоциированном с болезнью Грейвса аутоиммунном поражении.
Важным оказался успех антитела к рецептору инсулиноподобного фактора роста 1-го типа, тепротумумаба в лечении эндокринной офтальмопатии и, как выяснилось позже, претибиальной микседемы. R. Crespo-Trevino и соавторы доказали эффективность п
репарата и при этом ассоциированном с болезнью Грейвса аутоиммунном поражении.
В 2022 г. опубликованы работы, потенциально способные изменить лечение классических форм врожденной дисфункции коры надпочечников (ВДКН), при которой соблюдение баланса между подавлением продукции андрогенов, достижимым только на супрафизиологических дозах глюкостероидов, и отсутствием передозировки стероидов далеко не всегда возможно, особенно у взрослых.
К настоящему времени несколько молекул доказали потенциальную эффективность – Tildacerfont, предложенный для лечения взрослых. По данным K. Sarafoglou и соавторов, этот нестероидный антагонист рецептора 1-го типа к кортиколиберину обладает высокой связывающей активностью и активно снижает секрецию АКТГ, что позволяет у лиц с ВДКН снизить продукцию предшественников надпочечниковых андрогенов.
К настоящему времени несколько молекул доказали потенциальную эффективность – Tildacerfont, предложенный для лечения взрослых. По данным K. Sarafoglou и соавторов, этот нестероидный антагонист рецептора 1-го типа к кортиколиберину обладает высокой связывающей активностью и активно снижает секрецию АКТГ, что позволяет у лиц с ВДКН снизить продукцию предшественников надпочечниковых андрогенов.
- Это уже вторая попытка выпустить подобные молекулы, и на основании двух законченных исследований (NCTJ03257464 и NCT03687242) получены данные о снижении продукции АКТГ, андростендиона и 17-оксипрогестерона при хорошей переносимости препарата. Вопросы оптимальной биодоступности этого липофильного препарата, как и оптимальных дозировок, станут предметом дальнейших исследований.
Разработан препарат Macimorelin – синтетический агонист рецептора к грелину для тестов на секрецию соматотропного гормона, прирост оценивается при пероральном приеме. Возможно, мы простимся с инсулиновой гипогликемией как тестом в поисках дефицита гормона роста. Впрочем, стоимость этого препарата сегодня так велика, что радость по поводу его появления может быть преждевременной.
Для усовершенствования диагностики эктопированных и множественных аденом околощитовидных желез у больных первичным гиперпаратиреозом (ПГПТ) в настоящее время в мире предложено использование ПЭТ/КТ с 11С-метионином или холином.
Расширение показаний для этого метода с включением больных ПГПТ позволяет улучшить диагностику, повысить эффективность оперативного лечения и обеспечить лучший прогноз заболевания. Данная методика в 2021–2023 гг. активно используется и в РФ.
Расширение показаний для этого метода с включением больных ПГПТ позволяет улучшить диагностику, повысить эффективность оперативного лечения и обеспечить лучший прогноз заболевания. Данная методика в 2021–2023 гг. активно используется и в РФ.
Лечение ахондроплазии не входит в функцию эндокринолога в нашей стране, тем не менее многим врачам будет интересно сообщение, что FDA разрешило препарат Vosoritide (Voxzogo), вводимый ежедневно в виде инъекций, для лечения детей с этим заболеванием в возрасте от пяти лет с открытыми зонами роста. Генетически детерминированное заболевание, ахондроплазия, связано с аномалиями энхондрального окостенения, блокатором которого является СNP, натрийуретический пептид. По химической структуре Vosoritide является аналогом CNP, и его применение позволяет улучшить ростовой прогноз.
Locke A.E., Kahali B., Berndt S.I. et al. Genetic studies of body mass index yield new insights for obesity biology //Nature. 2015;518:197–206. DOI: 10.1038/nature14177
Khera A.V., Chaffin M., Wade K.H. et al. Polygenic prediction of weight and obesity trajectories from birth to adulthood // Cell. 2019;177:587–596.e9. DOI: 10.1016/j.cell.2019.03.028
Khera A.V., Chaffin M., Wade K.H. et al.Polygenic prediction of weight and obesity trajectories from birth to adulthood // Cell.2019;177:587–596.e9. DOI: 10.1016/j.cell.2019.03.028
Murthy V.L., Xia R., Baldridge A.S. et al.Polygenic risk, fitness, and obesity in the coronary artery risk development in young adults (CARDIA) study // JAMA Cardiol.2020;5:40–48.
Murthy V.L., Xia R., Baldridge A.S. et al.Polygenic risk, fitness, and obesity in the coronary artery risk development in young adults (CARDIA) study // JAMA Cardiol.2020;5:40–48.
Tremblay J., Haloui M., Attaoua R. et al. Polygenic risk scores predict diabetes complications and their response to intensive blood pressure and glucose control // Diabetologia. 2021;64:2012–2025. DOI: 10.1007/s00125-021-05491-7
Rosenberg N.A., Edge M.D., Pritchard J.K., Feldman M.W. Interpreting polygenic scores, polygenic adaptation, and human phenotypic differences // Evol Med Public Heal. 2019;1:26–34. DOI: 10.1093/emph/eoy036
He Y., Lakhani C.M., Rasooly D. et al. Comparisons of polyexposure, polygenic, and clinical risk scores in risk prediction of type 2 diabetes // Diabetes Care. 2021;44:935–943. DOI: 10.2337/dc20-2049
He Y., Lakhani C.M., Rasooly D. et al. Comparisons of polyexposure, polygenic, and clinical risk scores in risk prediction of type 2 diabetes // Diabetes Care. 2021;44:935–943. DOI: 10.2337/dc20-2049
Mars N., Koskela J.T., Ripatti P. et al. Polygenic and clinical risk scores and their impact on age at onset and prediction of cardiometabolic diseases and common cancers // Nat Med.2020;26:549–557. DOI: 10. 1038/s41591-020-0800-0
Mars N., Koskela J.T., Ripatti P. et al. Polygenic and clinical risk scores and their impact on age at onset and prediction of cardiometabolic diseases and common cancers // Nat Med.2020;26:549–557. DOI: 10. 1038/s41591-020-0800-0
Raal F.J., Kallend D., Ray K.K. et al. Inclisiran for the treatment of heterozygous familial hypercholesterolemia // N Engl J Med. 2020;382(16):1520-1530. DOI: 10.1056/NEJMoa1913805
Ray K.K., Wright R.S., Kallend D. et al. Two Phase 3 Trials of Inclisiran in patients with elevated LDL cholesterol // N Engl J Med. 2020;382(16):1507-1519. DOI: 10.1056/NEJMoa1912387
Hirsch J.S. FDA approves teplizumab: a milestone in type 1 diabetes // Lancet Diabetes Endocrinol. 2023;11(1):18. DOI: 10.1016/S2213-8587(22)00351-5
Rosenstock J., Wysham C., Frías J.P. et al. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): a double-blind, randomised, phase 3 trial // Lancet. 2021;398(10295):143-155. DOI: 10.1016/S0140-6736(21)01324-6
Agarwal R., Filippatos G., Pitt B. et al. Cardiovascular and kidney outcomes with finerenone in patients with type 2 diabetes and chronic kidney disease: FIDELITY pooled analysis // EurHeart J. 2022;43(6):474-484. DOI: 10.1093/eurheartj/ehab777
González-Juanatey J.R., Górriz J.L., Ortiz A. et al. Cardiorenal benefits of finerenone: protecting kidney and heart // Ann Med. 2023;55(1):502-513. DOI: 10.1080/07853890.2023.2171110
Tsai W.H., Chuang S.M., Liu S.C. et al. Effects of SGLT2 inhibitors on stroke and its subtypes in patients with type 2 diabetes: a systematic review and meta-analysis // Scient Rep. 2021.11(1):15364. DOI: 10.1038/s41598-021-94945-4
Li H.L., Lip G., Feng Q. et al. Sodium-glucose cotransporter 2 inhibitors (SGLT2i) and cardiac arrhythmias: a systematic review and meta-analysis // Cardiovasc Diabetol. 2021; 20(1): 100. DOI: 10.1186/s12933-021-01293-8
Haqq A.M., Chung W.K., Dollfus H. et al. Efficacy and safety of setmelanotide, a melanocortin-4 receptor agonist, in patients with Bardet-Biedl syndrome and Alström syndrome: a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial with an open-label period // Lancet Diabetes Endocrinol. 2022;10(12):859-868. DOI: 10.1016/S2213-8587(22)00277-7
Gadelha M., Bex M., Feelders R.A. et al. Randomized trial of osilodrostat for the treatment of cushing disease // J Clin Endocrinol Metab. 2022;107(7):e2882-e2895. DOI: 10.1210/clinem/dgac178
Fleseriu M., Newell-Price J., Pivonello R. et al. Long-term outcomes of osilodrostat in Cushing’s disease: LINC 3 study extension // Eur J Endocrinol. 2022;187(4):531-541. DOI: 10.1530/EJE-22-0317
Fleseriu M., Newell-Price J., Pivonello R. et al. Long-term outcomes of osilodrostat in Cushing’s disease: LINC 3 study extension // Eur J Endocrinol. 2022;187(4):531-541. DOI: 10.1530/EJE-22-0317
Fleseriu M., Newell-Price J., Pivonello R. et al. Long-term outcomes of osilodrostat in Cushing’s disease: LINC 3 study extension // Eur J Endocrinol. 2022;187(4):531-541. DOI: 10.1530/EJE-22-0317
Walia R., Gupta R., Bhansali A. et al. Molecular imaging targeting corticotropin-releasing hormone receptor for corticotropinoma: a changing paradigm // J Clin Endocrinol Metab. 2021;106(4):1816-1826. DOI: 10.1210/clinem/dgaa755
Crespo-Trevino R., Schiffman J., Ugradar S. et al. Thyroid dermopathy responds to teprotumumab therapy // Endocrinol Diabetes Metab Case Reports. 2022;2022(10295):143-155. DOI: 10.1530/EDM-21-0201
Sarafoglou K., Barnes C.N., Huang M. et al. Tildacerfont in adults with classic congenital adrenal hyperplasia: results from two phase 2 studies // J Clin Endocrinol Metab. 2021;106(11):e4666-e4679. DOI: 10.1210/clinem/dgab438
Auchus R.J., Sarafoglou K., Fechner P.Y. et al. Crinecerfont lowers elevated hormone markers in adults with 21-hydroxylase deficiency congenital adrenal hyperplasia // J Clin Endocrinol Metab. 2022;107(3):801-812. DOI: 10.1210/clinem/dgab749
Зарегистрированные в мире лекарственные препараты или изделия, которые внедрены в практику и имеют персонализированные показания к применению
Тирзепатид (Mounjaro™)
– новый препарат, двойной агонист рецепторов глюкагоноподобного пептида 1-го типа и глюкозозависимого инсулинотропного полипептида (одобрен в мае 2022 г. FDA (США) для подкожных инъекций один раз в неделю для контроля гликемии).
На сегодняшний день этот препарат является непревзойденным по эффективности средством для лечения СД2 в сочетании с ожирением. В 2023 г. планируется ускоренное рассмотрение FDA нового показания для этого препарата, а именно лечение ожирения без сопутствующего СД2.
Финеренон
– первый представитель нового класса препаратов, нестероидный антагонист минералокортикоидных рецепторов (МКР) зарегистрирован в 2022 г. в США и Европе для лечения пациентов с СД2 и хронической болезнью почек, который в серии рандомизированных клинических исследований (FIDELIO-DKD и FIGARO-DKD, объединенных в программу FIDELITY) доказал высокую эффективность в качестве кардионефропротектора.
Осилдростат
– ингибитор 11-бета-гидроксилазы, одобрен ЕМА и FDA для лечения всех форм гиперкортизолизма.
Меченный галлием кортиколиберин (68Ga CRH)
– тераностик в области нейро- и онкоэндокринологии.
Палтусотин
– оральный селективных небелковый (не-пептидный) агонист соматостатиновых рецепторов 2, разработан для лечения акромегалии и карциноидного синдрома.
Tesofensine +metoprolol (Tesomet)
– комбинация ингибитора обратного захвата моноаминов и β-1-селективного блокатора для лечения синдрома Прадера – Вилли.
Сетмеланотид
– комбинация ингибитора обратного захвата моноаминов и β-1-селективного блокатора для лечения синдрома Прадера – Вилли.
Tildacerfont и Crinecerfont
– лечение классических форм врожденной дисфункции коры надпочечников (ВДКН).
Основные достижения российской науки и индустрии за последние годы
В НМИЦ эндокринологии МЗ РФ (Москва) реализуются следующие направления:
- создание на базе регистра эндокринопатий аналитической системы прогнозирования развития осложнений и исходов течения эндокринных заболеваний с использованием наукоемких алгоритмов диагностики ИИ и анализа больших данных;
- разработка прогрессивных технологий для персонализированной диагностики эндокринных и онкоэндокринных заболеваний на основе разрабатываемой с помощью системы ИИ платформы, объединяющей клинико-катамнестические, геномные, метаболомные и иммуногистохимические параметры;
- разработка прогрессивных методов терапии эндокринных и онкоэндокринных патологий на основе современных радионуклеидных, генетических и клеточных технологий.
Достигнуты следующие результаты:
- Модуль ИАСРазработан модуль ИАС, который обеспечивает логистический контроль и прозрачность многостадийной обработки образцов. Повышение качества и бесперебойности лабораторных процессов.
Благодаря автоматизации приема, рутинной обработки и хранения данных высвобождаются человеческие ресурсы, упрощается коммуникация между сотрудниками, а также повышается оперативность и бесперебойность лабораторных процессов.
Программное обеспечение, разработанное в рамках данного проекта, позволяет поточно анализировать точечные замены и короткие вставки/делеции в герминальных генетических данных (панели генов, результаты полноэкзомного и полногеномного анализа). Доступны инструменты аннотации, фильтрации и предсказания патогенности, что облегчает решение научных и диагностических задач по поиску и приоритизации молекулярно-генетических вариантов с учетом фенотипа.
Готовится заявка «программы для электронных вычислительных машин (программы для ЭВМ)». - Логистика коллекции гистологических препаратовПереработана логистика коллекции гистологических препаратов для автоматизации внесения информации об образцах в единый регистр; добавлено штрихкодирование гистологических стекол 2D-штрих-кодом (datamatrix), содержащим информацию об уникальном идентификаторе исследования и номере гистологического стекла.
Коллекция изображений гистологических стекол продолжает пополняться новыми изображениями (40 000 образцов). Данный регистр интегрирован в прототип ИАС НЦМУ, где объединен с данными генетической диагностики путем стыковки по единым идентификаторам пациента из медицинской информационной системы.
Готовятся две заявки на «программы для электронных вычислительных машин (программы для ЭВМ)» и «база данных». - Разработка системы прогнозирования гипокальцемииРазработаны системы прогнозирования гипокальцемии на 1–3 сут после паратиреоидэктомии при ПГПТ и нарушения функции почек после паратттиреоидэктомии.
Поданы две заявки на патенты от 02.05.2023 (№ 2023111350 и 2023111351). - Разработка и первичная клиническая валидация нескольких тест-систем для выявления различных геновПроведена разработка и первичная клиническая валидация нескольких тест-систем (ПЦР):
- для выявления мутации в гене RET (медуллярный рак щитовидной железы (ЩЖ)),
- мутаций в гене CYP21A2 (врожденная дисфункция коры надпочечников),
- сиквенс-системы по анализу 378 генов для диагностики наследственных эндокринопатий,
- тест-системы для выявления генных транслокаций при раке ЩЖ;
- хромато-масс-спектрометрии уровня стероидов в сухих пятнах крови, набора для гормонального стероидного профилирования крови хромато-масс-спектрометрическим методом.
- Продолжается изучение факторов и механизмов повреждения β-клеток при СД2 в эксперименте (в качестве критерия – показатели НОМА-%В/ИИ).
- Изучение связи риска развития СД2 и этнического происхожденияИзучается связь риска развития СД2 и этнического происхождения. Исследование генетических маркеров СД2 в различных этнических группах населения, наряду с анализом влияния факторов внешней среды, позволит выявить этнические особенности развития заболевания, определить потенциальные терапевтические мишени для разработки лекарственных препаратов и разработать персонифицированный подход к профилактике и лечению данной патологии.
- Изучение полиморфизма генов, определяющих индивидуальные особенности метаболизма сахароснижающих препаратов.Продолжается изучение полиморфизма генов, определяющих индивидуальные особенности метаболизма сахароснижающих препаратов. На выборке из 450 пациентов определены частоты полиморфизмов генов: для метформина шесть вариантов для двух генов; сульфонилмочевины – четыре варианта для трех генов; агонистов рецепторов глюкагоноподобного пептида – 1-2 варианта одного гена.
- Проведено исследование поражений эндокринных органов у 169 пациентов, получивших лечение ингибиторами контрольных точек иммунного ответа (ИКТИО).
У 12 % выявлена дисфункция щитовидной железы. Даны рекомендации пациентам, получающим ИКТИО на фоне аутоиммунного гипотиреоза. Готовится заявка на «полезную модель». - Проведен анализ экспрессии М2 изоформы пируваткиназы РКМ – мишени DASA – ПЭТ-трейсеров у 45 пациентов с опухолями ЩЖ.Полученный результат позволяет дифферинцировать доброкачественные и злокачественные новообразования неинвазивно. Готовится заявка на «полезную модель».
- Выполнена дифференцировка СК с мономутацией в гене MEN 1 и без мутации (контроль) в клетки-прекурсоры паращитовидной железы, адипоциты и остеобласты.
Отредактирована мутация в последних двух с помощью CRISPR/Cas9 Prime editing (редактирование генома с целью создания новых методов лечения моногенных эндокринопатий). - Подана заявка на патент «Прогнозирование риска вторичной обтурации слезного протока при назначении радиойодтерапии по сцинтиграфическим изображениям».
- Изучены химерные серотипы ААВ-DJ и ААВ -DJ/8 с высокой трансдукцией клеток печени и надпочечников.
- Начаты исследования в области разработки прототипов лекарственных препаратов для лечения эндокринопатий и онкоэндокринных патологий с использованием клеточных технологий.
В НМИЦ им. В.А. Алмазова:
- Идентифицированы персонифицированные предикторы ответа на терапию антидиабетическими препаратами при сахарном диабете, в рамках экспериментального исследования продолжается изучение нейро- и остеотропных свойств сахароснижающих препаратов.
Получен патент «Способ экспериментального моделирования сахарного диабета 2-го типа в сочетании с менопаузой у самок крыс стока Wistar» № 2022133307/14(072552) (01.08.2023). - Проведение клэмп-исследований и исследований по иммуногенности способствовало выводу на рынок линейки отечественных биосимиляров аналогов инсулинов различной продолжительности действия.
- Разработаны математические модели и автоматизированные системы поддержки принятия решений для выбора тактики ведения больных с сердечно-сосудистой патологией и тиреотоксикозом различного генеза.
- Оптимизирована тактика ведения и профилактика неблагоприятных исходов у беременных с нарушениями функции щитовидной железы.
- Определены механизмы нарушений пубертатного развития и мужского гипогонадотропного гипогонадизма и разработаны новые подходы к лечению и профилактики, предложен новый лекарственный препарат на основе новых технологий для лечения мужского гипогонадизма.
- Разработан новый лекарственный препарат для лечения и профилактики сенильного и постменопаузального остеопороза.
- Определены долгосрочные эффекты дефицита витамина D, разработан персонифицированный подход к его профилактике и терапии.
Дополнительно в НЦМУ «Центр персонализированной медицины» НМИЦ им. В.А. Алмазова:
- Определены предикторы развития гестационного сахарного диабета, включая молекулярно-генетические, и оценено их влияние на плод.
- Разработана рекомендательная система (мобильное приложение) ДиаКомпаньон для пациенток с гестационным сахарным диабетом (ГСД) на диете.
Разработаны модели прогнозирования ППГО с применением методов машинного обучения. Встроенная в приложение модель прогнозирует какой будет уровень глюкозы в крови у женщины с ГСД после конкретного приема пищи, и, в случае прогнозирования высокого уровня, оценивает причины повышения и демонстрирует рекомендации по питанию для предотвращения гипергликемии. Получены три свидетельства о государственной регистрации программ для ЭВМ (№ 2022664462, 2022661781 и 2021681059). Готовится досье для подачи заявки на регистрацию медицинского изделия. - С использованием GWAS выявлены генетические маркеры динамики веса у пациентов с нарушениями углеводного обмена и ожирением, интегрированы в предсказательную модель.
- Уточнены молекулярно-генетические пути развития ожирения и реализации ответа на его медикаментозное и хирургическое лечение, выявлены молекулярно-генетические, гормональные и поведенческие предикторы эффективности терапии ожирения арГПП1 и редуксином, идентифицированы новые гормональные (чувствительность к грелину) и молекулярно-генетические (экспрессия CCl2, Hif1a, miR-142 в жировой ткани) маркеры метаболического здоровья.
- Разработаны новые методы диагностики нейроэндокринных опухолей гипофиза, поджелудочной железы, мозгового слоя надпочечников, околощитовидных желез, внедрены в клиническую практику ПЭТ/КТ с 11С-метионином и холином для диагностического поиска эктопированных и множественных аденом околощитовидных желез при ПГПТ.
- Определены предикторы ремиссии болезни Кушинга после транссфеноидальной аденомэктомии.
- Путем полноэкзомного секвенирования выявлены новые герминальные мутации, ответственные за развитие нейроэндокринных опухолей поджелудочной железы, надпочечников и околощитовидных желез.
- Создана база больных, перенесших COVID-19 средней и тяжелой степени, для динамического наблюдения за развитием нарушений со стороны эндокринной системы, проведена морфологическая оценка поджелудочной железы и щитовидной железы больных в острый период новой коронавирусной инфекции.
Достижение других центров:
Сотрудниками Института экспериментальной медицины (Санкт-Петербург) разработан метод выделения аутопробиотических энтерококков, применение которых при метаболическом синдроме было изучено совместно с сотрудниками НМИЦ им. В.А. Алмазова в рамках НЦМУ «Центр персонализированной медицины». В рандомизированном исследовании показаны преимущества использования аутопробиотических энтерококков при ожирении и нарушении толерантности к глюкозе в виде снижения гликемии натощак и уровня гликозилированного гемоглобина.
В Приволжском исследовательском медицинском университете (Нижний Новгород) выполняется разработка технологии инкапсуляции островков поджелудочной железы для компенсации абсолютных инсулин-дефицитных состояний. Разработана и сконструирована лабораторная установка по синтезу микрокапсул из альгинатного композита методом микрофлюидики (совместно с ИМХ РАН, Нижний Новгород). Разработана методика инкапсуляции островков Лангерганса поджелудочной железы. Проведена in vitro и in vivo оценка безопасности и стабильности альгинатной микрокапсулы, ее влияния на жизнеспособность и функциональную активность островков Лангерганса.
В НИИКЭЛ (филиал ИЦиГ СО РАН, Новосибирск) разработан метод персонализированного прогноза эпизодов гипогликемии и гипергликемии у больных сахарным диабетом 1-го типа на основе алгоритмов машинного обучения. Также разработана технология идентификации паттернов гликемии, основанная на кластерном анализе данных непрерывного мониторинга глюкозы, для персонификации инсулинотерапии у больных сахарным диабетом 1-го типа.
В ФИЦ «Институт цитологии и генетики сибирского отделения» Российской академии наук изучены молекулярно-генетические факторы риска развития нарушений углеводного и липидного обмена при моногенных формах заболеваний с помощью технологии секвенирования нового поколения. Определены редкие варианты в генах аполипопротеинов: APOB, APOE, APOC3 у пациентов с фенотипом СГХС и коронарным атеросклерозом. Разработана таргетная панель для диагностики моногенных форм сахарного диабета.
В ФМИЦ глазных болезней имени Геймгольца разработан доступный способ определения факторов риска развития диабетического макулярного отека (ДМО) за счет определения в СК содержания брадикинина (БК) и аденозин-превращающего фермента (АПФ) и их соотношения. На основе обучения нейронной сети ResNet50 создана система для распознавания признаков ДР по фундус-снимкам.
В ФМИЦ терапии и профилактической медицины в нозологических и популяционной выборках (n = 796) проводится апробация разработанной диагностической панели для оценки риска развития ожирения и сахарного диабета 2-го типа (СД2), включающей как гены, ответственные за развитие моногенных форм указанных заболеваний, так и шкалы генетического риска, разработанные на основе результатов исследований полногеномных ассоциаций. Создан промышленный образец тест-системы для определения носительства частых вариантов нуклеотидной последовательности, связанных с развитием аутосомно-рецессивных заболеваний: муковисцидоз, фенилкетонурия, нейросенсорная тугоухость и дефицит альфа-антитрипсина.
В ФГБУ «Центр стратегического планирования и управления медико-биологическими рисками здоровью» выполняется разработка и доклиническое исследование готовой лекарственной формы (ГЛФ) на основе вещества N-пентилрезорцинола, которое проявляет свойства видонеспецифического регулятора систем Quorum Sensing (QS) микробиоты кишечника, для модуляции эндокринной и метаболической функций жировой ткани.
В Курском государственном медицинском университете проведен анализ системной вовлеченности и совокупного вклада полиморфных вариантов генов ответа на неупакованные белки в молекулярные механизмы развития сахарного диабета 2-го типа и его прогрессирование, установлены ассоциации генотипов rs1882019-A/A HSP90B1 и rs1046495-T/C GFER с пониженным риском развития диабета, а минорных аллелей rs1043618-С HSPA1A и rs196914-C ERN1 – с повышенным, независимо от пола, возраста и ИМТ пациентов. У женщин протективным эффектом также обладал генотип rs899997-T/G SLCO1B1, а генотипы rs10778306-A/G HSP90B1, rs3095154-G/A HSPA1A и rs7838717-T/T HSF1 определяли повышенный риск. Полученные результаты будут использованы для создания диагностической панели, позволяющей выявить предрасположенность к заболеванию на доклинической стадии, а также для разработки программы персонализированного лечения пациентов с сахарным диабетом 2-го типа.
В Ростовском государственном медицинском университете выявлены гормонально-метаболические и иммунологические маркеры формирования нарушений пубертата у подростков с ожирением в условиях неблагоприятной экологической ситуации, оптимизирована их диагностика и терапия.
В Санкт-Петербургском государственном университете разработаны новые методы отслеживания нейропатии малых волокон и получены новые знания о патогенезе их поражения при постковидном синдроме.
В Сибирском государственном медицинском университете сформирована шкала факторов риска развития саркопении, при этом наиболее значимыми из них оказались: висцеральное ожирение, сахарный диабет, отсутствие приема витамина D в репродуктивном периоде, гиподинамия, неалкогольная жировая болезнь печени, гипотиреоз в настоящее время или в анамнезе. Выполняется разработка программы профилактики и реабилитации снижения мышечной массы для пациентов из группы риска.
Сотрудниками Российской медицинской академии непрерывного профессионального образования МЗ РФ установлено, что молекулярно-генетическое тестирование цитологических препаратов с заключением Bethesda IV с помощью отечественного молекулярно-генетического классификатора, разработанного в ИМКБ СО РАН (тест ТиройдИНФО), может с высокой точностью различать злокачественные и доброкачественные узлы щитовидной железы полученному при ТАБ узла щитовидной железы. Внедрение результатов исследования в клиническую практику позволит значительно уменьшить количество диагностических операций при узловых образованиях щитовидной железы.
В Северо-Западном государственном медицинском университете имени И.И. Мечникова МЗ РФ продолжаются успешные исследования по оценке метода газовой хромато-масс-спектрометрии (ГХ-МС ГХ-МС) в диагностике рецидива адренокортикального рака (АКР) и выявлении ранних признаков злокачественности опухолей у больных неклассической формой врожденной дисфункции коры надпочечников (НФ ВДКН) вследствие дефекта 21-гидроксилазы в сочетании с образованием коры надпочечников. Полученные результаты убедительно показывают, что ГХ-МС позволяет обнаружить признаки рецидива АКР после операции, а также ранние признаки малигнизации у больных НФ ВДКН вследствие дефекта 21-гидроксилазы в сочетании с образованиями коры надпочечников.
Ученые Федерального исследовательского центра комплексного изучения Арктики имени академика Н.П. Лаверова Уральского отделения РАН, изучая фотопериодическую зависимость физиологических эффектов дофамина на функциональную активность систем гипофиз – щитовидная железа и гипофиз – гонады у жителей арктических территорий, обнаружили различные соотношения уровней дофамина и содержания гормонов, белков и аутоантител системы гипофиз – щитовидная железа в крови в разные фотопериоды года у практически здоровых лиц, проживающих на территории АЗРФ. Результаты позволяли выявить значимые фотопериоды года для проведения диагностических и превентивных мер, направленных на предотвращение риска развития дезадаптационных реакций щитовидной железы. Продолжением исследования может служить выявление подобных закономерностей у женского населения, а также изучение возможного влияния дофамина на другие эндокринные звенья, в частности, систему гипофиз – гонады.
В Научно-исследовательском институте морфологии человека имени академика А.П. Авцына выполнено исследование морфогенеза и секреторной деятельности надпочечников в условиях пренатального и постнатального воздействия на организм эндокринных дисрапторов. Исследователями установлено, что воздействие низких доз ДДТ в пренатальном и постнатальном периодах онтогенеза приводит к нарушению постнатального морфогенеза и секреторной деятельности кортикостероцитов клубочковой, пучковой, сетчатой зон коркового вещества, а также хромаффинных клеток мозгового вещества. Результаты исследования не только расширяют существующие представления о механизмах действия эндокринных дисрапторов, но и устанавливают новый механизм – дисморфогенетический, что позволяет дополнить определение, данное эндокринным дисрапторам ВОЗ как экзогенных веществ, которые нарушают развитие эндокринных желез, а не только синтез, выделение, транспорт, метаболизм, связывание и выведение эндогенных гормонов, ответственных за гомеостаз, репродукцию и развитие.
Сотрудниками Научно-исследовательского института акушерства, гинекологии и репродуктологии имени Д.О. Отта разработаны диагностические критерии прогнозирования и преодоления репродуктивных потерь, что позволит создать алгоритм персонализированной диагностики причин репродуктивных потерь на разных сроках гестации и определить индивидуальный поэтапный подход к планированию и ведению супружеских пар.
Актуальность научного исследования обусловлена увеличением частоты репродуктивных потерь, что ведет к снижению показателей рождаемости в РФ, а широкое внедрение к практику стандартных общепринятых диагностических и лечебных подходов не улучшает ситуацию в целом. Целью НИР является разработка диагностических критериев прогнозирования и преодоления репродуктивных потерь. Определение диагностических критериев прогнозирования и преодоления репродуктивных потерь основывается на комплексном исследовании всех уровней организации организма как матери, так и плода. Так, изучение механизмов регуляции репродукции (от предгравидарной подготовки женщины и мужчины с целью выполнения репродуктивного потенциала, беременности с первых этапов имплантации и до родоразрешения), основывается на многоуровневом исследовании геномики, транскриптомики, протеомики и метаболомики. Данные уровни организации находятся в тесной взаимосвязи друг с другом, в них заложены все основные подходы к созданию принципиально новой медицины будущего – идентификация причин и определение нестандартных методов таргетной профилактики невынашивания беременности, что является приоритетным направлением научно-клинических исследований. Реализация планируемой фундаментальной темы позволит создать алгоритм персонализированной диагностики причин репродуктивных потерь на разных сроках гестации и определить индивидуальный поэтапный подход к планированию и ведению супружеских пар.
Актуальность научного исследования обусловлена увеличением частоты репродуктивных потерь, что ведет к снижению показателей рождаемости в РФ, а широкое внедрение к практику стандартных общепринятых диагностических и лечебных подходов не улучшает ситуацию в целом. Целью НИР является разработка диагностических критериев прогнозирования и преодоления репродуктивных потерь. Определение диагностических критериев прогнозирования и преодоления репродуктивных потерь основывается на комплексном исследовании всех уровней организации организма как матери, так и плода. Так, изучение механизмов регуляции репродукции (от предгравидарной подготовки женщины и мужчины с целью выполнения репродуктивного потенциала, беременности с первых этапов имплантации и до родоразрешения), основывается на многоуровневом исследовании геномики, транскриптомики, протеомики и метаболомики. Данные уровни организации находятся в тесной взаимосвязи друг с другом, в них заложены все основные подходы к созданию принципиально новой медицины будущего – идентификация причин и определение нестандартных методов таргетной профилактики невынашивания беременности, что является приоритетным направлением научно-клинических исследований. Реализация планируемой фундаментальной темы позволит создать алгоритм персонализированной диагностики причин репродуктивных потерь на разных сроках гестации и определить индивидуальный поэтапный подход к планированию и ведению супружеских пар.
Российские ученые активно изучают проблему мужского бесплодия. Так, исследования в Научном центре проблем здоровья семьи и репродукции человека были посвящены выявлению генетико-метаболических маркеров репродуктивных нарушений у мужчин для персонализированной коррекции и эффективной профилактики.
В Медико-генетическом научном центре имени академика Н.П. Бочкова были разработаны рекомендации по комплексному генетическому обследованию мужчин с бесплодием, а также сформирована панель из 133 генов, связанных с нарушением сперматогенеза, приводящих к мужскому бесплодию; показана эффективность комплексной диагностики с использованием геномных методов исследования.
Перечень создаваемых препаратов по направлению с указанием фазы разработки НМИЦ энокринологии:
- Клеточный препарат для лечения хронических ранРазработан прототип клеточного препарата – высокотехнологичного лекарственного препарата (соматоклеточного препарата) для лечения хронических ран, в том числе при синдроме диабетической стопы.
- Клеточный препарат состоит из мезенхимальных стромальных клеток костного мозга, является по сути суспензией живых клеток для заживления ран, который нарабатывается в асептических условиях путем культивирования с целью наработки терапевтических доз.
- Прототип проверен в доклинических и пилотных клинических исследованиях и продемонстрировал самую высокую в мире эффективность по скорости регенерации кожи при труднозаживающих диабетических язвах: язвы площадью от 4 до 40 см2 полностью эпителизировались, отсутствовали рецидивы в месте лечения после трех лет наблюдения.
- Клеточный препарат для восполнения объемных дефектов костной ткани при ее поврежденияхРазработан прототип клеточного препарата – тканеинженерной костной ткани для восполнения объемных дефектов костной ткани при ее различных повреждениях (в том числе для лечения стопы Шарко).
- Тканеинженерная костная ткань представляет собой иммобилизованные преддифференцированные живые клетки на биосовместимом материале (зарегистрированном медицинском изделии).
- Проведена доклиническая оценка применения тканеинженерной костной ткани на моделях повреждения костей у крыс, кроликов и собак.
- Прототип клеточного препарата позволяет ускорить регенерацию костной ткани в 2-2,5 раза, а также обеспечить регенерацию в практически невозможных для восстановления случаях (аваскулярные некрозы костей в единичных клинических случаях).
Предложения по перспективному планированию
Переход от унифицированной к ПМ, даже в такой быстро развивающейся области как эндокринология, займет немало времени:
Переход от унифицированной к ПМ, даже в такой быстро развивающейся области как эндокринология, займет немало времени:
- требуется усовершенствование законодательной базы, особенно в части клеточных и биомедицинских технологий,
- решение этических вопросов, в том числе по защите персональной генетической информации,
- подготовка высококвалифицированных кадров,
- наличие необходимого оборудования и расходных материалов,
- пересмотр клинических рекомендаций и протоколов лечения, реструктуризация фармацевтических производств,
- просвещение населения о возможностях нового направления.
В настоящее время ПМ стоит на пороге значительного расширения возможностей. Геномные и постгеномные технологии входят в повседневную практику. Основным препятствием в развитии персонализированной медицины наряду с пока еще высокой стоимостью необходимых исследований считают недостаточную подготовленность специалистов, большой разрыв между предоставляемыми ею новыми ценными диагностическими и терапевтическими возможностями и способностью практических врачей оценить их и применить на практике. Перечисленные факторы указывают на необходимость развития этой перспективной области в виде научных исследований по социально значимым и орфанным заболеваниям. В современных условиях интенсивного развития персонализированных биомедицинских технологий специалистам важно понимать, в чем состоят принципиальные особенности персонализированной медицины по сравнению с подходами недавнего прошлого. Медицина с самого начала стремилась к персонализации, но до расшифровки генома человека это было в большей степени мечтой, чем реальностью. Дальнейшая персонализация современной медицины, как представляется, будет развиваться по следующим основным направлениям:
- Разделение традиционных нозологических форм на молекулярные подгруппы для дифференциального подхода к лечению.
- Основанный на геномике предсказательный подход, позволяющий предупредить развитие заболевания вместо диагностики уже развернутой патологии. Геномный подход может быть совмещен с мониторингом начала заболевания посредством анализа про-теома и метаболома. Подход был проиллюстрирован мониторингом этих показателей у одного из исследователей в течение нескольких месяцев, что позволило вкупе с информацией о его геноме обнаружить у него преддиабет и скорректировать его развитие изменением образа жизни.
- Контроль эффективности лечения заболеваний и снижения степени выраженности побочных эффектов этого лечения посредством терапевтического лекарственного мониторинга.
- Организация криобанков биоматериала, связанного с социально-значимыми заболеваниями. Биобанки необходимы при разработке и валидации персонализированных подходов к диагностике заболевания. Депонирование образцов от пациента в течение всей его жизни обеспечивает персонализацию мониторинга его индивидуальных показателей; в качестве контроля используется биоматериал от этого же пациента, взятый ранее.
- «Цифровая» диагностика социально-значимых заболеваний, основанная на поиске белковых биомаркеров по принципу их присутствия (1) или отсутствия (0) в образцах больных или контрольных субъектов. Задача решается за счет обнаружения в доступном биоматериале от пациентов появления или исчезновения модифицированных ключевых белков протеома и за счет усиления чувствительности аналитических методов в протеомике.
- Персонализация клеточных технологий, в том числе применение собственных плюрипотентных и перепро-граммированных клеток для регенеративной медицины.
Неврология
Основные направления
мировых исследований
мировых исследований
- Персонализированные виртуальные модели мозга (The Virtual Brain) – парадигма «цифровых близнецов» – как система поддержки принятия врачебных решений и прецизионное таргетирование (в частности, в хирургическом лечении эпилепсии)
- Прецизионная медицина при инсульте – персонализация прогноза с помощью методикискусственного интеллекта
- Персонализация терапии и прогнозирования течения рассеянного склероза на основании клинических, нейровизуализационных, нейрофизиологических и лабораторных биомаркеров
- Индивидуализация выбора вида эндоваскулярного вмешательства и отбора пациентов для механической тромбэктомии при ишемическом инсульте с помощью инструментов искусственного интеллекта
- Использование индуцированных плюрипотентных стволовых клеток (иПСК) в персонализации итаргетировании терапии нейродегенеративных, цереброваскулярных и травматических поражений центральнойнервной системы: выявление респондеров с помощью технологии «орган-на-чипе»; 3D-моделирование на основеиПСК; «симуляция» заболевания с иПСК
- Программно-ассистированные технологии нейровизуализации в персонализации лечения и диагностики неврологической патологии (в частности, эпилепсии, рассеянного склероза)
- Фундаментальные исследования в области нейрогеномики, нейропротеомики, нейрометаболики, нейрофармакологии при различных заболеваниях нервной системы
Основные достижения ПМ и примеры успешной реализации в мире
1
Цереброваскулярная патология
В аспекте цереброваскулярной патологии большие успехи получены в области персонализированной диагностики феномена аспиринорезистентности, который признается важным фактором неэффективности лечения и профилактики ишемических нарушений мозгового кровообращения (НМК).
- В начале нынешнего века был апробирован и запатентован способ индивидуального подбора антиагрегантного препарата на основании тест-системы с определением АДФ-индуцированной агрегации тромбоцитов.
- В дальнейшем, в том числе в работах Научного центра неврологии, были продемонстрированы новые способы индивидуализации назначения антиагрегантной терапии пациентам с сосудистыми заболеваниями нервной системы, основанные на молекулярно-генетическом, фармакокинетическом и гемостазиологическом подходах.
Развитие методик искусственного интеллекта и машинного обучения позволяют внедрять в клиническую практику модели для персонализированной оценки прогноза у пациентов, в частности с острыми цереброваскулярными заболеваниями.
- Так, модель ASTRAL, основанная на рутинных клинико-лабораторных показателях (возраст, тяжесть инсульта, время до поступления, уровень гликемии, уровень бодрствования, объем дефекта полей зрения), продемонстрировала высокую предиктивную значимость в отношении прогноза восстановления неврологического дефицита после ишемического инсульта.
- Использование наиболее современных модальностей нейровизуализации (в частности, функциональной МРТ) позволяет с высокой долей вероятности прогнозировать моторный дефицит после инсульта, а также развитие поведенческих нарушений.
Важным звеном персонализированной неврологии в аспекте ангионеврологии является предиктивность – возможность на основании определенного пула биомаркеров предсказать (оценить риск) развития инвалидизирующего НМК у (относительно) здорового человека.
Одним из таких факторов риска являются молекулярно-генетические альтерации в генах-кандидатах, ассоциированных с сосудистыми заболеваниями (атеросклероз, гипертония, кардиальная патология).
Одним из таких факторов риска являются молекулярно-генетические альтерации в генах-кандидатах, ассоциированных с сосудистыми заболеваниями (атеросклероз, гипертония, кардиальная патология).
- В совместной многолетней работе Научного центра неврологии с Центральным НИИ эпидемиологии была исследована мультипликативная модель риска развития ишемического инсульта на основании почти полусотни однонуклеотидных полиморфизмов.
- Одним из важных результатов этой работы стала не только демонстрация вклада генетики в общий риск инсульта, но и возможность с помощью данной методики проанализировать возможность развития конкретного подтипа ишемического инсульта (например, атеротромботического, кардиоэмболического и т.д.).
Нельзя не упомянуть появившиеся недавно возможности таргетной коррекции ряда сосудистых заболеваний, тесно связанных с цереброваскулярной патологией.
Одним из ведущих факторов риска последних является церебральный атеросклероз – хроническое заболевание, в патогенезе которого важную роль отводят воспалению и нарушениям липидного обмена.
Одним из ведущих факторов риска последних является церебральный атеросклероз – хроническое заболевание, в патогенезе которого важную роль отводят воспалению и нарушениям липидного обмена.
- В 2022 г. было опубликовано исследование малой интерферирующей РНК, таргетно снижающей уровни липопротеина(а) – биомаркера, который значимо ассоциирован с нестабильностью каротидной атеросклеротической бляшки и риском инсульта.
- В пилотном проекте по исследованию таких маркеров церебрального атеросклероза как микроРНК было показано, что снижение экспрессии miR-126 является потенциальным биомаркером выявления значимого каротидного стеноза с очень большой чувствительностью и специфичностью.
- антитромботической терапии;
- липидснижающей терапии;
- ангиореконструктивного вмешательства.
2
Эпилепсия
Одним из наиболее успешных в плане персонализации является диагностика и терапия такой важнейшей патологии, как эпилепсии.
Персонализация в лечении эпилепсии затронула не только медикаментозный, но и хирургический аспект.
- Использование биомаркеров и методик для индивидуализации прогноза и лечения пациентов с эпилепсией на сегодняшний день доступно практически на всех этапах лечебно-диагностического процесса.
- Успешно применяющиеся молекулярно-генетические методики выявления наследственных форм эпилепсии позволяют персонализировать выбор противосудорожной терапии на основании мутации в конкретном гене.
- Уже внедрен в клиническую практику метод терапевтического лекарственного мониторинга, который позволяет устанавливать индивидуальные терапевтические концентрации противоэпилептических препаратов (например, ламотриджина) в плазме крови, «визуализировать» их фармакокинетику и, при необходимости, персонализировать дозировку и (или) комбинацию лекарственных агентов.
Персонализация в лечении эпилепсии затронула не только медикаментозный, но и хирургический аспект.
- Возможности нейровизуализации позволяют с помощью методики диффузионно-тензорной МРТ в режиме трактографии на этапе до операции оценить анатомию волокон белого вещества, реализующих речевую функцию, затем персонализированно определить и наметить объем резекции и траекторию доступа, оптимальных для сохранения речевых трактов.
- Указанная технология позволяет значительно улучшить функциональные исходы операций при резистентных формах эпилепсии.
- В сложных случаях (дети, МР-негативные или мультифокальные варианты) гибридное исследование ПЭТ/МРТ позволяет локализовать эпилептогенную зону.
3
Демиелинизирующие заболевания
Ярким примером персонализированной диагностики может являться открытие благодаря биомаркерным исследованиям новых форм демиелинизирующих заболеваний, требующих совершенно иных терапевтических подходов.
Открытие и изучение новых биомаркеров – аквапорина 4 (AQP4), антител к миелин-олигодендроцитарному гликопротеину (MOG), а затем внедрение в клиническую практику методик их определения (непрямая иммунофлуоресценция с клеточной презентацией антигена), позволило выделить ранее неописанные формы тяжелых иммуннопосредованных демиелинизирующих заболеваний:
Открытие и изучение новых биомаркеров – аквапорина 4 (AQP4), антител к миелин-олигодендроцитарному гликопротеину (MOG), а затем внедрение в клиническую практику методик их определения (непрямая иммунофлуоресценция с клеточной презентацией антигена), позволило выделить ранее неописанные формы тяжелых иммуннопосредованных демиелинизирующих заболеваний:
- спектра оптикомиелита (NMO-IgG+),
- GFAP-астроцитопатия, MOG-ассоциированные энцефаломиелиты (MOG-IgG+), требующих совершенно других персонализированных терапевтических подходов.
4
Нейродегенеративные заболевания
Интенсификация исследований в области нейрогеномики привела к своеобразному «ренессансу» в сфере диагностики и лечения нейродегенеративных заболеваний. Так, благодаря новой методике массового параллельного секвенирования кратно увеличилось выявление генетических форм заболеваний, а инновационные подходы к генной терапии позволили осуществлять персонифицированное лечение ранее фатальных болезней.
Серьезные изменения коснулись и биомаркеров ранней (иногда даже доклинической) диагностики ряда нейродегенеративных заболеваний, причем важным является в том числе и очередность выявления маркерных альтераций. -
- Наиболее исследованной в этом плане остается болезнь Альцгеймера, где ранним биомаркером заболевания считается изменение содержания бета-амилоида-42 в ликворе, с последующим присоединением маркеров тау-патологии, изменением на МРТ и затем постепенным когнитивным снижением по данным нейропсихологического тестирований.
- Но персонализация доступна не только для диагностики болезни Альцгеймера, но и для выбора таргетной терапии, в том числе с использованием человеческих индуцированных плюрипотентных стволовых клеток, что потенциально ускорит выделение пациентов-респондеров.
Современные методики нейровизуализации, в частности функциональная МРТ покоя и воксель-ориентированная МР-морфометрия, активно исследуются в отношении дифференциальной диагностики болезни Паркинсона.
- Так, корреляции между особенностями функциональных пластических перестроек коры головного мозга и особенностями течения болезни Паркинсона и (или) реакцией на проводимую терапию позволяют использовать указанные высокоспециализированные нейровизуализационные последовательности для персонализации ранней диагностики и оценки эффекта от лечения.
- Последовательная интеграция подобных данных с мультимодальными исследованиями геномики, транскриптомики, метаболомики и протеомики в сочетании с доступными клиническими тестами может обеспечить всестороннее понимание механизмов развития болезни Паркинсона и медикаментозной терапии на системном уровне.
Наиболее известным успешным примером генной терапии в неврологии являются предложенные препараты для лечения спинальной мышечной атрофии на основе антисмысловых олигонуклеотидов и на основе аденоассоциированного вируса.
На сегодняшний день также предложена генная терапия для клинического применения при боковом амитрофическом склерозе, миодистрофии Дюшенна.
На сегодняшний день также предложена генная терапия для клинического применения при боковом амитрофическом склерозе, миодистрофии Дюшенна.
- При этом терапия миодистрофии Дюшенна максимально персонализирована и зависит от конкретной мутации в гене дистрофина. Предложена целая линейка препаратов для лечения таких пациентов от векторной доставки микродистрофина до различных вариантов «пропуска экзонов».
Персонализированная терапия предлагается не только для моногенных заболеваний, но и для отдельных генетических форм, рассматриваемых в рамках мультифакторных заболеваний.
- В этом ключе развивается таргетная, персонализированная терапия двух генетических форм болезни Паркинсона: GBA1- и LRRK2-ассоциированной.Для обеих форм предложены препараты, проходящие клинические исследования в три фазы.
- Для GBA1-паркинсонизма предлагается фармакологический шаперон – амброксол, который способствует правильному фолдингу белка глюкоцереброзидазы.
- Для LRRK2-паркинсонизма – ингибитор киназного домена, с которым связывают патологическое действие белка.
Выявление целевой группы пациентов для максимально персонализированной терапии – это один из аспектов успешного лечения нейродегенеративной патологии.
Еще одним аспектом является максимально раннее начало данной терапии – на продромальных, а в идеале – на преклинических стадиях.
Манифестация заболевания – это условно каскадный «срыв» этих компенсаторных механизмов, переход от разнообразных начальных процессов к относительно единообразным развернутым стадиям.
Еще одним аспектом является максимально раннее начало данной терапии – на продромальных, а в идеале – на преклинических стадиях.
- Развернутые стадии заболеваний как результат необратимых нейродегенеративных изменений не являются тем временным отрезком, когда можно предложить эффективную «восстановительную» терапию, по крайней мере, в самом ближайшем будущем.
- Тогда как преклинические и продромальные стадии рассматриваются в качестве потенциального терапевтического окна для проведения нейропротекторной и эффективной нозомодифицирующей терапии.
Манифестация заболевания – это условно каскадный «срыв» этих компенсаторных механизмов, переход от разнообразных начальных процессов к относительно единообразным развернутым стадиям.
- В связи с этим скрининговый поиск лиц на продромальных/преклинических стадиях заболевания, их подразделение на более однородные группы и проведение у них таргетной персонализированной протекторной терапии являются ключом к вторичной профилактике распространенных нейродегенеративных заболеваний.
- Для идентификации лиц на продромальных/преклинических стадиях разрабатываются алгоритмы для количественного расчета индивидуального риска развития того или иного мультифакторного заболевания.
Танашян М.М., Раскуражев А.А., Корнилова A.А. и др. Мониторинг терапии ацетилсалициловой кислотой у пациентов с цереброваскулярной патологией // Рациональная фармакотерапия в кардиологии. 2021;17(4):537-543. DOI: 10.20996/1819-6446-2021-08-15
Танашян М.М., Раскуражев А.А., Корнилова А.А. Цереброваскулярные заболевания и персонифицированная профилактика // Профилактическая медицина. 2021;24(2):76‑81. DOI: 10.17116/profmed20212402176
Танашян М.М., Раскуражев А.А., Корнилова А.А. Цереброваскулярные заболевания и персонифицированная профилактика // Профилактическая медицина. 2021;24(2):76‑81. DOI: 10.17116/profmed20212402176
Liu C., Zhu M., Wang Y. Human Serum Anti-aquaporin-4 Immunoglobulin G Detection by Cell-based Assay // J Vis Exp. 2019;(146):10.3791/59014. DOI: 10.3791/59014
Щепарева М.Е., Кочергин И.А., Толпеева О.А., и др. Диагностическое значение антител к миелин-олигодендроцитарному гликопротеину при демиелинизирующих заболеваниях центральной нервной системы // Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(2‑2):18‑23. DOI: 10.17116/jnevro20191192218
Щепарева М.Е., Кочергин И.А., Толпеева О.А., и др. Диагностическое значение антител к миелин-олигодендроцитарному гликопротеину при демиелинизирующих заболеваниях центральной нервной системы // Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(2‑2):18‑23. DOI: 10.17116/jnevro20191192218
Основные достижения российской науки и индустрии за последние годы
Разделение доступных отчетов по фундаментальным и прикладным исследованиям, которые касаются в той или иной степени персонализации в неврологии, в значительной степени условно, как и ориентировочное количество работ по соответствующим тематикам.
Разделение доступных отчетов по фундаментальным и прикладным исследованиям, которые касаются в той или иной степени персонализации в неврологии, в значительной степени условно, как и ориентировочное количество работ по соответствующим тематикам.
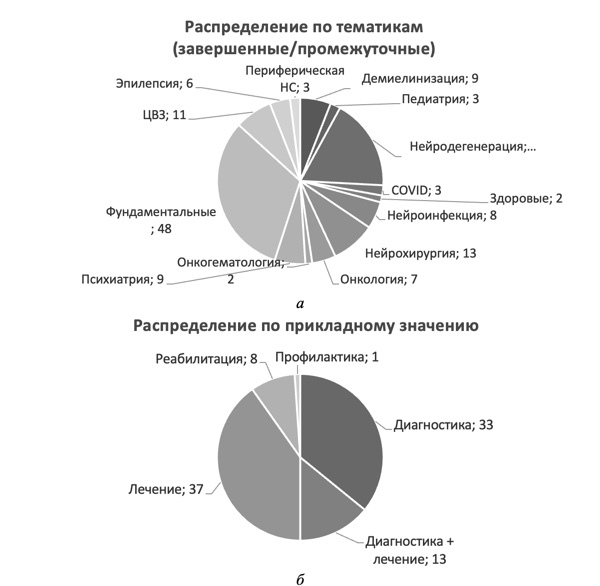
Рис. Распределение ключевых исследований по тематикам (а) и прикладному значению (б)
За период 2021–2022 гг. в рамках фундаментальных исследований проведено 48 работ.
В НМИЦ им. В.А. Алмазова (Санкт-Петербург) проведен ряд исследований, из которых можно выделить следующие:
- Исследование, направленное на разработку персонифицированного подхода к эндоваскулярному лечению церебральных артериовенозных мальформаций на основе изучения молекулярных механизмов ангиогенеза.В настоящее время выявлен прогностический биомаркер прогнозирования формирования de novo в церебральных артериовенозных мальформациях у больных с аневризмами, сочетающимися с артериовенозными мальформациями, при многоэтапной эндоваскулярной эмболизации.
Способ прогнозирования формирования аневризм de novo в церебральных артериовенозных мальформациях у больных с аневризмами, сочетающимися с артериовенозными мальформациями при многоэтапной эндоваскулярной эмболизации - Разработка новых молекулярно-биологических маркеров патогенеза центральной нервной системы и их коррекции на основе экспериментальных моделей зебраданио (zebrafish)Доказано, что модель травматического мозга вызывает гиполокомоцию и нарушения памяти у данио-рерио, а хронический стресс вызывает выраженные нарушения баланса нейровоспалительных клеток мозга
- Исследование морфометрических параметров мозга и коннектома у пациентов с прогрессирующим рассеянным склерозом для оценки нейропластичностиВ этой когорте пациентов выявлено снижение объема белого вещества головного мозга, мозжечка, с компенсаторным увеличением объема ликворных пространств – наиболее выраженные изменения отмечаются в функциональной коннективности медиальной префронтальной коры.
Достижение других центров:
В НМИЦ реабилитологии и курортологии (Москва) исследовали применение высокоинтенсивной импульсной магнитной стимуляции (ВИМТ) у онкологических пациентов с дистальной полинейропатией, индуцированной приемом цитостатических препаратов.
Полученные результаты позволяют сделать предварительные выводы о том, что применение ВИМТ предотвращает дальнейшее прогрессирование аксонально-сенсорных поражений в периневральных структурах дистальных зон, потенцируя в них обратное развитие.
Полученные результаты позволяют сделать предварительные выводы о том, что применение ВИМТ предотвращает дальнейшее прогрессирование аксонально-сенсорных поражений в периневральных структурах дистальных зон, потенцируя в них обратное развитие.
В ФГБУ «Федеральный центр мозга и нейротехнологий» (Москва) проводилась работа по разработке аннотированной базы данных индуцированных плюрипотентных стволовых клеток пациентов для исследования молекулярных основ неврологических заболеваний. На текущий момент сформирована коллекция клеточных культур, собраны данные по транскриптомике, протеомике и метаболомике клеток разных типов, разработана база данных с веб-интерфейсом.
В Приволжском исследовательском медицинском университете (Нижний Новгород) разрабатываются новые молекулярно-клеточные подходы к прогнозированию и коррекции нейросетевой патологии мозга и когнитивных функций, ассоциированных с нейровоспалением. Найдены новые мишени и методы для стратегии терапии, выявлены объективные критерии нарушения когнитивных функций при регистрации когнитивных вызванных потенциалов.
В Казанском государственном медицинском университете (Казань) изучалось влияние обогащенного генетическим материалом аутологичного лейкоконцентрата на пластичность спинного мозга, спинномозговых нервов и скелетных мышц мини-свиней с контузионной травмой. На данном этапе выполнены экспериментальные исследования по созданию и наработке рекомбинантных репликативно-дефектных аденовирусов человека пятого серотипа (Ad5) с модифицированным фибером (Ad5/35F), приготовлению аутологичного лейкоконцентрата, обогащенного генетическим материалом, и анализу экспрессии трансгенов и его аутоинфузии.
В Якутском государственном научном центре комплексных медицинских проблем (Якутск) изучались эпидемиологические, медико-генетические аспекты и разрабатывались методы трансляционой и персонализированной медицины при нейродегенеративных заболеваниях. В данном исследовании впервые в условиях реализации крупномасштабных федеральных программ охраны здоровья населения проводится комплексное изучение и лечение в круглосуточном стационаре пациентов с нейродегенеративными заболеваниями в Республике Саха (Якутия) с разработкой персонализированного подхода и трансляцией полученных результатов в практическую медицину.
В ФГБНУ «Научный центр проблем здоровья семьи и репродукции человека» (Иркутск) в рамках проекта «Геномные и постгеномные технологии оптимизации фармакотерапии как основа персонализированной медицины» проводилось определение вариативности метаболизма лекарственных препаратов (в частности, антикоагулянтов – варфарин, дабигатран) у носителей разных генетических профилей в разные периоды онтогенеза. Также проводился поиск и идентификация полиморфных локусов генов – метаболизаторов ксенобиотиков, их частотных различий и клинико-фармакологической значимости у представителей монголоидной и европеоидной рас
В Институте физиологии им. И.П. Павлова (Санкт-Петербург) был создан Научный центр мирового уровня «Интегративная физиология – медицине, высокотехнологичному здравоохранению и технологиям стрессоустойчивости». Из наиболее важных результатов за отчетный период можно выделить: определение роли социальной изоляции (в том числе во время COVID-19), которая повлияла на психическое здоровье и привела к усугублению хронических заболеваний пациентов; проведены исследования электрической стимуляции спинного мозга для лечения язвенной болезни желудка; выявлены гендерные и возрастные различия при применении транскраниальной электростимуляции пациентов сурдологического профиля; получены новые данные о корреляции когнитивных и аудиологических показателей.
По клиническим направлениям неврологии 11 исследований было посвящено цереброваскулярной патологии и последствиям перенесенных НМК.
Среди них можно выделить несколько работ, проведенных в Федеральном центре мозга и нейротехнологий (Москва):
- Разработка методов исследования редокс-метаболизма органоидов нервной ткани при ишемии-реперфузии.
В результате впервые получены индуцированные плюрипотентные клетки человека, экспрессирующие биосенсоры рН, пероксида водорода. В будущем при разработке системы скрининга лекарственных кандидатов, действующих на коррекцию метаболических и сигнальных процессов при ишемическом повреждении мозга могут появиться новые способы лечения ишемии мозга. - Изучение распределения мезенхимальных стволовых клеток (МСК) в веществе головного мозга на модели экспериментального инфаркта мозга.Оптимизированы протоколы операции по моделированию инфаркта у животных, протоколы трансплантации МСК животным, отработаны МР-протоколы для визуализации меченых микрочастицами оксида железа МСК. Полученные результаты в будущем могут способствовать разработке клеточной терапии ишемического инсульта
- Разработка омиксных технологий для исследования ишемических повреждений мозгаНа текущий момент собраны образцы клеток и тканей мозга различного происхождения, разработаны и применены методики метаболомного и протеомного анализа тканей мозга, методы высокоэффективной жидкостной хроматогрофии и масс-спектрометрии.
В Научном центре неврологии (Москва) определены маркеры аспиринорезистентности на основании мониторинга содержания салицилатов в крови у пациентов с различными формами сосудистой патологии мозга
В НИИ фундаментальной и клинической иммунологии (Новосибирск) проводилась разработка клеточных технологий различной тканевой и целевой направленности, средств и способов модуляции процессов пролиферации, дифференцирования и элиминации клеток с целью восстановления утраченных функций органов. В качестве нового метода лечения/реабилитации больных с органическими поражениями ЦНС разработана технология локорегиональной цитокинотерапии на основе использования биоактивных факторов, продуцируемых макрофагами 2-го типа
В исследовании НМИЦ им. В.А. Алмазова (Санкт-Петербург) проводилось изучение нейропластичности при цереброваскулярных заболеваниях путем использования новых биомаркеров ишемического повреждения мозга и исследования коннектома для выявления предикторов, разработки новых профилактических и терапевтических стратегий. Выявлено значимо лучшее восстановление неврологических функций на фоне гиперкапнически-гипоксических дыхательных тренировок
В Институте физиологии им. И.П. Павлова (Санкт-Петербург) на базе Научного центра мирового уровня «Интегративная физиология – медицине, высокотехнологичному здравоохранению и технологиям стрессоустойчивости» разработана неинвазивная технология спинальной нейромодуляции для регуляции двигательных функций у постинсультных пациентов.
Среди шести исследований, посвященных эпилептологии, можно выделить работу НМИЦ им. В.А. Алмазова (Санкт-Петербург), в которой проводилось исследование гистологических и иммуногистохимических изменений в эпилептическом очаге головного мозга – получены морфометрические данные о клеточном нейроглиальном дисбалансе и выявлены особенности экспрессии виментина в ядрах гиппокампа и зубчатой извилине при очаговой фармакорезистентной эпилепсии. В данном исследовании впервые показана роль виментина в генезе склероза гиппокампа. Методами машинного обучения был проанализирован риск развития эпилепсии у пациентов с цереброваскулярными и онкогеметологическими заболеваниями, а также сформированы диагностические модели для персонализации тактики ведения таких пациентов
В Медицинском институте РУДН (Москва) активно разрабатывается тема персонификации фармакотерапии у пациентов крайних возрастных групп (новорожденные, в том числе глубоко недоношенные, а также пациенты пожилого и старческого возраста). Продемонстрировано, что подход простой экстраполяции результатов клинических исследований на подобные когорты пациентов в большинстве случаев не позволяет проводить эффективную и безопасную фармакотерапию. Особую значимость приобретают исследования, посвященные разработке популяционных фармакокинетических моделей различных препаратов, в том числе антиконвульсантов, антибиотиков для лечения инфекций центральной нервной системы, на основе данных терапевтического лекарственного мониторинга и индивидуализации дозирования лекарственных препаратов с учетом гестационного и постнатального возраста
В Институте физиологии им. И.П. Павлова (Санкт-Петербург) был создан Научный центр мирового уровня «Интегративная физиология – медицине, высокотехнологичному здравоохранению и технологиям стрессоустойчивости». Из наиболее важных результатов за отчетный период можно выделить: определение роли социальной изоляции (в том числе во время COVID-19), которая повлияла на психическое здоровье и привела к усугублению хронических заболеваний пациентов; проведены исследования электрической стимуляции спинного мозга для лечения язвенной болезни желудка; выявлены гендерные и возрастные различия при применении транскраниальной электростимуляции пациентов сурдологического профиля; получены новые данные о корреляции когнитивных и аудиологических показателей.
Среди 13 исследований, посвященных нейрохирургии, можно выделить следующие:
- На базе НМИЦ им. В.А. Алмазова (Санкт-Петербург) были разработаны и внедрены минимально-инвазивные персонифицированные технологии (индивидуальные межтеловые имплантаты, индивидуальные 3D-матрицы, суперселективная химиоэмболизация опухолей позвонков) для лечения пациентов с патологией позвоночника (дегенеративно-дистрофические заболевания, опухоли позвоночника); созданы дифференцированные алгоритмы хирургического лечения пациентов с нейрогенными опухолями спинного мозга и нервных сплетений, основанные на методах нейрофизиологического мониторинга и интраоперационной ассистенции.
- В Первом Санкт-Петербургском государственном медицинском университете им. И.П. Павлова (Санкт-Петербург) проведено исследование по применению технологий 3D-печати для навигации при операциях на позвоночнике; разработан алгоритм изготовления навигационных матриц, их оптимальный дизайн
- В Приволжском исследовательском медицинском университете (Нижний Новгород) проводится разработка технологий, повышающих эффективность декомпрессивно-стабилизирующих вмешательств с применением транспедикулярной фиксации и костной пластики у пациентов с дегенеративной патологией и травматическими повреждениями позвоночника. В настоящее время разработана дифференцированная тактика с применением различных видов декомпрессии, спондилодеза и рационального использования имплантатов, уточнены показания к применению непрямой декомпрессии корешков спинного мозга при дегенеративных заболеваниях позвоночника, снижена травматичность оперативных вмешательств и частота имплантатзависимых осложнений.
В рамках исследований, посвященных нейродегенерации, проведено 27 работ, из которых можно выделить следующие:
- В ФГБУН «Институт мозга человека им. Н.П. Бехтеревой РАН» (Санкт-Петербург)исследовались интегративные процессы головного мозга человека для создания новых конкурентноспособных методов и технологий диагностики и лечения заболеваний головного мозга:
- разработка роботизированного манипулятора для стереотаксических операций на головном мозге для прицельной точности;
- создание новой технологии использования оптической безрамной и оптической нейронавигации; изучение роли микроРНК в мониторинге эволюционирования глиальных церебральных опухолей на различных этапах комплексного лечения;
- разработка сенсорных обучающих программ на основе компьютеризированных когнитивных тренингов для нейрореабилитации отдельных категорий пациентов с нарушениями познавательных функций и эмоционально-волевыми расстройствами;
- исследования, направленные на повышение эффективности диагностики глиом взрослого и детского типов на дооперационном этапе при помощи совмещенной позитронно-эмиссионной и компьютерной томографии (ПЭТ/КТ) с [11С]-метионином.
- В Научном центре неврологии (Москва)оценивалась эффективность и механизмы нейропротекторного действия новых соединений и наноструктурных комплексов на основе антиоксидантов в условиях моделирования патологий ЦНС, сопровождающихся развитием окислительного стресса.
- Впервые при моделировании ишемии головного мозга на нейрональной культуре в условиях глюкозо-кислородной депривации и NMDA-индуцированной экзайтотоксичности выявлена нейропротекторная активность новых соединений салицил-карнозина и пирролил-карнозина.
- Впервые в клинико-биохимических исследованиях дана диагностическая и прогностическая оценка значимости продуктов окислительного метаболизма липидов, белков и ДНК, регистрируемых в крови пациентов с болезнь Паркинсона; анализ профилей оксилипинов позволит в дальнейшем прогнозировать течение заболевания и вовлечение различных патологических каскадов в патогенез болезни Вильсона – Коновалова, что особенно важно с точки зрения подходов к ПМ.
- В ФИЦ «Пущинский научный центр биологических исследований Российской Академии наук» (Пущино)проводилось исследование механизмов нейрогенеза во взрослом мозге и коррекция их нарушений для разработки эффективной терапии болезни Альцгеймера.
- Исследовались клеточные механизмы действия мультипотентных мезенхимальных стромальных клеток (ММСК), стресс-белка YB1, а также химических нейрогенных факторов в условиях развитого нейродегенеративного процесса в культуре гиппокампа трансгенных мышей и блокады АСЕ2 рецептора – клеточной модели COVID-19.
- Рассмотрена возможность перепрограммирования эндогенных астроцитов в нейроны путем введения различных нейрогенных факторов для восстановления функций мозга, которые во многом зависят от количественного баланса нейроны/астроглия.
- В Институте биологии развития им. Н.К. Кольцова РАН (Москва)проводилась экспериментальная разработка способа определения скрытой функциональной недостаточности нигростриарной системы мозга при болезни Паркинсона (БП) с помощью эндогенного ингибитора тирозингидроксилазы – монойодтирозина (МИТ).
Полученные данные свидетельствуют об эффективности и безопасности разработанного провокационного теста для ранней диагностики нейродегенерации при БП, что может не только лечь в основу новых способов ранней диагностики БП, но и открыть путь к созданию новых лекарств, направленных на превентивную фармакотерапию этого заболевания. - В ФГБУ «Центр стратегического планирования и управления медико-биологическими рисками здоровью» (Москва)проводились доклинические исследования лекарственного препарата для терапии болезни Альцгеймера. Продемонстрирован положительный эффект препарата на модели амнезии in vivo.
В области нейрореабилитации
Можно выделить работу, ведущуюся в Санкт-Петербургском государственном университете (Санкт-Петербург) в аспекте исследования моделей нейронной активности и биомаркеров состояний мозга человека с помощью методов искусственного интеллекта, в том числе для интеграции в общество людей с ограниченными возможностями.
В Научном центре неврологии (Москва) разрабатывается совместно с компанией-производителем система для транскраниальной магнитной стимуляции, совмещенной с когнитивным тренингом для персонализации адъювантной терапии различных вариантов нейрокогнитивной дисфункции.
В Санкт-Петербургском научно-исследовательском институте фтизиопульмонологии (Санкт-Петербург) проводится разработка инновационных технологий реабилитации на основе сочетанного применения ходьбы в экзоскелете и чрескожной электростимуляции спинного мозга у детей и подростков с нарушением локомоторной функции.
В отношении нейроинфекций
Особый интерес представляют исследования, проведенные в Детском научно-клиническом центре инфекционных болезней Федерального медико-биологического агентства (Санкт-Петербург), где проводились исследования с целью оптимизации системы мониторинга эффективности нейрореабилитации у детей-реконвалесцентов нейроинфекций.
В Научном центре неврологии (Москва) разрабатывается совместно с компанией-производителем система для транскраниальной магнитной стимуляции, совмещенной с когнитивным тренингом для персонализации адъювантной терапии различных вариантов нейрокогнитивной дисфункции.
В Санкт-Петербургском научно-исследовательском институте фтизиопульмонологии (Санкт-Петербург) проводится разработка инновационных технологий реабилитации на основе сочетанного применения ходьбы в экзоскелете и чрескожной электростимуляции спинного мозга у детей и подростков с нарушением локомоторной функции.
В отношении нейроинфекций
Особый интерес представляют исследования, проведенные в Детском научно-клиническом центре инфекционных болезней Федерального медико-биологического агентства (Санкт-Петербург), где проводились исследования с целью оптимизации системы мониторинга эффективности нейрореабилитации у детей-реконвалесцентов нейроинфекций.
- В качестве инструмента использовался специально разработанный протокол проведения диагностической транскраниальной магнитной стимуляции с оценкой параметров коркового вызванного моторного ответа с m. abductor hallucis и последующей коррекцией применяемых схем терапии в зависимости от динамики нейрофизиологических данных.
- В результате разработан алгоритм объективизации и мониторинга эффективности нейрореабилитационного процесса, проведена оценка его экономической эффективности за счет персонализированного подхода к реабилитации детей-реконвалесцентов нейроинфекций.
Сильные и слабые стороны.
Предложения по перспективному планированию
Предложения по перспективному планированию
Персонализированная неврология
является эволюцией существующих диагностических и терапевтических трендов.
В числе направлений ее дальнейшего развития:
является эволюцией существующих диагностических и терапевтических трендов.
В числе направлений ее дальнейшего развития:
- углубление интеграции результатов отечественных и мировых исследований по персонализации;
- потенциальное производство собственных аналогов ряда таргетных препаратов;
- внедрение методик искусственного интеллекта;
- финансовая оценка и пересмотр модели обеспечения медицины с учетом ее персонализации.
- расширение спектра неврологических заболеваний, для которых доступна персонализация;
- обобщение клинического материала, поиск надежных и валидных биомаркеров клинического течения и эффективности терапии;
- обеспечение возможностей использования передовых технологий в рутинной клинической практике с соответствующим финансовым и законодательным сопровождением.
К слабым сторонам развития данного направления в РФ можно отнести:
- недостаточную готовность первичного звена здравоохранения к внедрению высокотехнологичных методик персонализации;
- дефицит межотраслевой коммуникации в сфере научных разработок;
- слабую выраженность трансляции фундаментальных исследований в практическую плоскость и, особенно, клиническую практику;
- разрозненность тематик научно-исследовательских работ основных учреждений и отсутствие единой концепции в отношении изучения заболеваний нервной системы;
- низкий уровень приверженности пациентов (иногда врачей) к рекомендациям по профилактике и снижению риска социально значимых заболеваний нервной системы, что резко уменьшает потенциальную экономическую эффективность от имплементации результатов наработок по персонализированной неврологии;
- неудовлетворительное (в доступном нам понимании) юридическое сопровождение вопросов персонализации в медицине.
В отношении предложений по перспективному планированию:
- продолжение (и, возможно, расширение объема) работы Совета по ПМ РАН;
- расширение возможностей патентного сопровождения по разработанным технологиям;
- формирование научных тематик и планов заинтересованных учреждений с учетом возможностей трансляции результатов в сферу персонализации в неврологии;
- работа с клиническими учреждениями в отношении популяризации результатов собственных исследований и внедрения отечественных разработок;
- включение аспектов персонализации в медицине в образовательные программы для обучения студентов, ординаторов и аспирантов по соответствующим специальностям;
- привлечение компаний-производителей (оборудования, изделий, лекарственных препаратов и т.д.) и специалистов IT-сферы для ускорения технологического перехода с последующим выводом перспективных проектов на этап практической реализации.

Психиатрия
Основные направления
мировых исследований
мировых исследований
В области персонализированной профилактики наиболее важными следует признать направления поиска и валидации специфических биомаркеров высокого риска развития психических расстройств (прежде всего, геномных и эпигеномных) в целях стратификации популяции по наличию таких маркеров и проведения адресных специфических профилактических мероприятий.
Важным аспектом этих исследований является оценка взаимодействия генома и окружающей среды, в частности в виде неблагоприятного детского опыта в формировании уровня индивидуального риска развития психических расстройств. Сложная генетическая архитектура психических расстройств и объективные трудности оценки клинических фенотипов в психиатрии существенно затрудняют исследования.
В области персонализированной диагностики на первый план в современной психиатрии выходят исследования по поиску и валидации специфических биомаркеров и их систем, позволяющих надежно классифицировать основные варианты психических расстройств для целей максимально возможной объективизации индивидуальной диагностики. Важным направлением является разработка систем биомаркеров для ситуаций коморбидности психических расстройств и хронических соматических заболеваний в рамках комплексного персонализированного подхода.
В вопросах персонализированной терапии основное место занимают исследования в области фармакогеномики психических расстройств и разработка на основе результатов индивидуального фармакогенетического тестирования надежных систем поддержки принятия решений для врачей-психиатров в реальной клинической практике.
Другими многообещающими подходами являются:
Оценка роли клинических показателей, как дополнительных переменных, оптимизирующих прогностические модели, сегодня в сфере интересов персонализированной психиатрии. Учитывая, что ни один отдельный биомаркер, вероятно, не определит какое-либо психическое расстройство, риск его манифеста или ответ на фармакологическое воздействие, основной тренд – использование комплексных подходов к обнаружению для определения многомерных и комбинаторных профилей биомаркеров (в разных направлениях анализа), которые объясняют гетерогенность психических заболеваний в том виде, в каком они проявляются клинически.
В психиатрии, в отличие от прочих медицинских специальностей, имеется спектр специфических сложностей и ограничений, затрудняющих исследования и разработки в области персонализированной медицины.
Наиболее важными следует признать:
Вместе с тем, учитывая множественные ограничения этих исследований в психиатрии, важным является осторожность оценки трансляционного потенциала полученных результатов и необходимость их репликации на независимых выборках.
Важным аспектом этих исследований является оценка взаимодействия генома и окружающей среды, в частности в виде неблагоприятного детского опыта в формировании уровня индивидуального риска развития психических расстройств. Сложная генетическая архитектура психических расстройств и объективные трудности оценки клинических фенотипов в психиатрии существенно затрудняют исследования.
В области персонализированной диагностики на первый план в современной психиатрии выходят исследования по поиску и валидации специфических биомаркеров и их систем, позволяющих надежно классифицировать основные варианты психических расстройств для целей максимально возможной объективизации индивидуальной диагностики. Важным направлением является разработка систем биомаркеров для ситуаций коморбидности психических расстройств и хронических соматических заболеваний в рамках комплексного персонализированного подхода.
В вопросах персонализированной терапии основное место занимают исследования в области фармакогеномики психических расстройств и разработка на основе результатов индивидуального фармакогенетического тестирования надежных систем поддержки принятия решений для врачей-психиатров в реальной клинической практике.
- Наибольшее количество надежных фармакогенетических маркеров получено для оценки риска плохой переносимости психофармакотерапии и риска развития побочных эффектов на основе геномных маркеров в фармакокинетических системах.
- Научные сообщества (Международный консорциум по имплементации фармакогенетического тестирования в клиническую практику (Clinical Pharmacogenetics Implementation Consortium – CPIC)) и руководящие принципы FDA поддерживают использование генетической информации о ферментах печени в обычной клинической практике для определения терапевтической стратегии, подходящей дозировки или оценки вероятности пользы или токсичности.
- Однако генетические варианты, экспрессируемые в головном мозге, являются более сложными. После первоначального энтузиазма последних десятилетий научное сообщество пришло к пониманию того, что варианты оценки только печеночного метаболизма имеют ограниченный клинический эффект и, что наиболее важно, с большой вариабельностью у разных субъектов из-за компенсаторных систем и сложных механизмов экспрессии генов.
Другими многообещающими подходами являются:
- визуализация головного мозга,
- когнитивные тесты
- биомаркеры крови.
Оценка роли клинических показателей, как дополнительных переменных, оптимизирующих прогностические модели, сегодня в сфере интересов персонализированной психиатрии. Учитывая, что ни один отдельный биомаркер, вероятно, не определит какое-либо психическое расстройство, риск его манифеста или ответ на фармакологическое воздействие, основной тренд – использование комплексных подходов к обнаружению для определения многомерных и комбинаторных профилей биомаркеров (в разных направлениях анализа), которые объясняют гетерогенность психических заболеваний в том виде, в каком они проявляются клинически.
В психиатрии, в отличие от прочих медицинских специальностей, имеется спектр специфических сложностей и ограничений, затрудняющих исследования и разработки в области персонализированной медицины.
Наиболее важными следует признать:
- недостаточность данных об этиологии и патогенезе психических расстройств;
- высокий уровень психиатрической и соматической коморбидности;
- низкий уровень комплайенса психиатрических пациентов;
- отсутствие надежных, верифицированных и объективных лабораторных тестов и инструментальных методов диагностики.
Вместе с тем, учитывая множественные ограничения этих исследований в психиатрии, важным является осторожность оценки трансляционного потенциала полученных результатов и необходимость их репликации на независимых выборках.
Основные достижения ПМ и примеры успешной реализации в мире
Основные достижения в области персонализированной профилактики психических расстройств в мире связаны с существенным прогрессом в области геномики и биоинформатики, позволившими выявить системы геномных маркеров риска развития психических расстройств как в клинических, так и в популяционных исследованиях.
Основные достижения в области персонализированной профилактики психических расстройств в мире связаны с существенным прогрессом в области геномики и биоинформатики, позволившими выявить системы геномных маркеров риска развития психических расстройств как в клинических, так и в популяционных исследованиях.
Наибольшую роль играют полногеномные ассоциативные исследования (GWAS) больших и очень больших (до 1-2 млн участников) когорт, а также возможности построения и валидации полигенных шкал риска (PRS) и менделевской рандомизации на основе данных GWAS.
- Использование систем PRS как объективного метода оценки полигенного риска является перспективным и важным, прежде всего, в научном плане, в том числе для понимания общих механизмов формирования риска разных диагностических форм психических расстройств (Smoller et al., 2023), а также состояний коморбидности психических расстройств, особенно депрессии и многих хронических соматических заболеваний (Fanelli et al., 2022).
- Внедрение в клиническую практику персонализированных методов диагностики и профилактики, основанных на полигенных шкалах риска на данном этапе развития науки, затруднено из-за малой предсказательной силы (Martin et al., 2019).
- Исследования прогностических оценок (Koutsouleris et al., 2021) при психотических расстройствах отмечают, что полигенные оценки риска незначительно повышают эффективность моделей, основанных на клинических когнитивных данных, но остаются недостаточными для скрининга риска в общей популяции.
- Но последние сообщения Консорциума психиатрической геномики Британского биобанка-23 и исследования Me genome-wide association приходят к заключению о том, что полигенные оценки риска могут быть полезны для прогнозирования уязвимости к депрессии и устойчивости к стрессу (Fang et al., 2020).
Основное направление, получившее наиболее последовательное развитие в персонализированной психиатрии – это возможность использования фармакогенетического (PGx) тестирования, как инструмента поддержки принятия решений, помогающего продуманно осуществлять качественную клиническую помощь, улучшая, а не предлагая альтернативу стандартным протоколам лечения.
В этом контексте генетические маркеры могут дополнять
В этом контексте генетические маркеры могут дополнять
- демографическую (например, возраст, пол, семейный анамнез),
- клиническую информацию (например, сопутствующие лекарственные препараты)
- образ жизни (например, диета, курение), помогая принимать решения о выборе лечения.
Хотя до сих нет случаев официального одобрения ни одной системы фармакогенетического тестирования для медицинского применения, наиболее важным фактом является то, что сегодня учет результатов фармакогенетического тестирования в отношении безопасности применяемых лекарственных средств является частью инструкций по применению многих препаратов, применяемых для лечения психических расстройств в США и некоторых европейских странах. FDA, регулятор обращения лекарственных средств в США, отмечает, что многие фармакогенетические тесты предлагаются в виде лабораторно разработанных тестов, и публикует официальные таблицы, которые включают в себя определенные установленные взаимодействия генов и лекарств, которые фигурируют в маркировке лекарств, одобренных FDA. В таблицу также включены некоторые дополнительные взаимодействия генов и лекарств, которые соответствуют текущей маркировке FDA и для которых имеется достаточно научных доказательств, основанных на опубликованной литературе. Эти научные данные, основанные на литературе, часто используются в поддержку рекомендаций, содержащихся в профессиональных руководствах, используемых врачами.
По мнению FDA, фармакогенетические тесты, наряду с другой информацией о пациентах и их заболевании или состоянии, могут играть важную роль в лекарственной терапии. Когда поставщик медицинских услуг рассматривает возможность назначения лекарства, знание генотипа пациента может быть использовано для определения терапевтической стратегии, определения подходящей дозировки или оценки вероятности пользы или токсичности.
Крупнейший международный консорциум по имплементации фармакогенетического тестирования в клиническую практику (Clinical Pharmacogenetics Implementation Consortium – CPIC) среди ряда клинических рекомендаций
Имеется несколько примеров успешного продвижения систем фармакогенетических тестов в психиатрии.
Метаанализ шести подобных тестов при лечении депрессии в Канаде показал значительную вариабельность терапевтического и экономического эффекта тестирования и СПРР на его основе в зависимости и от самих тестов, и от клинической гетерогенности пациентов, что затрудняет принятие решения о возможности широкого использования подобного тестирования в реальной клинической практике (Ontario Health (Quality), 2021).
Сегодня эффективность рутинного фармакогенетического тестирования в психиатрической практике в ряде стран Европы и в США является предметом многочисленных исследований, делающих акцент на переносимости, частоте смены препаратов, специфических пациентов с полипрагмазией, а также на экономической целесообразности тестирования и систем помощи принятия решений (СППР) на их основе (Frye et al., 2023; Paribello et al., 2023; Correia et al., 2022).
В условиях широкого применения в мире алгоритмов СППР в психиатрии на основе фармакогенетических тестов следует ожидать накопления критической массы оценки терапевтической и фармакоэкономической целесообразности их использования в качестве обязательного элемента в системе оказания психиатрической помощи. Следует отметить, что все существующие фармакогенетические тесты были разработаны в эпоху «генов-кандидатов» и, возможно, имеющиеся проблемы с их применением связаны именно с этим.
Появление новых комплексных систем для персонализации терапии психических расстройств на основе фармакогеномики может изменить ситуацию.
Сегодня ведутся исследования с применением технологий GWAS и PRS для поиска комплексных геномных маркеров терапевтического ответа
Таким образом, ожидается, что PGx-тестирование станет важным инструментом в психиатрии, облегчающим процесс проб и ошибок, которому в настоящее время подвергаются многие люди.
По мнению FDA, фармакогенетические тесты, наряду с другой информацией о пациентах и их заболевании или состоянии, могут играть важную роль в лекарственной терапии. Когда поставщик медицинских услуг рассматривает возможность назначения лекарства, знание генотипа пациента может быть использовано для определения терапевтической стратегии, определения подходящей дозировки или оценки вероятности пользы или токсичности.
Крупнейший международный консорциум по имплементации фармакогенетического тестирования в клиническую практику (Clinical Pharmacogenetics Implementation Consortium – CPIC) среди ряда клинических рекомендаций
- имеет рекомендации по трициклическим антидепрессантам (генотипы цитохромов CYP2D6, CYP2C19),
- антидепрессантам-ингибиторам обратного захвата серотонина (СИОЗС) (генотипы CYP2D6, CYP2C19, CYP2B6, SLC6A4, HTR2A)
- атомоксетина для лечения СДВГ (генотипы CYP2D6).
- В этом исследовании были собраны индивидуальные данные из 13 клинических исследований популяций европейского и восточноазиатского происхождения.
- Среди 5843 пациентов с депрессией была обнаружена более высокая частота ремиссии у лиц с плохим метаболизмом CYP2C19 по сравнению с нормальными метаболизаторами при номинальном значении уровня значимости (OR = 1,46, 95 % ДИ [1,03, 2,06], р = 0,033), которое исчезло при поправке на множественное сравнение.
- Ни один метаболический фенотип не был связан с процентным улучшением по сравнению с исходным уровнем. После разделении антидепрессантов по метаболизму преимущественно с помощью CYP2C19 и CYP2D6, связи между метаболическими фенотипами и реакцией на антидепрессанты обнаружено не было.
Имеется несколько примеров успешного продвижения систем фармакогенетических тестов в психиатрии.
- Наиболее успешным и известным является алгоритм Combinatorial Pharmacogenomic (CPGx™) GeneSight test, первично разработанный для применения антидепрессантов (Altar et al., 2015). Алгоритм является коммерческим продуктом и использует генотипы цитохромов P450 (CYP) CYP2D6, CYPC19, CYP1A2, генотипы некоторых полиморфизмов генов белка-переносчика серотонина (SLC6A4) и рецептора серотонина 5-HT2A (HTR2A).
- сертралина (Parikh et al., 2021), циталопрама и эсциталопрама (Shelton et al., 2020),
- при лечении депрессии в условиях реальной клинической практики без выделения определенного препарата (Brown et al., 2020).
- Показана хорошая эффективность алгоритма у пациентов молодого возраста и подростков (Dagar et al., 2022). В то же время для педиатрических пациентов требуется особая осторожность (Ariefdjohan et al., 2021).
Метаанализ шести подобных тестов при лечении депрессии в Канаде показал значительную вариабельность терапевтического и экономического эффекта тестирования и СПРР на его основе в зависимости и от самих тестов, и от клинической гетерогенности пациентов, что затрудняет принятие решения о возможности широкого использования подобного тестирования в реальной клинической практике (Ontario Health (Quality), 2021).
Сегодня эффективность рутинного фармакогенетического тестирования в психиатрической практике в ряде стран Европы и в США является предметом многочисленных исследований, делающих акцент на переносимости, частоте смены препаратов, специфических пациентов с полипрагмазией, а также на экономической целесообразности тестирования и систем помощи принятия решений (СППР) на их основе (Frye et al., 2023; Paribello et al., 2023; Correia et al., 2022).
В условиях широкого применения в мире алгоритмов СППР в психиатрии на основе фармакогенетических тестов следует ожидать накопления критической массы оценки терапевтической и фармакоэкономической целесообразности их использования в качестве обязательного элемента в системе оказания психиатрической помощи. Следует отметить, что все существующие фармакогенетические тесты были разработаны в эпоху «генов-кандидатов» и, возможно, имеющиеся проблемы с их применением связаны именно с этим.
Появление новых комплексных систем для персонализации терапии психических расстройств на основе фармакогеномики может изменить ситуацию.
Сегодня ведутся исследования с применением технологий GWAS и PRS для поиска комплексных геномных маркеров терапевтического ответа
- на антидепрессанты (Fanelli et al., 2022),
- терапевтической резистентности в отношении антидепрессантов (Wigmore et al., 2020),
- ответа на терапию литием у пациентов с БАР (Schubert et al., 2021),
- риска индукции маниакального состояния в результате применения антидепрессантов (Zai et al., 2023),
- терапевтической резистентности при шизофрении (Pardiñas et al., 2022).
Таким образом, ожидается, что PGx-тестирование станет важным инструментом в психиатрии, облегчающим процесс проб и ошибок, которому в настоящее время подвергаются многие люди.
Fanelli G., Sokolowski M., Wasserman D. et al. Polygenic risk scores for neuropsychiatric, inflammatory, and cardio-metabolic traits highlight possible genetic overlap with suicide attempt and treatment-emergent suicidal ideation // Am J Med Genet B Neuropsychiatr Genet. 2022;189(3-4):74-85. DOI: 10.1002/ajmg.b.32891
Rothschild A.J., Parikh S.V., Hain D. et al. Clinical validation of combinatorial pharmacogenomic testing and single-gene guidelines in predicting psychotropic medication blood levels and clinical outcomes in patients with depression // Psychiatry Res. 2021;296:113649. DOI: 10.1016/j.psychres.2020.113649
Schubert K.O., Thalamuthu A., Amare A.T., et al. Combining schizophrenia and depression polygenic risk scores improves the genetic prediction of lithium response in bipolar disorder patients [published correction appears in Transl Psychiatry. 2022 Jul 11;12(1):278] // Transl Psychiatry. 2021;11(1):606. DOI: 10.1038/s41398-021-01702-2
Зарегистрированные в мире лекарственные препараты или изделия (в том числе ПО), которые внедрены в практику и имеют персонализированные показания к применению:
Метод, доступный через веб-интерфейс, и система, предоставляющая персонифицированные рекомендации по применению лекарственных средств, а также машиночитаемый носитель.
Нейрофармаген предоставляет информацию в общей сложности о 62 препаратах, используемых при депрессии, шизофрении, СДВГ, обсессивно-компульсивном, биполярном и тревожном расстройствах, на основе более чем 60 полиморфизмов, проанализированных в 25 генах, регулирующих фармакокинетику и фармакодинамику препаратов.
Включает соответствующую фармакогенетическую информацию, содержащуюся в инструкциях по применению препаратов, одобренных основными агентствами, а также рекомендации признанных групп экспертов.
Анализируемые гены:
В дополнение к фармакогенетическому анализу терапевтическая система управления демонстрирует в режиме реального времени влияние возможных лекарственных взаимодействий.
Доказательная база включает
Нейрофармаген предоставляет информацию в общей сложности о 62 препаратах, используемых при депрессии, шизофрении, СДВГ, обсессивно-компульсивном, биполярном и тревожном расстройствах, на основе более чем 60 полиморфизмов, проанализированных в 25 генах, регулирующих фармакокинетику и фармакодинамику препаратов.
Включает соответствующую фармакогенетическую информацию, содержащуюся в инструкциях по применению препаратов, одобренных основными агентствами, а также рекомендации признанных групп экспертов.
Анализируемые гены:
- энзимы, метаболизирующие лекарственные препараты (DME): цитохром P450 (CYP2D6, CYP2C19, CYP3A4, CYP1A2, CYP2B6, CYP2C9); другие (CES1, EPHX1, UGT2B15);
- транспортировка лекарственного препарата: ABCB1;
- гены серотонина: SLC6A4, HTR2A, HTR2C;
- протеины, передающие сигнал: BDNF, GRIK4, AKT1-DDIT4-FCHSD1-RPTOR;
- протеины главного комплекса гистосовместимости: HLA-A;
- другие: CACNG2, COMT, DDIT4, FCHSD1, GRIK2, LPHN3, OPRM1, RPTOR.
В дополнение к фармакогенетическому анализу терапевтическая система управления демонстрирует в режиме реального времени влияние возможных лекарственных взаимодействий.
Доказательная база включает
- многоцентровое рандомизированное контролируемое исследование при тяжелой депрессии, проведенное в 18 государственных больницах Испании;
- 6 дополнительных рандомизированных и наблюдательных исследований у психиатрических пациентов разных национальностей и с различными диагнозами, включая пациентов с шизофренией, биполярным расстройством и СДВГ;
- 1 мета-анализ тестов RCT, проведенных с продуктом у пациентов с большим депрессивным расстройством.
– коммерческий продукт: алгоритм СППР для врача на основе фармакогенетического тестирования, включает блоки по переносимости и эффективности. Включен в руководтсва (Clinical Pharmacogenetics Implementation Consortium – CPIC) для СИОЗС.
Анализ полноты исследований экспертной группой
Исследования в области персонализированных подходов в психиатрии в РФ находятся в русле основных мировых направлений, тенденций и отражает все трудности, которые имеются в развитии персонализированной психиатрии. Различные психические расстройства часто имеют много общих клинических симптомов и аналогичным образом большинство нейробиологических субстратов присутствуют во всех диагностических категориях. Хотя диагностические категории помогают осмыслить высокую вариабельность симптомов, трудности представляет точная стратификация подгрупп пациентов на основе как надежных клинических данных, так и соответствующих биомаркеров.
Сегодня можно говорить об определенных результатах в области персонализированной профилактики и в разработке фармакогенетических систем поддержки принятия решений, а исследования в области персонализированной диагностики находятся в развитии. Одного лидера в области персонализированной психиатрии в нашей стране выделить нельзя, каждый из научных центров обладает уникальными компетенциями и развивается в наиболее перспективном для него направлении.
Исследования в области персонализированных подходов в психиатрии в РФ находятся в русле основных мировых направлений, тенденций и отражает все трудности, которые имеются в развитии персонализированной психиатрии. Различные психические расстройства часто имеют много общих клинических симптомов и аналогичным образом большинство нейробиологических субстратов присутствуют во всех диагностических категориях. Хотя диагностические категории помогают осмыслить высокую вариабельность симптомов, трудности представляет точная стратификация подгрупп пациентов на основе как надежных клинических данных, так и соответствующих биомаркеров.
Сегодня можно говорить об определенных результатах в области персонализированной профилактики и в разработке фармакогенетических систем поддержки принятия решений, а исследования в области персонализированной диагностики находятся в развитии. Одного лидера в области персонализированной психиатрии в нашей стране выделить нельзя, каждый из научных центров обладает уникальными компетенциями и развивается в наиболее перспективном для него направлении.
1.Успешными и перспективными являются исследования ФГБУ НМИЦ ПН им. В.М. Бехтерева (Санкт-Петербург) в рамках проектов по поиску полигенных шкал риска развития психических расстройств на основе полногеномных ассоциативных исследований (GWAS) на популяционном уровне с клинической валидацией.
3.Важными и перспективными являются исследования в области поиска биологических и генетических маркеров высокого риска развития тяжелых побочных эффектов психофармакотерапии (Томский НИМЦ, НИИ психического здоровья, г. Томск), применение которых возможно для проведения персонализированных профилактических программ среди пациентов с психическими расстройствами. Ряд результатов имеют мировой уровень новизны. Широкое применение современных методов анализа и «омиксных» технологий делают эти исследования особенно интересными.
4.Важными являются многолетние исследования НЦПЗ (Москва) в области поиска геномных маркеров рискаразвития шизофрении,в том числе в рамках взаимодействия генома и окружающей среды с учетом особенностей личности.
- Исследования проводятся на современном научном и технологическом уровне с применением комплексного методологического подхода, включающего методологию психиатрии, генетики, биоинформатики и клинической психологии. Получены и подготовлены для дальнейшей валидации на независимых выборках системы полигенных шкал риска развития депрессий, а также предварительные полигенные шкалы риска развития генетически коморбидных с депрессией хронических соматических заболеваний.
- Выявление и валидация геномных маркеров высокого риска коморбидных депрессии и хронических соматических заболеваний может способствовать поиску общих биологических механизмов этих заболеваний с возможностью получения валидных генетических маркеров для успешной стратификации популяционных когорт в целях формирования групп высокого и ультравысокого риска развития генетически коморбидных заболеваний.
- Полученные системы геномных маркеров могут быть использованы в целях адресной специфической профилактики в популяционных группах, стратифицированных на основе таких маркеров. Полученные результаты имеют мировой уровень новизны и являются совершенно новыми для российской популяции.
- Развитие этого направления продолжается с фокусом на оценку риска суицидального поведения у пациентов с психическими расстройствами на основе анализа взаимодействия генома и неблагоприятного детского опыта.
3.Важными и перспективными являются исследования в области поиска биологических и генетических маркеров высокого риска развития тяжелых побочных эффектов психофармакотерапии (Томский НИМЦ, НИИ психического здоровья, г. Томск), применение которых возможно для проведения персонализированных профилактических программ среди пациентов с психическими расстройствами. Ряд результатов имеют мировой уровень новизны. Широкое применение современных методов анализа и «омиксных» технологий делают эти исследования особенно интересными.
4.Важными являются многолетние исследования НЦПЗ (Москва) в области поиска геномных маркеров рискаразвития шизофрении,в том числе в рамках взаимодействия генома и окружающей среды с учетом особенностей личности.
- В этом направлении представляется перспективным исследование разработки высоконадежной модели раннего прогнозирования риска шизофрении в группах больных с аттенуированными симптомами шизофренического спектра.
- Исследование включает результаты морфометрического обследования головного мозга (снижение толщины серого вещества в левых постцентральных извилинах коры головного мозга, и увеличение толщины в правой задней поясной коре и передней части передней поясной извилины), иммунологических показателей, нейрофизиологических показателей (когерентность и спектральная мощность бета-1 диапазона), а также молекулярно-генетических данных (показатели полигенного риска с использованием данных полногеномного анализа ассоциаций).
Проблемы персонализированного подхода к терапии тяжелых многофакторных психических расстройств связаны, прежде всего, с недостаточными знаниями о молекулярных механизмах их патогенеза.
В последние годы появляется все больше сведений о том, что шизофрения, биполярное расстройство, депрессия и другие психические расстройства являются фенотипами, соответствующими множеству генотипических и биологических вариантов. В каждом из таких биотипов ведущую роль играют отдельные молекулярные механизмы. В связи с этим разработка принципиально новых подходов к терапии психических расстройств возможна с учетом персонифицированного подхода – с выделением внутри разнообразной группы больных с общим психиатрическим диагнозом подтипов не с учетом фенотипических проявлений, а с учетом общих молекулярных механизмов патогенеза.
Наиболее важные результаты получены в НЦПЗ в результате многолетних исследований биологических, в частности, иммунологических маркеров различных клинических вариантов развития психических расстройств.
Интересные результаты пилотных исследований получены в ФФМ МГУ им. М.В. Ломоносова, кафедра психиатрии, наркологии и психотерапии ФДПО МГМСУ им. А.И. Евдокимова.
В последние годы появляется все больше сведений о том, что шизофрения, биполярное расстройство, депрессия и другие психические расстройства являются фенотипами, соответствующими множеству генотипических и биологических вариантов. В каждом из таких биотипов ведущую роль играют отдельные молекулярные механизмы. В связи с этим разработка принципиально новых подходов к терапии психических расстройств возможна с учетом персонифицированного подхода – с выделением внутри разнообразной группы больных с общим психиатрическим диагнозом подтипов не с учетом фенотипических проявлений, а с учетом общих молекулярных механизмов патогенеза.
Наиболее важные результаты получены в НЦПЗ в результате многолетних исследований биологических, в частности, иммунологических маркеров различных клинических вариантов развития психических расстройств.
- В результате перспективных исследований НЦПЗ в отношении возможности построения комплексных предиктивных моделей возможно появление алгоритмов персонализации диагностических подходов.
Интересные результаты пилотных исследований получены в ФФМ МГУ им. М.В. Ломоносова, кафедра психиатрии, наркологии и психотерапии ФДПО МГМСУ им. А.И. Евдокимова.
Наиболее успешными в области поиска фармакогенетических маркеров и систем поддержки принятия решений для врачей-психиатров являются разработки РМАНПО (Москва) и Томского НИМЦ, НИИ психического здоровья (Томск). Лидеры этого направления работают в параллельных областях.
К таким факторам относятся:
Возможно, противоречивость результатов клинических исследований по применению нутриентов, полученных до недавнего прошлого, была обусловлена неоднородностью всей популяции пациентов с каждым из изучаемых психических расстройств: у разных пациентов ведущими могут быть разные патогенетические механизмы, и даже у одного и того же пациента на разных этапах развития болезни один патогенетический механизм может сменяться другим (например, известно, что оксидативный стресс играет наиболее значимую роль при первом эпизоде психоза, а в дальнейшем уступает место другим механизмам).
Классический кросс-секционный дизайн локальных исследований на малых выборках предоставил к настоящему времени обширное количество разрозненных данных, синтез и валидизация которых, вероятно, требует новых подходов: многоцентровых исследований в рамках мультидисциплинарных консорциумов с глубоким фенотипированием и расширенным лабораторным обследованием пациентов (с использованием омиксных технологий) для стратификации выборок пациентов.
Диагностика большинства известных биомаркеров сейчас может осуществляться доступными даже в рутинной клинической практике методами.
Современные возможности лабораторной диагностики и новые данные, полученные в общебиологических, в частности генетических исследованиях, открывают новые перспективы для этиопатогенетического вмешательства при мультифакторных психических расстройствах.
Тонкая молекулярная диагностика наличия у пациента отклонений ряда биологических параметров, имеющих отношение к этиопатогенезу, может позволить таргетно для конкретного пациента подобрать безопасные стратегии компенсации выявленных нарушений, что дает надежды на улучшение терапевтического прогноза.
В совместных исследованиях НМИЦ ПН им. В.М. Бехтерева и ПИМУ успешно проведено такое исследование и получены результаты, которые имеют трансляционный потенциал.
Общими проблемами всех научных центров являются невысокий технологический уровень исследований, низкий уровень финансирования, в основном за счет РНФ и других грантов, а также системная разобщенность и отсутствие полноценных и продуктивных коллабораций между научными центрами. Имеет место частое дублирование тем и направлений, многие исследования выполняются с идентичным дизайном на близких клинических выборках пациентов.
В отношении результатов фармакогенетических исследований в области психиатрии имеется известное ограничение в виде отсутствия национальных исследований для формирования отечественных регуляторных механизмов в отношении применения результатов фармакогенетического тестирования в практической психиатрии.
- Коллектив РМАНПО ведет поиск фармакогенетических маркеров переносимости различных вариантов психофармако терапии у пациентов с алкогольной зависимостью с коморбидными аффективными расстройствами. Ряд важных результатов получен при изучении фармакогенетики применения антипсихотиков у подростков с шизофренией.
- Коллектив Томского НИМЦ, НИИ психического здоровья, ведет успешные многолетние исследования фармакогенетических маркеров высокого риска развития серьезных побочных эффектов терапии антипсихотиками у пациентов с шизофренией: метаболических нарушений и экстрапирамидных расстройств.
- Фармакогенетические исследования небольших выборок проведены в НМИЦ ПН им. В.М. Бехтерева, НМИЦ ПН им. В.М. Сербского;
- Интересные пилотные результаты получены в ГБУЗ «Психиатрическая клиническая больница № 1 им. Н.А. Алексеева Департамента здравоохранения города Москвы», а также в НИИ фармакологии и Читинской государственной медицинской академии Минздрава РФ.
- Существенными ограничениями этих исследований следует признать ретроспективный метод оценки клинических фенотипов и кросс-секционный дизайн.
К таким факторам относятся:
- дефициты витаминов (фолатов, кобаламина, витамина D),
- редокс-дисбаланс (дефицит эндогенных антиоксидантов, в частности восстановленного глутатиона),
- нейровоспаление и аутоиммунные состояния (связанные с выработкой аутоантител к белкам головного мозга),
- дефицит окситоцина, митохондриальная дисфункция (дефицит коэнзима Q10), нарушения кишечной микробиоты.
Возможно, противоречивость результатов клинических исследований по применению нутриентов, полученных до недавнего прошлого, была обусловлена неоднородностью всей популяции пациентов с каждым из изучаемых психических расстройств: у разных пациентов ведущими могут быть разные патогенетические механизмы, и даже у одного и того же пациента на разных этапах развития болезни один патогенетический механизм может сменяться другим (например, известно, что оксидативный стресс играет наиболее значимую роль при первом эпизоде психоза, а в дальнейшем уступает место другим механизмам).
Классический кросс-секционный дизайн локальных исследований на малых выборках предоставил к настоящему времени обширное количество разрозненных данных, синтез и валидизация которых, вероятно, требует новых подходов: многоцентровых исследований в рамках мультидисциплинарных консорциумов с глубоким фенотипированием и расширенным лабораторным обследованием пациентов (с использованием омиксных технологий) для стратификации выборок пациентов.
Диагностика большинства известных биомаркеров сейчас может осуществляться доступными даже в рутинной клинической практике методами.
Современные возможности лабораторной диагностики и новые данные, полученные в общебиологических, в частности генетических исследованиях, открывают новые перспективы для этиопатогенетического вмешательства при мультифакторных психических расстройствах.
Тонкая молекулярная диагностика наличия у пациента отклонений ряда биологических параметров, имеющих отношение к этиопатогенезу, может позволить таргетно для конкретного пациента подобрать безопасные стратегии компенсации выявленных нарушений, что дает надежды на улучшение терапевтического прогноза.
В совместных исследованиях НМИЦ ПН им. В.М. Бехтерева и ПИМУ успешно проведено такое исследование и получены результаты, которые имеют трансляционный потенциал.
Общими проблемами всех научных центров являются невысокий технологический уровень исследований, низкий уровень финансирования, в основном за счет РНФ и других грантов, а также системная разобщенность и отсутствие полноценных и продуктивных коллабораций между научными центрами. Имеет место частое дублирование тем и направлений, многие исследования выполняются с идентичным дизайном на близких клинических выборках пациентов.
В отношении результатов фармакогенетических исследований в области психиатрии имеется известное ограничение в виде отсутствия национальных исследований для формирования отечественных регуляторных механизмов в отношении применения результатов фармакогенетического тестирования в практической психиатрии.
Специальные государственные программы, федеральные целевые программы, ведомственные программы
В настоящее время проводится несколько фундаментальных исследований, направленных на разработку новых препаратов. К ним относятся:
1. Поиск новых терапевтических подходов:
3. «Серотониновые рецепторы как новая мишень для лечения болезни Альцгеймера» (ИЦиГ СО РАН, Новосибирская обл.). Объединенные результаты, полученные в рамках проекта, лягут в основу разработки новой терапевтической стратегии лечения БА и нейродегенеративных заболеваний в целом.
В настоящее время проводится несколько фундаментальных исследований, направленных на разработку новых препаратов. К ним относятся:
1. Поиск новых терапевтических подходов:
- «Иммунные механизмы хронического системного воспаления в патогенезе шизофрении» (Институт химической биологии и фундаментальной медицины Сибирского отделения Российской академии наук – ИХБФМ СО РАН, Новосибирская обл.).
- Идентификация иммунных механизмов, приводящих к хроническому системному воспалению при шизофрении, даст направления для разработки новых терапевтических подходов для противовоспалительной терапии, которые будут влиять на причины воспалительных реакций.
3. «Серотониновые рецепторы как новая мишень для лечения болезни Альцгеймера» (ИЦиГ СО РАН, Новосибирская обл.). Объединенные результаты, полученные в рамках проекта, лягут в основу разработки новой терапевтической стратегии лечения БА и нейродегенеративных заболеваний в целом.
Заключение.
Предложения по перспективному планированию
Предложения по перспективному планированию
- В настоящее время имеющиеся сведения свидетельствуют о том, что нейробиологические данные могут повысить прогностическую точность клинических моделей для прогнозирования риска психических расстройств и оценки результатов терапевтических вмешательств, однако в настоящее время в РФ, как и в мировой психиатрии, имеющиеся результаты находятся не на том уровне значимости, чтобы оправдать целесообразность ежедневного использования в клинической практике. Более высокая специфичность, иногда наблюдаемая в моделях, основанных на нейробиологии, по сравнению с исключительно клиническими данными, в большей степени имеет научное значение и представляет интерес для выявления лежащих в основе этиологических процессов психических расстройств, учитывая гетерогенность клинической феноменологии. Наиболее перспективными представляются прогностические модели комплексного характера, учитывающие биологические, в том числе геномные маркеры, анамнестические и клинические характеристики, а также ряд факторов, характеризующих личностные особенности. Таким образом, наилучшие возможности для персонализированной психиатрии открываются при построении прогностических моделей на основе современной трактовки биопсихосоциальной модели этиологии и патогенеза психических расстройств.
- Передовая наука о мультимодальных данных, использующая клинические, нейровизуализационные, протеомные, геномные и количественные показатели биомаркеров, обладает потенциалом для решения ключевых задач в психиатрии. Это включает в себя определение подгрупп для новых целенаправленных методов лечения, улучшение индивидуальной направленности существующих методов лечения и выявление лиц, подверженных риску развития расстройства или рецидива существующих состояний. Однако рутинное использование машинного обучения для вынесения клинических заключений еще не принесло результатов, а его независимое использование еще не превзошло возможности самых точных предположений клиницистов. Возможно, это не фундаментальный недостаток персонифицированной психиатрии, а существующая проблема доступности данных для уже разработанных, высокоэффективных моделей, которые имеют перспективу применения в условиях реального мира.
- Выявление и анализ значимых клинических фенотипов или биологически информативных фенотипов, пригодных для точного количественного анализа, имеет основополагающее значение для прогресса в развитии персонализированной психиатрии. Различные психические расстройства часто имеют много общих индивидуальных симптомов, и, аналогичным образом, большинство нейробиологических субстратов присутствуют в разнообразных диагностических категориях. Хотя диагностические категории помогают осмыслить высокую вариабельность симптомов, необходимы исследования для точной стратификации подгрупп пациентов на основе как надежных клинических данных, так и соответствующих биомаркеров. Это будет способствовать разработке селективных показаний для персонализированных методов лечения.
- Реализация мультидисциплинарного подхода и объединение компетенций клиницистов, генетиков, физиологов, биохимиков и специалистов в области биоинформатики и анализа больших данных. Учитывая, что ни один отдельный биомаркер, вероятно, не определит какое-либо психическое расстройство в соответствии с традиционными диагностическими границами, важно использовать параллельные подходы для определения многомерных и комбинаторных профилей биомаркеров и их систем на основе мультимодальных данных, которые объясняют гетерогенность психических заболеваний в том виде, в каком они проявляются клинически. Такой подход может помочь клиницистам в диагностике, прогнозировании реакции на лечение и выборе метода лечения, а также дать ключ к молекулярной основе для разработки новых и более адаптированных и специфичных методов лечения.
- Более тесное объединение отдельных научных коллективов в рамках национальных научных коллабораций с исследовательскими целями и задачами и создание общих исследовательских проектов даст возможность увеличить мощность выборки и выделить когорты для репликации полученных результатов. Для РФ важность объединения определяется географическими и мультикультуральными факторами, важными для изучения психических расстройств, полиэтничностью населения и необходимостью минимизации и контроля влияния факторов, имеющих локальную или региональную специфичность.
- Расширение биологических знаний и параллельное развитие электронных медицинских карт в психиатрических стационарах сделают доступным беспрецедентный объем информации для понимания индивидуальной реакции на лечение.
- Учитывая высокую коморбидность психических расстройств с широким кругом соматических заболеваний, важным представляются совместные исследования психиатров и специалистов в соматической медицине для выявления общих звеньев патогенеза и формирования комплексных программ персонифицированного подхода к лечению конкретного пациента.
- Развитие биобанков для приема, обработки и хранения биологических образцов лиц с психическими расстройствами и ассоциированной с ними клинической информации для текущих и будущих исследований в соответствии со стандартными операционными процедурами.
- На настоящий момент в НМИЦ ПН им. В.М. Бехтерева развивается биобанк, направленный на коллекционирование биообразцов и ассоциированная с ними информация о лицах с психическими расстройствами и неврологическими заболеваниями. Общий фонд биобанка НМИЦ ПН им. В.М. Бехтерева составляет уже более 2700 биообразцов различных нозологий.

Редкие наследственные болезни
Основные направления
мировых исследований
мировых исследований
Основные направления исследований в области ПМ наследственных орфанных заболеваний определяются успехами молекулярно-генетической диагностики и установления патогенетических механизмов развития болезней. Для разработки таргетной терапии наследственных болезней необходимо глубокое понимание этио-патогенетических составляющих, зачастую зависящих от разных факторов в каждом отдельном случае. Неврологические, офтальмологические, гастроэнтерологические и другие наследственные болезни, зачастую инвалидизирующие и нередко жизнеугрожающие, связаны с проблемами не только разработки препаратов, но и доставки препарата до таргетного органа или ткани.
Основные направления мировых исследований в области ПМ по профилю редкие наследственные болезни базируются на результатах фундаментальных исследований, раскрывающих этиологию и ключевые патогенетическе пути реализации генетической информации от гена до симптома заболевания, что позволяет разрабатывать эффективную таргетную терапию, влияющую на звенья патогенеза. Прогрессирующий характер большинства наследственных заболеваний повышает значимость ранней постановки диагноза для принятия терапевтических решений.
Ключевые направления:
Основные направления мировых исследований в области ПМ по профилю редкие наследственные болезни базируются на результатах фундаментальных исследований, раскрывающих этиологию и ключевые патогенетическе пути реализации генетической информации от гена до симптома заболевания, что позволяет разрабатывать эффективную таргетную терапию, влияющую на звенья патогенеза. Прогрессирующий характер большинства наследственных заболеваний повышает значимость ранней постановки диагноза для принятия терапевтических решений.
Ключевые направления:
- Точная диагностика и мониторинг заболеваний требует открытия биомаркеров наследственных заболеваний, позволяющих диагностировать болезнь на ранних этапах, проводить мониториг лечения и разрабатывать эффективные методы массового скрининга.
- Разработка тест-систем на основе NGS-секвенирования и подходов диагностики для заболеваний, обусловленных низкоуровневым соматическим мозаицизмом (PROS, RAS-патий и др.), в том числе сегметарных форм факоматозов для верификации каузативного гена и подбора таргетной терапии, останавливающей патологический рост опухолевой ткани.
- Разработка и внедрение программных алгоритмов и искусственного интеллекта для анализа фенотипических признаков пациента с целью диагностики наследственных синдромов, характеризующихся особенностями фенотипа.
- Использование результатов «статистической медицины», полученных при анализе больших массивов данных различных групп, в том числе популяционных, нозологических и других в биоинформатическом анализе геномных данных конкретного случая с целью определения индивидуальной диагностической и терапевтической траектории.
- Генная терапия путем доставки и встраивания копий генов или мини-, микрогенов в геном соматических клеток пациентов. В качестве примеров можно привести многочисленные разработки не только для наследственных нервно-мышечных, но и для разных других групп наследственных болезней. В частности, стадию доклинических испытаний проходит лентивирусный вектор LV-Mpz.SH3TC2.mycдля лечения аутосомно-рецессивной моторно-сенсорной нейропатии типа 4С.
- Редактирование генов с использованием технологий на основе CRISPR, ZFNs или TALENs. Редактирование генома с помощью системы CRISPR/Cas9 показало свою эффективность в терапии ряда заболеваний и остается перспективным для лечения многих состояний. Активно изучается возможность удаления экспансии тринуклеотидных повторов CTG в гене DMPK, ответственных за развитие дистрофической миотонии 1-го типа.
- Модуляция РНК (пропуск экзона, блокировка нонсенс-опосредованного распада мРНК, транс-сплайсинг, применение антисмысловых олигонуклеотидов). Крайне перспективными препаратами являются антисмысловые олигонуклеотиды для лечения одной из самых частых мышечных дистрофий Ландузи – Дежерина, обусловленной активацией транскрипционного фактора DUX4.
- Клеточная терапия (применение перепрограммированных плюрипотентных стволовых клеток, сателлитных клеток). В течение десятилетий изучаются возможности лечения мышечных дистрофий с помощью мезоангиобластов, миобластов и перепрограммированных плюрипотентных стволовых клеток. На сегодняшний день перспективными для восстановления мышечной ткани являются аллогенные интерстициальные клетки PW1pos/Pax7neg, полученные из скелетных мышц свиньи.
Основные достижения ПМ и примеры успешной реализации в мире
Возможности персонализированного терапевтического вмешательства, как симптоматического, так и модифицирующего течение болезни, неуклонно расширяются с каждым годом, особенно это касается орфанных наследственных заболеваний.
Возможности ПМ для орфанных болезней варьируют от диетотерапии, фермент-заместительной терапии, трансплантации органов и стволовых клеток до возможности редактирования генома и генной терапии. Значительные успехи в эффективной таргетной терапии достигнуты для ряда наследственных нервно-мышечных болезней. Сегодня существуют не единичные препараты, а выбор препаратов для лечения спинальной мышечной атрофии 5q (СМА 5q) и мышечной дистрофии Дюшенна.
Возможности персонализированного терапевтического вмешательства, как симптоматического, так и модифицирующего течение болезни, неуклонно расширяются с каждым годом, особенно это касается орфанных наследственных заболеваний.
Возможности ПМ для орфанных болезней варьируют от диетотерапии, фермент-заместительной терапии, трансплантации органов и стволовых клеток до возможности редактирования генома и генной терапии. Значительные успехи в эффективной таргетной терапии достигнуты для ряда наследственных нервно-мышечных болезней. Сегодня существуют не единичные препараты, а выбор препаратов для лечения спинальной мышечной атрофии 5q (СМА 5q) и мышечной дистрофии Дюшенна.
Выбор препарата при мышечной дистрофии Дюшенна зависит от типа патогенного варианта, выявленного при проведении молекулярно-генетического исследования.
- Так, препарат Аталурен сегодня успешно применяется только у пациентов с нонсенс-вариантами в гене DMD (McDonald, 2017) как в России, так и во всем мире.
- Механизм действия ряда других лекарственных средств направлен на пропуск экзона или экзонов без сдвига рамки считывания, в котором или которых находится патогенный вариант нуклеотидной последовательности.
- Разработаны системы, приводящие к пропуску экзонов 44, 45, 51, 53 гена DMD, которые успешно проходят разные стадии клинических испытаний (Brogna, 2019).
- На третьей фазе клинических испытаний находится препарат генной терапии – микродистрофин (SRP-9001), короткая и функциональная версия гена DMD, доставка которого осуществляется с помощью аденовирусного вектора rAAV-rh74 (Manini, 2022).
Бесспорным достижением ПМ в области генетики также является успешная терапия жизнеугрожающего заболевания СМА 5q, которое в большинстве случаев обусловлено гомозиготной делецией экзонов 7-8 гена SMN1(Hjartarson, 2022).
Разработаны разные подходы к терапии, выбор наиболее подходящего зависит от числа копий псевдогена SMN2, определение которых успешно реализуется в клинической практике.
На сегодняшний день в мире применяется три препарата этиотропной и патогенетической терапии:
Разработаны разные подходы к терапии, выбор наиболее подходящего зависит от числа копий псевдогена SMN2, определение которых успешно реализуется в клинической практике.
На сегодняшний день в мире применяется три препарата этиотропной и патогенетической терапии:
- антисмысловые олигонуклеотиды (Нусинерсен),
- модификатор сплайсинг мРНК SMN2 (Рисдиплам),
- генная терапия путем доставки полноразмерной копии гена SMN1 с помощью аденоассоциированного вируса AAV9 (Онасемногена Абепарвовек) (Hjartarson, 2022).
Селективный скрининг болезни Помпе позволяет диагностировать заболевание на раннем клиническом этапе и осуществлять своевременную заместительную терапию данного состояния препаратом Алглюкозидаза альфа (Bolano-Diaz, 2022).
Второй по распространенности мышечной дистрофией является мышечная дистрофия Ландузи – Дежерина (Jagannathan 2022), развитие которой связывают с релаксацией хроматина в области макросаттелитных повторов D4Z4 хромосомы 4 и экспрессией транскрипционного фактора DUX4 (Mocciaro, 2021).
Значительную клиническую эффективность в виде замедления прогрессирования мышечной дистрофии Ландузи – Дежерина показал препарат Лосмапимод, который в настоящее время проходит третью фазу клинический испытаний в разных странах Европы и в США (Leo Wang, 2023).
Значительную клиническую эффективность в виде замедления прогрессирования мышечной дистрофии Ландузи – Дежерина показал препарат Лосмапимод, который в настоящее время проходит третью фазу клинический испытаний в разных странах Европы и в США (Leo Wang, 2023).
- Действие препарата реализуется через ингибирование фермента p38α/β MAPKs, который является модулятором экспрессии транскрипционного фактора DUX4 (Leo Wang, 2023).
Большие надежды дает применение дезоксицитидина и дезокситимидина для лечения синдромов истощения или деплеции митохондриальной ДНК, которые проходят вторую фазу клинических испытаний в настоящее время (ClinicalTrials.gov, ID NCT04802707).
Опубликованы результаты по безопасности и эффективности данного препарата для лечения быстро прогрессирующей митохондриальной миопатии с недостаточностью тимидинкиназы 2 (Domínguez-González, 2019).
Опубликованы результаты по безопасности и эффективности данного препарата для лечения быстро прогрессирующей митохондриальной миопатии с недостаточностью тимидинкиназы 2 (Domínguez-González, 2019).
Выбор давно зарегистрированных лекарственных средств сегодня определяется генотипом конкретного больного при врожденных миастенических синдромах и наследственных эпилепсиях.
- Так, при миастенических синдромах, обусловленных патогенными вариантами в генах DOK7 и COLQ, и при миастении медленных каналов (гены рецептора ацетилхолина) необходимо избегать приема пиридостигмина бромида – препарата, который часто назначается пациентам с миастениями (Engel, 2015).
- При этом существует ряд других препаратов, показанных при данных формах миастенических синдромов, такие как 3,4-диаминопиридин, эфедрин, сальбутамол в пероральной форме.
Благодаря активному внедрению в диагностические схемы обязательного молекулярно-генетического исследования пациентов с наследственными болезнями глаз, в том числе патологии сетчатки и зрительного нерва, позволило установить корректные курабельные клинико-генетические диагнозы.
- В России проведено более 2000 молекулярно-генетических исследований с учетом высокотехнологического современного обследования пациентов.
- Для группы таргетных пациентов стала доступна персонифицированная генная терапия.
- В настоящее время в мире активно внедрен в практику генозаместительный препарат Воретиген непарвовек, показавший положительный эффект.
- Проводимая терапия позволила полностью остановить необратимый дегенеративный процесс в сетчатке в следствии амавроза Лебера 2-го типа и пигментного ретинита 20-го типа, вызываемого мутациями в гене RPE65.
- В европейских странах лечение получили более 250 человек. В России с 2022 г. терапия проведена у 21 ребенка с подтвержденным генетическим диагнозом. Во всех случаях отмечается положительная динамика.
Благодаря персонализированному подходу в диагностике орфанной наследственной патологии органа зрения сформирована группа пациентов таргентных с наследственной атрофией зрительного нерва Лебера, хороидеремии, Х-сцепленным пигментным ретинитом.
Данный подход позволил сформировать единый реестр пациентов с наследственной офтальмопатологией, подтвержденной молекулярно-генетическим методами.
Данный подход позволил сформировать единый реестр пациентов с наследственной офтальмопатологией, подтвержденной молекулярно-генетическим методами.
Редактирование генов нашло применение у пациентов.
- Так терапевтический препарат для редактирования генома на основе ZFN SB-913 был клинически введен пациентам с диагнозом мукополисахаридоз II-го типа.
- Одной из целей этого исследования было оценить влияние SB-913 на активность фермента идуронат-2-сульфатазы (IDS) в лейкоцитах и плазме с целью создать возможность синтеза активного фермента на протяжении всей жизни (NCT03041324).
- Терапия редактирования генома ZFN также тестируется при мукополисахаридозе I-го типа (SB-318, NCT02702115) и тяжелой гемофилии B (SB-FIX, NCT02695160).
Клеточные технологии также широко используются в терапии, одним из примеров включают митохондриальную заместительную терапию (МРТ).
Митохондриальные заболевания могут возникать в результате мутаций в митохондриальной ДНК (мтДНК) и передаются потомству по материнской линии. Для проведения МРТ здоровое ядро из материнской яйцеклетки с измененным митохондриальным геномом переносится в здоровую яйцеклетку с донорскими митохондриями без ядра. По сути, этот подход может привести к получению оплодотворенной яйцеклетки, содержащей ядерную ДНК от двух родителей и митохондриальную ДНК от донора, что позволит предотвратить генетические заболевания у потомства.
Митохондриальные заболевания могут возникать в результате мутаций в митохондриальной ДНК (мтДНК) и передаются потомству по материнской линии. Для проведения МРТ здоровое ядро из материнской яйцеклетки с измененным митохондриальным геномом переносится в здоровую яйцеклетку с донорскими митохондриями без ядра. По сути, этот подход может привести к получению оплодотворенной яйцеклетки, содержащей ядерную ДНК от двух родителей и митохондриальную ДНК от донора, что позволит предотвратить генетические заболевания у потомства.
Мутации в митохондриальной ДНК, особенно в гене 12S rRNA, являются наиболее важными причинами потери слуха.
Обнаружено, что мутации A1555G и C1494T связаны как с индуцированной аминогликозидами, так и с несиндромальной потерей слуха во многих семьях по всему миру.
В некоторых странах скрининг патогенных мутаций мтДНК был рекомендован для раннего выявления, профилактики и диагностики митохондриальной глухоты, особенно в случаях необходимости применения аминогликозидов в неонатальном периоде. Другие исследователи показали возможность проведения такого скринга в рамках неинвазивного пренатального теста (НИПТ).
Обнаружено, что мутации A1555G и C1494T связаны как с индуцированной аминогликозидами, так и с несиндромальной потерей слуха во многих семьях по всему миру.
В некоторых странах скрининг патогенных мутаций мтДНК был рекомендован для раннего выявления, профилактики и диагностики митохондриальной глухоты, особенно в случаях необходимости применения аминогликозидов в неонатальном периоде. Другие исследователи показали возможность проведения такого скринга в рамках неинвазивного пренатального теста (НИПТ).
Основные достижения российской науки и индустрии за последние годы
- Исследование редких, малоизученных и неизвестных заболеваний стало одной из основных современных мировых тенденций клинической медицины и биомедицины.Изучение данной проблемы является одним из приоритетных направлений Центра Алмазова, для чего в рамках работы НЦМУ «Центр персонализированной медицины» реализуется научный проект «Изучение патогенеза редких, малоизученных и неизвестных ранее заболеваний: персонифицированная генетическая диагностика, биомоделирование и поиск новых подходов к терапии и определению прогноза». В марте 2021 г. создан Центр компетенций «Неизвестные, редкие и малоизученные заболевания». Это единая структура, которая объединяет регистры пациентов с редкими заболеваниями, механизмы развития которых малоизучены либо неизвестны, а диагностика и терапия не определена стандартными протоколами, и фундаментальные проекты, направленные на выявление новых конкретных генетических детерминант редкой и неизвестной патологии и раскрытие молекулярных механизмов их развития, создание экспериментальных клеточных и животных моделей как для более глубокого изучения патомеханизмов развития заболеваний, так и для создания и тестирования новых генно-инженерных и генно-терапевтических препаратов для лечения наследственных заболеваний.
- Сегодня регистр Центра Алмазова включает более 400 детей с 75 крайне редкими нозологиями.Приоритетными для исследований являются следующие нозологии: состояния, сопровождающиеся нарушением функции автономной нервной системы – синдром врожденной центральной гиповентиляции; митохондриальные заболевания (болезни с поражением дыхательной цепи митохондрий и ТК-2-ассоциированные митохондриальные миопатии; врожденный гиперинсулинизм и др.).
- Митохондриальные заболевания представляют собой одну из самых частых патологий в группе наследственных заболеваний обмена (1,6:5000 популяции).В центре наблюдаются все российские пациенты с ТК2-ассоциированной митохондриальной миопатией. Пациенты получают экспериментальную терапию дезоксинуклеозидами (дезокситимидин и дезоксицитидин). Показана эффективность данной терапии – нормализация моторного развития при раннем начале терапии, стабилизация состояния при позднем начале. Подготовлены методические рекомендации по диагностике и терапии ТК2-ассоциированной миопатии.
- Состояния, сопровождающиеся нарушением функции автономной нервной системы, в том числе синдром врожденной центральной гиповентиляции
- Состояния, сопровождающиеся нарушением функции автономной нервной системы, в том числе синдром врожденной центральной гиповентиляции (СЦВГ) – в локальном регистре 31 ребенок.
- Выявлены пациенты с очень редким генотипом (PARM) – мутации с удвоением 28 и 33 полиаланиновых повторов, пациент с мутацией с.733 789dup в гетерозиготном состоянии.
На основании анализа базы данных пациентов с СЦВГ выработан персонифицированный алгоритм респираторной поддержки, а также объема и кратности обследования, направленного на выявление проявлений автономной дисрегуляции, в том числе жизнеугрожающих. Оценивается психомоторное и нейрокогнитивное развитие детей. - Впервые описан случай синдрома центральной гиповентиляции (СЦГВ) с мутацией в гене РНОХ2В с формированием экспансии в 36 аланинов, прерванной тремя другими аминокислотами.Подобный тип мутации описан только в экспериментальном исследовании Trochet и соавторов (2005), обнаружившем нормализацию трансактивации и связывания ДНК при прерывании полиаланиновой экспансии.
- Известно, что в 90 % случаев СЦГВ мутация в гене РНОХ2В приводит к удвоению участка полиаланинового повтора с формированием экспансии в 24–33 аминокислоты, причем тяжесть фенотипических проявлений прямо пропорциональна длине полиаланинового тракта с круглосуточной потребностью в искусственной вентиляции при наибольшем числе повторов.
- Нами впервые описан клинический случай, подтверждающий возможную «защитную» роль включения других аминокислот в полиаланиновую экспансию.
- Синдром ROHHAD – заболевание неустановленной этиологии, включающее быстро прогрессирующее ожирение, гиповентиляцию, дисфункцию гипоталамуса и нарушение регуляции вегетативной нервной системы (Rapid-onset Obesity, Hypoventilation, Hypothalamic and Autonomic Dysfunction).Все три ребенка имеют сходные клинические проявления, жизнеугрожающую гиповентиляцию, однако генез данного состояния требует дальнейшего исследования.
- Так, в одном из случаев выявлена мутация в 8 экзоне гена RET (chr10: 43607621G> A, rs75873440): аминокислотная замена в 533 позиции белка (p.Gly533Ser, NM 020975.4), ранее описанная при болезни Гиршпрунга.
- У двух пациенток дебют заболевания произошел после перенесенной COVID-19 пневмонии, принято решение о противовоспалительной терапии внутривенными иммуноглобулинами, на фоне которой отмечено клиническое улучшение.
- Врожденный гиперинсулинизмВрожденный гиперинсулинизм (ВГИ) – врожденное заболевание, в основе которого лежит нерегулируемая автономная гиперпродукция инсулина, которая приводит к тяжелым гипогликемиям и органическому необратимому повреждению головного мозга.
- При несвоевременном оказании помощи дети с данным заболеванием могут погибнуть в раннем возрасте или иметь тяжелое повреждение головного мозга с утратой интеллекта.
- Частота ВГИ составляет около 1:30000–1:50000, по статистике ведущих центров врожденного гиперинсулинизма в мире. В РФ распространенность данного заболевания составляет 1:50638 живых новорожденных (М. Меликян, 2019).
- В отличие от опухолевого гиперинсулинизма (инсулиномы), при ВГИ очаг секреции инсулина невозможно визуализировать обычными методами.
- Единственным способом диагностики этого заболевания является радиоизотопная технология ПЭТ-КТ с радиофармацевтическим препаратом [18F]фтор-L-дигидроксифенилаланин (18F-ДОФА), который по характеру распределения радиофармацевтического препарата позволяет выполнять дифференциальную диагностику фокальной и диффузной форм врожденного гиперинсулинизма, а также определять локализации аденоматозного очага при фокальной форме.
- Для эффективного хирургического лечения необходимо иметь информацию о границах между пораженной и здоровой тканью, поэтому, в соответствии с современным протоколом, необходима многократная интраоперационная биопсия до получения информации о неповрежденной ткани. Учитывая тяжесть общего состояния детей с ВГИ, высокий риск осложнений сопроводительной терапии, для успешного исхода необходимо медицинское сопровождение пациентов опытной бригадой специалистов на всех этапах оказания помощи.
- В «НМИЦ им. В.А. Алмазова» с 2017 г. выполняются все описанные этапы медицинской помощи детям с ВГИ, проведение которых ранее было возможно только при направлении пациентов на лечение за пределы РФ. В настоящее время в клинике Центра оказана помощь более чем 120 детям с ВГИ, все пациенты с фокальными формами были успешно прооперированы и в настоящее время являются здоровыми, не имея нарушений углеводного обмена.
- Пациенты продолжают наблюдаться детскими эндокринологами Центра, периодически получают курсы стационарной медицинской реабилитации. Проводится оценка их роста и развития, неврологического статуса и длительное медицинское сопровождение.
- Совершенствование диагностики врожденного гиперинсулинизма и поиска факторов, влияющих на исходы терапииТакже проводятся научные исследования, направленные на совершенствование диагностики этого редкого заболевания и поиска факторов, влияющих на исходы терапии.
- Установлено, что в ряде случаев при анализе ПЭТ-сканограмм и расчете стандартного панкреатического индекса (ПИ) невозможно сделать заключение о топике процесса, так как ПИ<1,3 считается диагностическим для диффузной формы, а ПИ> 1,5 – для фокальной. Значения между 1,3 и 1,5 не позволяют сделать однозначное заключение, при этом установление формы заболевания является критически важным для принятия последующих тактических решений.
- В ходе исследований научным коллективом «НМИЦ им. В.А. Алмазова» и СПбГЭТУ «ЛЭТИ» был создан программный модуль на основе искусственного интеллекта Python module for differentiating forms of congenital hyperinsulinism 1.1 и разработана диагностическая технология с расчетом нового коэффициента, получившего название «Цветовой панкреатический индекс» (ЦПИ), имеющего сопоставимую с ПИ специфичность и более высокую чувствительность.
- Применение данного индекса позволило более точно определять топику форм ВГИ, ранее представлявших большую диагностическую сложность. Программный модуль успешно используется в диагностике форм ВГИ, оптимизируя диагностику морфологических форм ВГИ, что важно для принятия решений и позволяет персонализованно подходить к оказанию помощи детям с ВГИ. Создан Центр компетенций «Оказание помощи детям с врожденным гиперинсулинизмом», в котором оказывается помощь экспертного уровня детям не только из РФ, но из стран ближнего зарубежья.
Накопленный клинический опыт наблюдения и лечения пациентов с наследственными и редкими заболеваниями, в том числе с лизосомными болезнями накопления, наследственными болезнями обмена, нейромышечными заболеваниями, множественными врожденными пороками развития, острым неонатальным поражением печени, наследственными двигательными расстройствами, сформированные мультидисциплинарные команды врачей-специалистов, доступность лабораторных и молекулярно-генетических тестов, возможность целевого использования средств реализации научных проектов может стать платформой для исследования новых возможностей генной терапии.

